ヒスタミン
堀尾修平
徳島大学大学院 医歯薬学研究部 分子情報薬理学分野
DOI:10.14931/bsd.7520 原稿受付日:2018年3月1日 原稿完成日:2018年3月25日
担当編集委員:林 康紀(京都大学大学院 医学研究科 システム神経薬理学分野)
英語名:histamine 独:Histamin 仏:histamine
ヒスタミンは生体内で、アミノ酸であるヒスチジンから合成される。末梢では主に肥満細胞に貯えられ、刺激に応じて放出されアレルギー反応に関与する。また、摂食によってエンテロクロマフィン様細胞から遊離され、胃酸分泌に関与する。中枢では、視床下部乳頭体にヒスタミンニューロンが集まっており、そこから脳内各部位に投射し、神経伝達物質として働いている。睡眠・覚醒、摂食調節などに関与している。
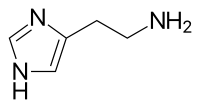
| ヒスタミン | |
|---|---|
| |
| |
2-(1H-Imidazol-4-yl)ethanamine | |
別称 1H-Imidazole-5-ethanamine, 2-(4-Imidazolyl)ethanamine, 2-(1H-Imidazol-4-yl)ethylamine , 2-(1H-Imidazol-5-yl)ethylamine, β-Imidazolyl-4-ethylamine | |
| Identifiers | |
| 51-45-6 | |
| ChEBI | |
| ChEMBL | ChEMBL90 |
| ChemSpider | 753 |
| |
| 1204 | |
| Jmol-3D images | Image |
| KEGG | D08040 |
| MeSH | Histamine |
| PubChem | 774 |
| |
| UNII | 820484N8I3 |
| Properties | |
| C5H9N3 | |
| Molar mass | 111.148 g·mol−1 |
| Melting point | 83.5 °C (182.3 °F; 356.6 K) |
| Boiling point | |
| Easily soluble in cold water, hot water[1] | |
| Solubility in other solvents | Easily soluble in methanol. Very slightly soluble in diethyl ether.[1] Easily soluble in ethanol. |
| log P | −0.7[2] |
| Acidity (pKa) | Imidazole: 6.04 Terminal NH2: 9.75[2] |
| 特記なき場合、データは常温(25 °C)・常圧(100 kPa)におけるものである。 | |
発見
ヒスタミンは、1907年にWindausとVogtによって化学的に合成された[3]。その後、Daleらにより様々な生理作用を持つことが示されたが、ようやく1927年になって、哺乳動物の種々の組織に含まれることが明らかにされ[4]、実際に生体内で働いている物質であることが判った。ヒスチジン由来のアミンという意味でヒスタミンと命名されたが[5]、組織(histos)由来のアミンから命名されたという説明もある[6]。
生合成
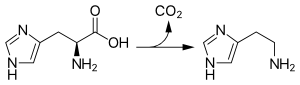
イミダゾール骨格にエチルアミンの側鎖を有する構造である。哺乳動物のほとんどすべての組織に含まれる。アミノ酸であるL-ヒスチジンから、L-ヒスチジン脱炭酸酵素(L-histidine decarboxylase: HDC)による脱炭酸反応により生合成される(図1)。
ヒスタミンは、細菌、すなわち海洋性ヒスタミン産生菌及び腸内ヒスタミン産生菌でも、ヒスチジンからHDCにより合成される。魚を食べた時に、魚肉中で繁殖した細菌により合成されたヒスタミンを体内に取り込み食中毒(じんましん等)を起こすことがある。ヒスタミンは一般には腸管から吸収される量は少ないものの、一部は吸収されることによる。
分布
哺乳動物組織では、ヒスタミンの大部分は、肥満細胞(mast cell)に存在する。血液中の好塩基球、胃粘膜のエンテロクロマフィン様細胞(enterochromaffin-like cell: ECL cell)にも存在する。脳内では、ヒスタミン神経に伝達物質として存在するが、肥満細胞、グリア細胞、血管内皮細胞にも存在する。ヒスタミンは血液脳関門を通過しない。
軟体動物(アメフラシ: Aplysia)[7]、昆虫(ショウジョウバエ: Drosophila)[8]、魚類(ゼブラフィッシュ: zebrafish)[9]などの神経系にもヒスタミンが伝達物質として存在するが、線虫(C. elegans)[10]の神経系には存在しない。
代謝
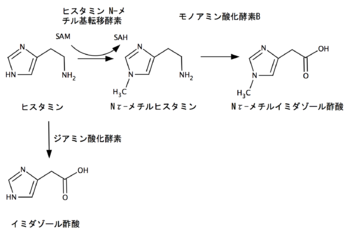
SAM:S-アデノシルメチオニン、SAH: S-アデノシルホモシステイン
代謝経路は2種類ある(図2)。
- ヒスタミンN-メチル基転移酵素(histamine N-methytransferase: HNMT)によりメチル化を受け、さらにモノアミン酸化酵素(monoamine oxidase: MAO)により酸化され、Nτ-メチルイミダゾール酢酸に代謝される。
- ジアミン酸化酵素(diamine oxidase: DAO)により酸化的脱アミノ化され、イミダゾール酢酸に代謝される。
脳では、HNMTにより不活性化される[11]。末梢組織では、主にDAOにより代謝される。神経終末への取り込みによる不活性化機構はないと考えられている。
貯蔵と放出
肥満細胞では、合成されたヒスタミンは細胞質の粗大分泌顆粒に貯蔵されている。細胞表面にIgE受容体を発現しており、そこにIgEが結合すると感作肥満細胞となる。IgEに特異的な抗原(アレルゲン)が結合すると架橋が形成され、それがトリガーとなって、脱顆粒によりヒスタミンが放出される。好塩基球もほぼ同様のメカニズムでヒスタミンを貯蔵、放出する。胃粘膜に存在するエンテロクロマフィン様細胞からは、摂食に伴ってヒスタミンが遊離され、壁細胞に作用し胃酸が分泌される。神経細胞では、小胞モノアミントランスポーター(vesicular monoamine-transporter: VMAT-2)によりシナプス小胞に輸送され貯蔵される[12]。
受容体
脊椎動物
現在、H1受容体、H2受容体、H3受容体、H4受容体の4種類が同定されている。いずれも、Gタンパク質共役型受容体である。
H1受容体
脳では、神経細胞とグリア細胞に発現している。神経細胞では、脱分極もしくは発火頻度の上昇を引き起こす。末梢では、気管支、腸管などの平滑筋、血管内皮細胞、副腎髄質細胞などに分布している。アレルギー反応を引き起こす主要原因である。
H2受容体
神経細胞とグリア細胞に発現している。神経細胞に対して興奮性に作用する。末梢では主に胃壁細胞に存在し、胃酸分泌に関与している。H2阻害薬は、胃潰瘍治療薬として用いられている。
H3受容体
ヒスタミン神経終末部のシナプス前膜に存在し、ヒスタミンの合成および遊離を抑制する。また、他の神経系のシナプス前膜にも存在し、アセチルコリン、セロトニン、ノルアドレナリン、ドパミン、グルタミン酸、GABAの遊離を抑制する。選択的スプライシングにより複数のアイソフォームが存在する[13]。
H4受容体
H4受容体が中枢に存在するという確証は得られていない[14]。末梢では、骨髄、好酸球、Tリンパ球、マスト細胞などに存在する。とくに免疫系の細胞に発現が多く見られ、炎症やアレルギーへの関与が考えられるため、抗炎症薬、抗アレルギー薬の標的分子の候補となっている。
| 受容体 | 遺伝子 | Allen Brain Atlas | 細胞内情報伝達 | 作動薬 | 阻害薬 |
|---|---|---|---|---|---|
| H1受容体 | HRH1 | 69257755 | Gq/11 ホスホリパーゼC活性化 IP3とDG産生 |
2-メチルヒスタミン ヒスタプロジフェン |
ジフェンヒドラミン クロルフェニラミン メピラミン(ピリラミン) プロメタジン ドキセピン テルフェナジン フェキソフェナジン エバスチン エピナスチン セチリジン ロラタジン |
| H2受容体 | HRH2 | 69257761 | Gs アデニル酸シクラーゼ活性化 cAMP上昇 |
4-メチルヒスタミン アムタミン ジマプリット |
シメチジン ラニチジン ファモチジン チオチジン ブリマミド |
| H3受容体 | HRH3 | 71393412 | Gi/o アデニル酸シクラーゼ抑制 cAMP濃度低下、細胞内Ca2+濃度上昇 |
(R)-α-メチルヒスタミン イメピップ イメティット プロキシファン |
チオペラミド グロベンプロピット シプロキシファン プロキシファン MK-0249 |
| H4受容体 | HRH4 | 69257767 | Gi/o アデニル酸シクラーゼ抑制 cAMP濃度低下、細胞内Ca2+濃度上昇 |
クロザピン 4-メチルヒスタミン ST-1006 VUF-8430 |
チオペラミド JNJ-7777120 VUF-6002(JNJ-10191584) JNJ-39758979 |
文献[15]、IUPHAR/BPS Guide to Pharmacologyから作製。
ヒスタミンがGABAA受容体に作用するという報告がある[16]。また、ヒスタミンは、NMDA型グルタミン酸受容体を、そのポリアミン結合部位に作用して活性化させる[17][18]。
無脊椎動物
無脊椎動物では、上記のヒスタミン受容体の存在は示されていない。一方で、ショウジョウバエにおいて、histamine-gated chloride channels (HisCl1およびHisCl2) が同定されている[19][20]。これらは、視覚情報の伝達に重要な働きをしている[21]。脊椎動物にこれらのチャンネルが存在するかどうかはまだ不明である[22]。
リガンド
作動薬
H1受容体作動薬としては、2-メチルヒスタミン、ヒスタプロジフェン、H2受容体作動薬としては、4-メチルヒスタミン、アムタミン, ジマプリット、H3受容体作動薬としては、(R)-α-メチルヒスタミン、イメピップ、イメティット、H4受容体作動薬としては、クロザピン、4-メチルヒスタミンがある。
このうち、H4受容体作動薬のクロザピンは、セロトニン5-HT2A、ドーパミンD4、ムスカリン性アセチルコリンM1,アドレナリンα1受容体に阻害作用を示し、統合失調症治療薬として用いられている。
阻害薬
H1受容体阻害薬は一般に抗ヒスタミン薬と言われているものである。第一世代H1受容体阻害薬には、ジフェンヒドラミン、クロルフェニラミン、メピラミン(ピリラミン)、プロメタジンなどがあり、第二世代H1受容体阻害薬には、フェキソフェナジン、エバスチン、エピナスチン、セチリジンなどがある。これらは、蕁麻疹、アトピー性皮膚炎、アレルギー性鼻炎などのアレルギー疾患に対する第一選択薬である。第一世代の阻害薬は、血液脳関門を通過して脳内に入るため、中枢抑制作用による眠気、抗コリン作用による口渇などの副作用が出る。第二世代の阻害薬は血液脳関門を通過しにくいためこれらの副作用は少なく、通常はこちらを選択すべきである。
H2受容体阻害薬には、シメチジン、ファモチジン、ラニチジンなどがある。消化性潰瘍治療薬として用いられる。
H3受容体阻害薬には、チオペラミド、クロベンプロピット、プロキシファンがある。H3阻害薬は、アルツハイマー病、注意欠陥・多動性障害(ADHD)、統合失調症、多発性硬化症の治療薬としての開発が進められている。
H4受容体阻害薬には、チオペラミド、JNJ-7777120(Johnson & Johnson社)がある。アレルギー性疾患や、リューマチなどの自己免疫疾患の治療薬としての可能性がある。
逆作動薬
受容体は、活性化状態と不活性化状態という2つの状態(コンフォメーション)をとりうる。作動薬が結合した場合には、ほとんどが活性化状態になる。作動薬がない状況では、大部分は不活性化状態にあるが一部は活性化状態にある。従って、わずかではあるが、受容体シグナル伝達が起こっている。阻害薬は、通常受容体結合部位に結合して、作動薬の結合を邪魔する(受容体に結合するが反応を起こさない)ものを言う。その定義においては、阻害薬は、受容体の活性化状態、不活性化状態の割合に影響を与えない。
逆作動薬(インバースアゴニスト)は、受容体のほとんどを不活性状態に移行させるものを言う。従って逆作動薬が存在すると、作動薬がなくてもわずかに起こっていた受容体反応を抑えることができる。この概念が有用になるのは、例えばアレルギー性鼻炎におけるH1受容体の例である。この症状が進んだ場合にはH1受容体レベルの上昇が考えられる[23]。すると、ヒスタミンが遊離されていない場合でも、H1受容体反応が進行しアレルギー反応が出てしまう。この反応はさらにH1受容体レベルを上げる。この悪循環を断ち切るには、H1受容体の逆作動薬を、できる限り早期に利用するのが有効である[24]。ほとんどのH1受容体阻害薬は逆作動薬である。
H1受容体の結晶構造がX線解析から明らかになった[25]。逆作動薬であるドキセピンが結合した不活性化状態の構造を見たものである。今後さらに特異性の高いH1阻害薬の開発に役立つと考えられる。
H3受容体、H4受容体は恒常的活性がかなり高い受容体である[26][27](すなわち、作動薬がなくても受容体のかなりの割合が活性化状態にある)。H3受容体阻害薬のチオペラミド、クロベンプロピットは逆作動薬である。H4受容体阻害薬のチオペラミド、JNJ-7777120は、動物種によって、逆作動薬、部分逆作動薬、部分作動薬、ニュートラルアンタゴニストと性質が異なるので注意が必要である[15]。
末梢機能
H1受容体を介して、気管支平滑筋収縮、腸管収縮、血管平滑筋弛緩、血管透過性亢進、Th1細胞活性化[28]、第一次求心性線維のC線維上に存在して痒みを中枢に伝える作用などがある。
H2受容体を介して、胃酸分泌促進、心臓への陽性変時・陽性変力作用、Th1、Th2細胞の活性化を抑制する作用[28]等がある。
H4受容体を介して、マスト細胞、好酸球の遊走を引き起こす。炎症、アレルギー反応に関与する。
ヒスタミン神経系
解剖学的特徴
ヒスタミンニューロン細胞体は、視床下部乳頭体(tuberomamillary nucleus)に集まっている。E1, E2, E3, E4, E5の5つの亜核に分類されている[29][30]。そこから脳内の各部位に投射している[31][32]。大脳皮質、扁桃体、黒質、線条体、海馬、視床、視床下部、小脳、脳幹部、脊髄などである。ヒスタミン神経の終末部位はバリコシティ(varicosity)と呼ばれるこぶ上の膨らみを多数形成し、そこのシナプス小胞からヒスタミンが遊離される。密接なシナプスの形成は殆ど見られない。
ヒスタミンニューロンに発現している受容体として、GABAA受容体、GABAB受容体、ニコチン性アセチルコリン受容体、セロトニン5-HT2受容体、AMPA型グルタミン酸受容体、NMDA型グルタミン酸受容体、オレキシン受容体、TRH受容体、グリシン受容体、P2X受容体、P2Y受容体、ガラニン受容体が判っている[32]。
ヒスタミンニューロンは自発発火をしている[32]。主な投射先である視床下部において、ヒスタミン遊離量は活動期に多く、休息期に少ないという日内リズムを示す[33]。
上述のように、ヒスタミンニューロンは様々な脳部位からの入力を受け、神経線維を脳のほとんどすべての部位に送っている。ヒスタミンニューロンは均一ではなく、入力を受ける脳部位、投射部位に従って種々のタイプが存在すると考えられる[34]。
H1受容体は、主として視床下部、脳幹、視床、大脳皮質に発現が見られ、H2受容体は、大脳基底核、扁桃体、海馬、大脳皮質に発現が見られる[32]。H3受容体は各種の神経系のシナプス前膜に存在し、ヒスタミンの他、アセチルコリン、セロトニン、ノルアドレナリン、ドーパミン、グルタミン酸、GABAの遊離を抑制する。
機能
ヒスタミンの中枢機能は、2つに大別される。
- 脳内各ニューロンに存在するH1受容体、あるいはH2受容体刺激を介した作用
- ニューロン終末部位のH3受容体に作用し、ヒスタミン、ドーパミン、ノルアドレナリン、セロトニンなどの遊離抑制による作用
H1受容体、H2受容体を介した機能としては、睡眠・覚醒[35]、学習記憶[36]、食欲調節[37]などがある。これらの機能を担う神経回路の特定のニューロンに、H1受容体、あるいはH2受容体が発現していて、ヒスタミンが作用することによりニューロン活動を調節(modulate)していると考えられる。
H3受容体を介した機能としては、各種伝達物質の遊離調節によるものが考えられる。H3受容体がもともと恒常的活性が高い受容体であることを考えると、正常時は脳全般の活動を大まかに調節していると考えてよい。むしろ、H3受容体逆作動薬の作用が重要であり、各種伝達物質の遊離量を増やすことで、種々の病態の改善が期待できる[38][39]。
精神疾患との関連
パーキンソン病患者では、黒質、被殻、淡蒼球でヒスタミンレベルが顕著に増加している[40]。H3受容体に作用してドパミン遊離低下が起こっている可能性がある。統合失調症患者の前頭前皮質、帯状回のH1受容体量が減少している[41][42]。アルツハイマー病患者では、前頭葉、側頭葉でヒスタミンレベルが低下している[43]。
H3受容体は各種の神経系のシナプス前膜に存在し、ヒスタミンの他、アセチルコリン、セロトニン、ノルアドレナリン、ドーパミン、グルタミン酸、GABAの遊離を抑制する。H3受容体阻害薬は、これらの抑制を解除し遊離量を増やすため、アルツハイマー病、注意欠陥・多動性障害(ADHD)、統合失調症、多発性硬化症の治療薬となる可能性がある[38][39][44]。
ヒスタミンは動揺病(乗り物酔い)の原因となる。空間認知の情報処理における齟齬からヒスタミンニューロンが活性化され、嘔吐中枢のH1受容体を活性化することによる。
てんかん発作に対しては、ヒスタミンがH1受容体を介して抑制すること、H3受容体阻害薬が抑制すること、逆にH1受容体阻害薬は発作を悪化させること等が考えられているが、まだ確定していない[45]。
関連項目
参考文献
- ↑ 1.0 1.1 Histamine Material Safety Data Sheet (Technical report). sciencelab.com. 2013-05-21.
- ↑ 2.0 2.1
Vuckovic, D., & Pawliszyn, J. (2011).
Systematic evaluation of solid-phase microextraction coatings for untargeted metabolomic profiling of biological fluids by liquid chromatography-mass spectrometry. Analytical chemistry, 83(6), 1944-54. [PubMed:21332182] [WorldCat] [DOI] - ↑ Windaus A, Vogt W
Synthese des Imidazolyl-äthylamins.
Ber. Dtsch. Chem. Gess: 1907, 40:3691–3695 PDF - ↑
Best, C.H., Dale, H.H., Dudley, H.W., & Thorpe, W.V. (1927).
The nature of the vaso-dilator constituents of certain tissue extracts. The Journal of physiology, 62(4), 397-417. [PubMed:16993860] [PMC] [WorldCat] [DOI] - ↑
Dale, H.H., & Richards, A.N. (1918).
The vasodilator action of histamine and of some other substances. The Journal of physiology, 52(2-3), 110-65. [PubMed:16993411] [PMC] [WorldCat] [DOI] - ↑ Brunton LL ed.
Goodman & Gilman's the pharmacological basis of therapeutics, 12th edition
McGraw-Hill Medical: 2011 - ↑
Elste, A., Koester, J., Shapiro, E., Panula, P., & Schwartz, J.H. (1990).
Identification of histaminergic neurons in Aplysia. Journal of neurophysiology, 64(3), 736-44. [PubMed:2230920] [WorldCat] [DOI] - ↑
Goitia Aular, M., & de Boiso, J.F. (1982).
[Culture of Trypanosoma cruzi (Elpidio Padrón strain) in a semidefined medium. Effect of variations in its composition and condition]. Cultivo del Trypanosoma cruzi (cepa Elpidio Padrón) en un medio semidefinido. Efecto de algunas variaciones en la composición y condiciones del mismo. Acta cientifica venezolana, 33(6), 488-96. [PubMed:6765065] [WorldCat] - ↑
Sundvik, M., & Panula, P. (2012).
Organization of the histaminergic system in adult zebrafish (Danio rerio) brain: neuron number, location, and cotransmitters. The Journal of comparative neurology, 520(17), 3827-45. [PubMed:22522821] [WorldCat] [DOI] - ↑
Pokala, N., Liu, Q., Gordus, A., & Bargmann, C.I. (2014).
Inducible and titratable silencing of Caenorhabditis elegans neurons in vivo with histamine-gated chloride channels. Proceedings of the National Academy of Sciences of the United States of America, 111(7), 2770-5. [PubMed:24550306] [PMC] [WorldCat] [DOI] - ↑
Barnes, W.G., & Hough, L.B. (2002).
Membrane-bound histamine N-methyltransferase in mouse brain: possible role in the synaptic inactivation of neuronal histamine. Journal of neurochemistry, 82(5), 1262-71. [PubMed:12358773] [WorldCat] [DOI] - ↑
Puttonen, H.A.J., Semenova, S., Sundvik, M., & Panula, P. (2017).
Storage of neural histamine and histaminergic neurotransmission is VMAT2 dependent in the zebrafish. Scientific reports, 7(1), 3060. [PubMed:28596586] [PMC] [WorldCat] [DOI] - ↑
Leurs, R., Bakker, R.A., Timmerman, H., & de Esch, I.J. (2005).
The histamine H3 receptor: from gene cloning to H3 receptor drugs. Nature reviews. Drug discovery, 4(2), 107-20. [PubMed:15665857] [WorldCat] [DOI] - ↑
Schneider, E.H., Neumann, D., & Seifert, R. (2015).
Histamine H4-receptor expression in the brain? Naunyn-Schmiedeberg's archives of pharmacology, 388(1), 5-9. [PubMed:25420523] [WorldCat] [DOI] - ↑ 15.0 15.1
Panula, P., Chazot, P.L., Cowart, M., Gutzmer, R., Leurs, R., Liu, W.L., ..., & Haas, H.L. (2015).
International Union of Basic and Clinical Pharmacology. XCVIII. Histamine Receptors. Pharmacological reviews, 67(3), 601-55. [PubMed:26084539] [PMC] [WorldCat] [DOI] - ↑
Saras, A., Gisselmann, G., Vogt-Eisele, A.K., Erlkamp, K.S., Kletke, O., Pusch, H., & Hatt, H. (2008).
Histamine action on vertebrate GABAA receptors: direct channel gating and potentiation of GABA responses. The Journal of biological chemistry, 283(16), 10470-5. [PubMed:18281286] [WorldCat] [DOI] - ↑
Bekkers, J.M. (1993).
Enhancement by histamine of NMDA-mediated synaptic transmission in the hippocampus. Science (New York, N.Y.), 261(5117), 104-6. [PubMed:8391168] [WorldCat] [DOI] - ↑
Vorobjev, V.S., Sharonova, I.N., Walsh, I.B., & Haas, H.L. (1993).
Histamine potentiates N-methyl-D-aspartate responses in acutely isolated hippocampal neurons. Neuron, 11(5), 837-44. [PubMed:8240807] [WorldCat] [DOI] - ↑
Gisselmann, G., Pusch, H., Hovemann, B.T., & Hatt, H. (2002).
Two cDNAs coding for histamine-gated ion channels in D. melanogaster. Nature neuroscience, 5(1), 11-2. [PubMed:11753412] [WorldCat] [DOI] - ↑
Zheng, Y., Hirschberg, B., Yuan, J., Wang, A.P., Hunt, D.C., Ludmerer, S.W., ..., & Cully, D.F. (2002).
Identification of two novel Drosophila melanogaster histamine-gated chloride channel subunits expressed in the eye. The Journal of biological chemistry, 277(3), 2000-5. [PubMed:11714703] [WorldCat] [DOI] - ↑
Hardie, R.C. (1989).
A histamine-activated chloride channel involved in neurotransmission at a photoreceptor synapse. Nature, 339(6227), 704-6. [PubMed:2472552] [WorldCat] [DOI] - ↑
Fleck, M.W., Thomson, J.L., & Hough, L.B. (2012).
Histamine-gated ion channels in mammals? Biochemical pharmacology, 83(9), 1127-35. [PubMed:22192818] [WorldCat] [DOI] - ↑ 堀尾修平
ヒスタミン受容体をめぐるクロストーク
生物物理: 50:290-293 :2010 - ↑
Kitamura, Y., Nakagawa, H., Fujii, T., Sakoda, T., Enomoto, T., Mizuguchi, H., ..., & Takeda, N. (2015).
Effects of antihistamine on up-regulation of histamine H1 receptor mRNA in the nasal mucosa of patients with pollinosis induced by controlled cedar pollen challenge in an environmental exposure unit. Journal of pharmacological sciences, 129(3), 183-7. [PubMed:26598006] [WorldCat] [DOI] - ↑
Shimamura, T., Shiroishi, M., Weyand, S., Tsujimoto, H., Winter, G., Katritch, V., ..., & Iwata, S. (2011).
Structure of the human histamine H1 receptor complex with doxepin. Nature, 475(7354), 65-70. [PubMed:21697825] [PMC] [WorldCat] [DOI] - ↑
Morisset, S., Rouleau, A., Ligneau, X., Gbahou, F., Tardivel-Lacombe, J., Stark, H., ..., & Arrang, J.M. (2000).
High constitutive activity of native H3 receptors regulates histamine neurons in brain. Nature, 408(6814), 860-4. [PubMed:11130725] [WorldCat] [DOI] - ↑
Wifling, D., Löffel, K., Nordemann, U., Strasser, A., Bernhardt, G., Dove, S., ..., & Buschauer, A. (2015).
Molecular determinants for the high constitutive activity of the human histamine H4 receptor: functional studies on orthologues and mutants. British journal of pharmacology, 172(3), 785-98. [PubMed:24903527] [PMC] [WorldCat] [DOI] - ↑ 28.0 28.1
Jutel, M., Watanabe, T., Klunker, S., Akdis, M., Thomet, O.A., Malolepszy, J., ..., & Akdis, C.A. (2001).
Histamine regulates T-cell and antibody responses by differential expression of H1 and H2 receptors. Nature, 413(6854), 420-5. [PubMed:11574888] [WorldCat] [DOI] - ↑
Miklós, I.H., & Kovács, K.J. (2003).
Functional heterogeneity of the responses of histaminergic neuron subpopulations to various stress challenges. The European journal of neuroscience, 18(11), 3069-79. [PubMed:14656302] [WorldCat] [DOI] - ↑ 千葉政一, 森脇千夏, 伊奈啓輔, 藤倉義久
摂食と肥満における視床下部神経ヒスタミンの役割
創薬へ向けて 日本薬理学雑誌: 147:48-55 :2016 - ↑
Haas, H., & Panula, P. (2003).
The role of histamine and the tuberomamillary nucleus in the nervous system. Nature reviews. Neuroscience, 4(2), 121-30. [PubMed:12563283] [WorldCat] [DOI] - ↑ 32.0 32.1 32.2 32.3
Haas, H.L., Sergeeva, O.A., & Selbach, O. (2008).
Histamine in the nervous system. Physiological reviews, 88(3), 1183-241. [PubMed:18626069] [WorldCat] [DOI] - ↑
Mochizuki, T., Yamatodani, A., Okakura, K., Horii, A., Inagaki, N., & Wada, H. (1992).
Circadian rhythm of histamine release from the hypothalamus of freely moving rats. Physiology & behavior, 51(2), 391-4. [PubMed:1313592] [WorldCat] [DOI] - ↑
Blandina, P., Munari, L., Provensi, G., & Passani, M.B. (2012).
Histamine neurons in the tuberomamillary nucleus: a whole center or distinct subpopulations? Frontiers in systems neuroscience, 6, 33. [PubMed:22586376] [PMC] [WorldCat] [DOI] - ↑
Lin, J.S., Anaclet, C., Sergeeva, O.A., & Haas, H.L. (2011).
The waking brain: an update. Cellular and molecular life sciences : CMLS, 68(15), 2499-512. [PubMed:21318261] [PMC] [WorldCat] [DOI] - ↑
Passani, M.B., Benetti, F., Blandina, P., Furini, C.R.G., de Carvalho Myskiw, J., & Izquierdo, I. (2017).
Histamine regulates memory consolidation. Neurobiology of learning and memory, 145, 1-6. [PubMed:28838882] [WorldCat] [DOI] - ↑
Masaki, T., & Yoshimatsu, H. (2006).
The hypothalamic H1 receptor: a novel therapeutic target for disrupting diurnal feeding rhythm and obesity. Trends in pharmacological sciences, 27(5), 279-84. [PubMed:16584790] [WorldCat] [DOI] - ↑ 38.0 38.1
Leurs, R., Vischer, H.F., Wijtmans, M., & de Esch, I.J. (2011).
En route to new blockbuster anti-histamines: surveying the offspring of the expanding histamine receptor family. Trends in pharmacological sciences, 32(4), 250-7. [PubMed:21414671] [WorldCat] [DOI] - ↑ 39.0 39.1
Vohora, D., & Bhowmik, M. (2012).
Histamine H3 receptor antagonists/inverse agonists on cognitive and motor processes: relevance to Alzheimer's disease, ADHD, schizophrenia, and drug abuse. Frontiers in systems neuroscience, 6, 72. [PubMed:23109919] [PMC] [WorldCat] [DOI] - ↑
Rinne, J.O., Anichtchik, O.V., Eriksson, K.S., Kaslin, J., Tuomisto, L., Kalimo, H., ..., & Panula, P. (2002).
Increased brain histamine levels in Parkinson's disease but not in multiple system atrophy. Journal of neurochemistry, 81(5), 954-60. [PubMed:12065607] [WorldCat] [DOI] - ↑
Nakai, T., Kitamura, N., Hashimoto, T., Kajimoto, Y., Nishino, N., Mita, T., & Tanaka, C. (1991).
Decreased histamine H1 receptors in the frontal cortex of brains from patients with chronic schizophrenia. Biological psychiatry, 30(4), 349-56. [PubMed:1912125] [WorldCat] [DOI] - ↑
Iwabuchi, K., Ito, C., Tashiro, M., Kato, M., Kano, M., Itoh, M., ..., & Yanai, K. (2005).
Histamine H1 receptors in schizophrenic patients measured by positron emission tomography. European neuropsychopharmacology : the journal of the European College of Neuropsychopharmacology, 15(2), 185-91. [PubMed:15695063] [WorldCat] [DOI] - ↑
Higuchi, M., Yanai, K., Okamura, N., Meguro, K., Arai, H., Itoh, M., ..., & Sasaki, H. (2000).
Histamine H(1) receptors in patients with Alzheimer's disease assessed by positron emission tomography. Neuroscience, 99(4), 721-9. [PubMed:10974435] [WorldCat] [DOI] - ↑
Lin, J.S., Sergeeva, O.A., & Haas, H.L. (2011).
Histamine H3 receptors and sleep-wake regulation. The Journal of pharmacology and experimental therapeutics, 336(1), 17-23. [PubMed:20864502] [WorldCat] [DOI] - ↑
Bhowmik, M., Khanam, R., & Vohora, D. (2012).
Histamine H3 receptor antagonists in relation to epilepsy and neurodegeneration: a systemic consideration of recent progress and perspectives. British journal of pharmacology, 167(7), 1398-414. [PubMed:22758607] [PMC] [WorldCat] [DOI]