DCC
桝 正幸、桝 和子
筑波大学 医学医療系 分子神経生物学
DOI:10.14931/bsd.7315 原稿受付日:2016年12月30日 原稿完成日:2016年月日
担当編集委員:村上 富士夫(大阪大学 大学院生命機能研究科)
英:Deleted in Colorectal Cancer
軸索ガイダンス分子ネトリンの受容体の1つであり、胎児期の神経回路形成に関わる。線虫、ショウジョウバエからヒトまで系統を超えて保存されたファミリーを形成する。1990年、大腸癌の進展に伴って起こる染色体欠失部位に存在する腫瘍抑制遺伝子の候補分子として同定された(それがこの分子の名前の由来である)が、その後、ネトリン受容体としての機能が明らかにされた。線虫UNC-40の相同遺伝子であり、DCC/UNC-40ファミリーと総称されることもある。免疫グロブリンスーパーファミリーに属する膜1回貫通分子であり、ネトリンが結合すると軸索誘引活性を発揮する。別種のネトリン受容体であるUNC5と共に機能すると、ネトリンに対して軸索反発活性を示す。最近、dependence receptor(リガンドが存在しない時アポトーシスを引き起こす受容体)としての機能も注目されている。
DCCとは
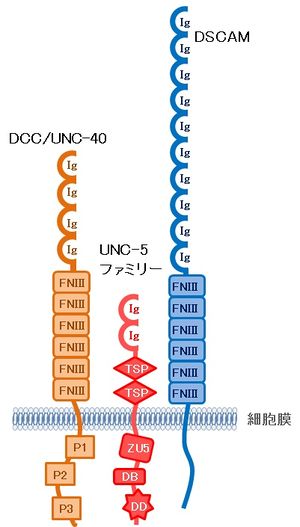
[1]より引用、改変。
大腸癌の70%では進展に伴い18番染色体18q21の欠失が起こることから、この領域に腫瘍抑制遺伝子があると想定されていた。その候補分子として同定されたのがDCCである[2]。多くの癌でDCCの発現が低下すること、DCCの欠失が患者の予後と相関すること、逆に形質転換した細胞にDCCを異所性に発現させると腫瘍原性が低下することなどの事実から、DCCが腫瘍抑制遺伝子として働く可能性があると考えられているが、因果関係を示すデータは無く、DCCが腫瘍抑制遺伝子であることは証明されていない。
1996年、3つのグループの遺伝学的・分子細胞生物学的研究により、 哺乳動物のDCC、線虫のUNC-40、ショウジョウバエのFrazzledがネトリン受容体であることが報告された[3] [4] [5]。UNC-40は、線虫の体周方向の神経軸索伸張に異常を持つ変異体であり、線虫のネトリンであるUNC-6依存性に働くことからネトリンの受容体である可能性が示唆されていた[6]。特にUNC-6へ向かって伸張する軸索の走行に異常が観察されることから、遺伝学的に誘引性のネトリン受容体と考えられた。DCCは、ネトリンに誘導される脊髄交連神経細胞に発現すること、ネトリンタンパク質と高い親和性で結合すること、抗DCC抗体がネトリン依存性の軸索誘引を阻害することから、DCCがネトリンの受容体であることが明らかにされた[3]。その後、DCCノックアウトマウスにおいて、脊髄交連神経が形成されないこと、その異常がネトリン-1ノックアウトマウスの異常と同一であることが示され、ネトリン—DCCシグナルが脊髄交連神経の形成に必要なことが証明された[7]。
分子構造
細胞膜を1回貫通する1型膜タンパク質である。細胞外に4つの免疫グロブリン様ドメインと6つのフィブロネクチン・タイプIIIドメインを持ち、細胞内には3つの保存された領域(P1~P3モチーフ)を持つ[3] [1]。パラログであるネオゲニン(neogenin)はDCCと50%の相同性を示す[3]。線虫のUNC-40、ショウジョウバエのFrazzledはDCCの相同遺伝子であり、同じドメイン構造を持つ[4] [5] [1]。
軸索反発作用を伝えるネトリン受容体UNC5(哺乳動物ではUNC5A-Dの4種類が存在する)も免疫グロブリンスーパーファミリーに属する膜1回貫通分子であり、細胞外領域に2つの免疫グロブリン様ドメインと2つのトロンボスポンジン・タイプI リピートを持つ[1] [8]。細胞内には、zona occludens 1に相同な ZU-5ドメイン、DCC結合(DB)ドメイン、deathドメイン(DD)を持つ。
DSCAMはダウン症候群で重複している遺伝子として同定されたが、ネトリンの受容体としても働く[9]。免疫グロブリンスーパーファミリーに属する膜1回貫通分子であり、細胞外に10個の免疫グロブリン様ドメインと6つのフィブロネクチン・タイプ IIIドメインを持つ。
機能
タンパク質としての機能
DCCとネオゲニンは、ネトリンと結合し、軸索の誘引を行う[3]。ネトリン1は、DCC細胞外領域の4番目・5番目のフィブロネクチンtype IIIドメインと結合する。DCCにネトリンが結合すると、細胞内のP3ドメインを介してDCCが二量体化し、細胞内シグナル系を活性化することにより、最終的にアクチン骨格の再編成を行う。ネトリン依存性に細胞内領域が切断され転写制御因子として働くことも示されている。ネオゲニンは、ネトリンファミリーに属さない別のリガンドであるrepulsive guidance molecule (RGMa)にも結合し、軸索反発を示す[10]。UNC5は、単独でネトリンに対し軸索反発作用を示すが、DCCと共発現して軸索反発を起こすこともある。DCC-UNC5による反発作用は、DCCの細胞内P1ドメインとUNC5の細胞内DBドメインの結合により引き起こされる。
DCCは、軸索ガイダンス以外に、移動細胞の誘引、軸索の分岐、シナプス形成、オリゴデンドロサイトの発生、髄鞘形成にも関与する[1]。DCCは細胞接着機能も有し、乳腺、肺、血管など神経系以外の臓器の形態形成にも関与する[11]。
DCC、ネオゲニン、UNC5は、リガンドであるネトリンが存在しない時にアポトーシスを誘導する。このようなdependence機構がDCCの腫瘍抑制遺伝子としての機能を説明する可能性も示唆されている[12]。
個体における機能
軸索ガイダンス
DCCノックアウトマウスでは脊髄交連神経細胞の軸索が伸張せず交連が形成されない [6]。これは、脊髄の腹側正中部に存在するフロアープレート細胞から分泌されるネトリン1による誘引シグナルを受容できないためであり、ネトリン1ノックアウトマウスでも全く同じ異常が観察される[13]。さらに、DCCあるいはネトリン1のノックアウトマウスでは、脳梁、海馬交連、前交連などの形成も異常になる[7]。一部の神経細胞(例えば滑車神経)では、ネトリン1が軸索を反発することにより誘導している。
細胞移動
ネトリン1あるいはDCCノックアウトマウスでは橋核が形成されない[7] [13]。これは、橋核を形成する細胞の移動が障害された結果であり、野生型マウスでは、延髄腹側正中部に発現するネトリン1がDCCを発現する小脳前核細胞を下菱脳唇から腹側前方へ誘引していると考えられる。
疾患との関わり
先天的鏡像運動症(congenital mirror movement syndrome)の原因遺伝子となる[14]。この遺伝性疾患は、片側の随意運動により反対側に不随意運動が誘発されるものであり、DCCがヒトの神経回路形成でも重要な役割を担っていることを示唆する。ヒトのネトリン1遺伝子、あるいはDCC遺伝子の一塩基多型がパーキンソン病や筋萎縮性側索硬化症になりやすさに関連する。これはシナプス形成と関連した異常だと考えられるが、発症のメカニズムは不明である。
関連語
参考文献
<refrences />
- ↑ 1.0 1.1 1.2 1.3 1.4
Lai Wing Sun, K., Correia, J.P., & Kennedy, T.E. (2011).
Netrins: versatile extracellular cues with diverse functions. Development (Cambridge, England), 138(11), 2153-69. [PubMed:21558366] [WorldCat] [DOI] 引用エラー: 無効な<ref>タグ; name "ref7"が異なる内容で複数回定義されています - ↑ Resource not found in PubMed.
- ↑ 3.0 3.1 3.2 3.3 3.4 Resource not found in PubMed.
- ↑ 4.0 4.1 Resource not found in PubMed.
- ↑ 5.0 5.1 Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ 7.0 7.1 7.2 Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ Resource not found in PubMed.
- ↑ 13.0 13.1 Resource not found in PubMed.
- ↑ Resource not found in PubMed.