小脳原基
川内大輔
ドイツがん研究センター 小児脳腫瘍部門
DOI:10.14931/bsd.7687 原稿受付日:2018年4月7日 原稿完成日:2018年6月23日
担当編集委員:村上 富士夫(大阪大学 大学院生命機能研究科)
英語名:Cerebellar primordium 独:Kleinhirn-Anlage 仏:l’ébauche du cervelet
小脳原基は小脳の元となる神経組織であり、発生過程において神経管の中脳-後脳境界領域の背側部分に形成される。小脳原基における神経上皮細胞は、将来小脳回路を構成する神経細胞やグリア細胞を場所特異的あるいは時期特異的にきわめて厳密に生み出す。この遺伝プログラムにより、成体小脳では細胞が正しく配置され、機能することが出来る。一方で、脳腫瘍や小脳萎縮などの遺伝病は、こういった遺伝子プログラムの異常が原因となっていることが最近になって示唆されている。
小脳原基とは
小脳原基は成体において小脳となる部分であり、発生期において、筒状の構造をもつ神経管の中脳後脳境界部尾側(後脳側)から派生する菱状の空間、第四脳室の上唇部に由来する。後脳領域は発生初期にロンボメアと呼ばれる分節構造を形成し、各分節構造から決まった神経器官が生じる。小脳原基はその第一分節の翼板が発達、肥大することにより、後脳背側部に形成される。
ヒトでは受精後7-9週齢で翼板の肥大が起こり、10週齢までに左右の小脳原基は正中線で融合する[1]。一方、マウスでは受精後7-8日目からこれらの現象が観察される。
小脳発生領域は種をまたいで保存されている一方、生み出される小脳細胞の種類や神経前駆細胞の移動経路が種間で異なるため、最終的には脊椎動物間、例えば両生類、鳥類、哺乳類で構造がかなり異なる[2]。特に小脳顆粒前駆細胞の分裂が見られるのは鳥類以降の高等動物であり、その結果、より複雑な小脳構造が形成される。
小脳原基発生領域決定の分子機構
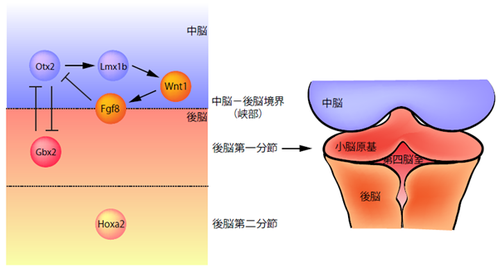
小脳原基の派生する後脳の第一分節は、ホメオボックス型転写因子であるGbx2陽性、かつOtx2およびHoxa2陰性の領域として発生初期に分子的に定義される[3][4](図1)。遺伝子組み換え動物を用いた実験から、Otx2およびGbx2転写因子は相互的に発現を抑制することで第一分節の吻側境界を決定すること[5][6][7]、また一方で、Hoxa2が第二分節より尾側で発現することにより、小脳神経細胞の分化を抑制していることが知られている[8][9]。Otx2の下流因子であるLmx1bは発現細胞において分泌たんぱく質Wnt1の発現を誘導する。Wnt1が隣接細胞でFgf8の発現を誘導し[10]、Fgf8がOtx2の発現を負に制御することにより[11][12]、厳密に中脳小脳の境界領域、峡部(isthmus)が形成される(図1)。
第一分節を規定するこれらの因子に加え、ホメオボックス型転写因子En1やEn2は中脳から第一分節内の吻側領域にかけて発現し、小脳吻側部分の領域決定に関与する[13]が、領域決定後も小脳小葉形成などに関わっている[14][15]。
哺乳類小脳原基において生み出される細胞群
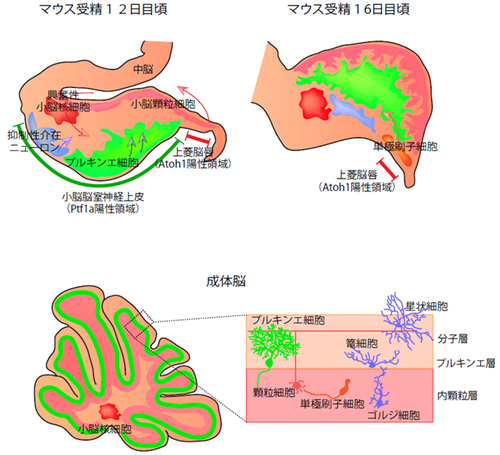
小脳原基は大別して二種類の胚ゾーンを含む器官である。胚ゾーンの一つは第四脳室における神経上皮細胞、もう一つは上菱脳唇(upper rhombic lip)である(図2)。これら二つの胚ゾーンは隣接しており、それぞれbHLH型転写因子であるPtf1a陽性とAtoh1陽性領域として分子的に定義される。これら二つのbHLH型転写因子が互いに発現を負に制御することにより[16][17]、胚ゾーンの境界領域が決定されている。小脳上皮におけるAtoh1陽性領域は発生初期にBMPシグナルによって誘導される[18]。各胚ゾーンからは、異なる複数の神経前駆細胞やグリア細胞が発生時期特異的に生み出される。第四脳室神経上皮細胞は抑制性神経細胞やアストロサイト、上菱脳唇は主に小脳興奮性細胞を生み出す。ウイルスや免疫組織化学を用いた生体内細胞標識技術により、上菱脳唇由来の細胞から小脳グリア細胞が生み出される証拠は得られていないが、小脳興奮性細胞の一つである小脳顆粒細胞の一部が培養下でアストロサイト様の個性を獲得することも観察されており[19]、上菱脳唇由来のグリア細胞の存在は完全には否定できない。
プルキンエ細胞
小脳皮質の抑制性出力細胞であるプルキンエ細胞は第四脳室の神経上皮から生まれる。マウスでは受精後十日頃から十三日までの間に誕生する。分化の過程で前駆細胞はPtf1aからOlig1/2、そしてLhx1/5と一時的に様々な転写因子を発現し、個性を獲得していく。これらの遺伝子を欠損した小脳原基ではプルキンエ細胞の前駆体が欠損、または細胞数が減少することが知られている[20][21][22]。プルキンエ細胞特異的な分子マーカーとしてカルビンジン(Calb1)[23]あるいはCorl2[24]がよく用いられる。小脳脳室で誕生した前駆細胞は、放射状に小脳表面に向かって移動し、最終的にプルキンエ細胞層にとどまる。最近の研究では、これらの前駆細胞の移動は接線方向への移動様式も含むことや分泌タンパク質リーリン(Reelin、Reln)が関与することも見出されているが[25][26]、分子機構を含むより詳細な細胞移動機構の解明が待たれる。
小脳核細胞
小脳核細胞は、興奮性と抑制性の細胞から成り、興奮性小脳核ニューロンはプルキンエ細胞からの入力を受け、小脳から他の脳組織へのシグナル伝達を担う。これらの興奮性小脳核細胞は、上菱脳唇においてマウスで受精後十日目頃から生み出され、小脳原基表層を移動し、小脳上層部から深部へと侵入する。一方で下オリーブ核へと投射する抑制性小脳核ニューロン、及びPax2陽性である小脳核介在神経細胞は、他の小脳抑制性細胞と同じく小脳脳室の神経上皮から発生する。小脳核抑制性細胞は小脳神経上皮から深部へと直接向かう[20]。遺伝子欠損マウスの実験から、抑制性および興奮性小脳核群の個性決定にはbHLH転写因子Ptf1aおよびAtoh1の発現がそれぞれ不可欠であることが知られている[20][27][28]。また、T-ボックス型転写因子Tbr1/2[29]やLIMホメオボックス型転写因子Lmx1a[30]は興奮性小脳核細胞の正常な分化に必須である。
小脳皮質抑制性介在ニューロン群
抑制性介在ニューロン群は、プルキンエ細胞に遅れPtf1a陽性の神経上皮で生まれ始める。マウスにおいては、まずゴルジ細胞(Golgi cell)が受精後十二日頃から[31]、その後に篭細胞(basket cell)と星状細胞(stellate cell)が生まれる。Olig1/2陽性のプルキンエ細胞とは異なり、抑制性介在ニューロンの前駆細胞の多くはGbx2陽性である。Gsx2はOlig1/2の発現を抑制し、介在ニューロンの個性を獲得する[21]。これらの細胞群はPax2陽性細胞となり、小脳白質からさらに最終目的地に向かって移動する。最終的にゴルジ細胞は小脳内顆粒層に、篭細胞や星状細胞は分子層にとどまり、局所的に回路を形成する(図2)。この移動様式は複雑で、移動を制御する分子機構には不明な点が多いが、PACAPやIGF1のような分泌たんぱく質が深く関わっている[32]。発生期の小脳原基の神経上皮は遺伝子発現の違いで細分化されるが、誕生時期の違いで異なる介在ニューロンを生みだす機構は未だ完全に理解されていない。
小脳皮質興奮性介在ニューロン群
顆粒細胞
成体脳で最も多く存在する神経細胞群であり、小脳においては興奮性介在ニューロンとして機能する。マウスにおいては、受精後12日目から16日目にかけて、Atoh1陽性の上菱脳唇から生まれる[27][28]。これらの前駆細胞は、興奮性の小脳核前駆細胞と同じく小脳原基表層を移動するが、顆粒細胞の前駆体は移動中も分裂能を示すのが特徴である。小脳表層に移動した顆粒細胞前駆体の有糸分裂は分泌たんぱく質ソニックヘッジホッグによって活性化され、マウスにおいては生後1週齢前後に分裂能がピークに達する[33]。またAtoh1の発現は前駆体においてもみられ、細胞分裂の停止を抑制する役割を担っている[34]。分裂を終えた顆粒細胞は、小脳外顆粒層を接線方向に移動した後、バーグマングリア細胞を足場として、小脳深部に向かって放射状に移動し、最終的に内顆粒層を形成する[35]。マウスにおいて小脳顆粒細胞の移動は約3週齢で終了する。遺伝子組換えマウスを用いた実験から、発生後期に生まれる顆粒細胞は主に尾側に分布すること[28]、特定の転写因子が吻側-尾側に異なって発現すること[36]は、小脳顆粒細胞の個性が小脳内で多様であることを示している。
単極刷子細胞
単極刷子細胞も主な興奮性介在ニューロンの一つであり、他の興奮性ニューロンと同じくAtoh1陽性の上菱脳唇から生まれる[37]。マウスでは受精後十三日目頃、ラットでは受精後十五日目ごろから生後数日までかけて生み出される(図2)。その前駆細胞は、他の興奮性ニューロンの前駆体とは異なり、接線方向移動の様式で直接小脳深部に向かって移動し、内顆粒層で成熟する。この細胞移動にRelnが関与していることが報告されている一方で[37]、他の小脳興奮性細胞と異なる移動経路をたどるための分子機構については不明な点が多い。この神経細胞は内顆粒層で軸索を伸長させ、顆粒細胞とシナプスを形成する。
グリア細胞
アストロサイト
神経上皮に存在する放射状グリアが起源であると考えられている[38]。最近の遺伝子組換えマウスを用いた実験により、アストロサイトとPax2陽性抑制性介在性ニューロンは同じ細胞を起源に持ち、抑制性介在性ニューロンへの運命決定にはbHLH型転写因子Ascl1が関与していることが示唆されている[38][39]。一方で、小脳の主な乏突起膠細胞(oligodendrocyte)起源は、ニワトリ-ウズラ胚脳組織などの移植実験により、小脳外部であるという説もある[39][40]が、まだ不明な点も多い。
バーグマングリア細胞
特徴的な形態を持つバーグマングリア細胞は、神経上皮から小脳原基内を放射状に移動し、最終的にプルキンエ細胞層で成熟する[41]。放射状グリアと異なり、成熟したバーグマングリアは複数の突起を小脳表層に伸長させる。これらの正常な突起形成にはNotchシグナルが関与していることが知られている[42][43]。
小脳原基に投射する求心性神経細胞群
発生期に小脳原基に投射する線維は主に苔状線維と登上線維に大別される[44]。
苔状線維
体性感覚経路や前庭小脳線維、小脳前核ニューロンとして小脳原基に投射し、最終的に小脳顆粒細胞の樹状突起にシナプスを形成する。
登上線維
後脳下オリーブ核より起こる登上線維は大脳皮質や視床、赤核、三叉核や脊髄など様々な小脳への入力を仲介、伝達する。登上線維も胎児期に小脳原基に投射するが、こちらはプルキンエ細胞とシナプスを形成する。
モノアミン系
また小脳はモノアミン系神経伝達物質作動性のニューロンの投射も受ける[44]。例えば縫線核(raphe nucleus)由来のセロトニン作動性ニューロンや青斑核(locus coeruleus)由来のノルアドレナリン作動性ニューロンは小脳顆粒細胞やプルキンエ細胞、小脳核に投射する。
小脳原基発生異常とがん、遺伝病
小脳神経上皮からの神経細胞の分化は特定の遺伝子によって厳密に制御されている。言い換えると、発生期におけるこれらの神経細胞の分化異常は、ヒトにおいて、遺伝病の発生に密接に関わる。特に近年のゲノムシーケンス技術の発達により、患者の生殖細胞突然変異を調べることで、原因遺伝子を特定しようとする試みが加速している。例えば、自閉症患者の生殖細胞突然変異は公共のデータベースで情報が共有されている[45]。チャージ症候群や自閉症患者では、小脳が萎縮しているケースがしばしば見られるが、最近の遺伝子組換えマウスを用いた研究で、原因遺伝子とされるクロマチン制御因子Chd7の機能欠損はOtx2の発現の脱抑制とFGF8の発現抑制を誘導し、結果として小脳の形成不全を起こすことが明らかになった[46]。さらにマウス小脳顆粒前駆細胞におけるChd7の体細胞突然変異は小脳萎縮、およびRelnシグナルの欠損によるプルキンエ細胞の分布に異常を引き起こす[47][48]。これは自閉症患者に見られる表現形を分子的に説明している。
脳腫瘍も神経細胞分化の異常が原因で起こりうる疾患である。近年のがんサンプルの体細胞突然変異のゲノム解析から、小脳で発生するがんと突然変異遺伝子群の関連性が明らかになり[49][50][51][52]、また情報共有のための公共のデータベースもよく整備されている[53][54]。これらを基盤として、特定の小脳細胞における遺伝子変異が腫瘍形成に関与していることが、モデル動物を用いて示されつつある。例えば、遺伝子変異によるソニックヘッジホッグシグナル異常活性が小脳顆粒細胞で生じることが、髄芽腫の一因とされる[55]。逆に小脳顆粒細胞においてEGFシグナルの異常活性を誘導することで膠芽腫が誘導されること[56]や、がん遺伝子Mycの小脳原基における過剰発現が異なるタイプの髄芽腫を誘導することも示されており[57](54)、どの細胞にどのような遺伝子変異が起こりうるかが、がんの個性決定に影響すると考えられている。
関連項目
参考文献
- ↑
Cho, K.H., Rodríguez-Vázquez, J.F., Kim, J.H., Abe, H., Murakami, G., & Cho, B.H. (2011).
Early fetal development of the human cerebellum. Surgical and radiologic anatomy : SRA, 33(6), 523-30. [PubMed:21380713] [WorldCat] [DOI] - ↑
Butts, T., Green, M.J., & Wingate, R.J. (2014).
Development of the cerebellum: simple steps to make a 'little brain'. Development (Cambridge, England), 141(21), 4031-41. [PubMed:25336734] [WorldCat] [DOI] - ↑
Millet, S., Bloch-Gallego, E., Simeone, A., & Alvarado-Mallart, R.M. (1996).
The caudal limit of Otx2 gene expression as a marker of the midbrain/hindbrain boundary: a study using in situ hybridisation and chick/quail homotopic grafts. Development (Cambridge, England), 122(12), 3785-97. [PubMed:9012500] [WorldCat] - ↑
Wingate, R.J., & Hatten, M.E. (1999).
The role of the rhombic lip in avian cerebellum development. Development (Cambridge, England), 126(20), 4395-404. [PubMed:10498676] [WorldCat] - ↑
Broccoli, V., Boncinelli, E., & Wurst, W. (1999).
The caudal limit of Otx2 expression positions the isthmic organizer. Nature, 401(6749), 164-8. [PubMed:10490025] [WorldCat] [DOI] - ↑
Wassarman, K.M., Lewandoski, M., Campbell, K., Joyner, A.L., Rubenstein, J.L., Martinez, S., & Martin, G.R. (1997).
Specification of the anterior hindbrain and establishment of a normal mid/hindbrain organizer is dependent on Gbx2 gene function. Development (Cambridge, England), 124(15), 2923-34. [PubMed:9247335] [WorldCat] - ↑
Katahira, T., Sato, T., Sugiyama, S., Okafuji, T., Araki, I., Funahashi, J., & Nakamura, H. (2000).
Interaction between Otx2 and Gbx2 defines the organizing center for the optic tectum. Mechanisms of development, 91(1-2), 43-52. [PubMed:10704829] [WorldCat] [DOI] - ↑
Gavalas, A., Davenne, M., Lumsden, A., Chambon, P., & Rijli, F.M. (1997).
Role of Hoxa-2 in axon pathfinding and rostral hindbrain patterning. Development (Cambridge, England), 124(19), 3693-702. [PubMed:9367425] [WorldCat] - ↑
Eddison, M., Toole, L., Bell, E., & Wingate, R.J. (2004).
Segmental identity and cerebellar granule cell induction in rhombomere 1. BMC biology, 2, 14. [PubMed:15198802] [PMC] [WorldCat] [DOI] - ↑
Matsunaga, E., Katahira, T., & Nakamura, H. (2002).
Role of Lmx1b and Wnt1 in mesencephalon and metencephalon development. Development (Cambridge, England), 129(22), 5269-77. [PubMed:12399317] [WorldCat] - ↑
Liu, A., Losos, K., & Joyner, A.L. (1999).
FGF8 can activate Gbx2 and transform regions of the rostral mouse brain into a hindbrain fate. Development (Cambridge, England), 126(21), 4827-38. [PubMed:10518499] [WorldCat] - ↑
Martinez, S., Crossley, P.H., Cobos, I., Rubenstein, J.L., & Martin, G.R. (1999).
FGF8 induces formation of an ectopic isthmic organizer and isthmocerebellar development via a repressive effect on Otx2 expression. Development (Cambridge, England), 126(6), 1189-200. [PubMed:10021338] [WorldCat] - ↑
Wurst, W., Auerbach, A.B., & Joyner, A.L. (1994).
Multiple developmental defects in Engrailed-1 mutant mice: an early mid-hindbrain deletion and patterning defects in forelimbs and sternum. Development (Cambridge, England), 120(7), 2065-75. [PubMed:7925010] [WorldCat] - ↑
Cheng, Y., Sudarov, A., Szulc, K.U., Sgaier, S.K., Stephen, D., Turnbull, D.H., & Joyner, A.L. (2010).
The Engrailed homeobox genes determine the different foliation patterns in the vermis and hemispheres of the mammalian cerebellum. Development (Cambridge, England), 137(3), 519-29. [PubMed:20081196] [PMC] [WorldCat] [DOI] - ↑
Sillitoe, R.V., Stephen, D., Lao, Z., & Joyner, A.L. (2008).
Engrailed homeobox genes determine the organization of Purkinje cell sagittal stripe gene expression in the adult cerebellum. The Journal of neuroscience : the official journal of the Society for Neuroscience, 28(47), 12150-62. [PubMed:19020009] [PMC] [WorldCat] [DOI] - ↑
Kawauchi, D., & Saito, T. (2008).
Transcriptional cascade from Math1 to Mbh1 and Mbh2 is required for cerebellar granule cell differentiation. Developmental biology, 322(2), 345-54. [PubMed:18723012] [WorldCat] [DOI] - ↑
Yamada, M., Seto, Y., Taya, S., Owa, T., Inoue, Y.U., Inoue, T., ..., & Hoshino, M. (2014).
Specification of spatial identities of cerebellar neuron progenitors by ptf1a and atoh1 for proper production of GABAergic and glutamatergic neurons. The Journal of neuroscience : the official journal of the Society for Neuroscience, 34(14), 4786-800. [PubMed:24695699] [PMC] [WorldCat] [DOI] - ↑
Alder, J., Lee, K.J., Jessell, T.M., & Hatten, M.E. (1999).
Generation of cerebellar granule neurons in vivo by transplantation of BMP-treated neural progenitor cells. Nature neuroscience, 2(6), 535-40. [PubMed:10448218] [WorldCat] [DOI] - ↑
Okano-Uchida, T., Himi, T., Komiya, Y., & Ishizaki, Y. (2004).
Cerebellar granule cell precursors can differentiate into astroglial cells. Proceedings of the National Academy of Sciences of the United States of America, 101(5), 1211-6. [PubMed:14745007] [PMC] [WorldCat] [DOI] - ↑ 20.0 20.1 20.2
Hoshino, M., Nakamura, S., Mori, K., Kawauchi, T., Terao, M., Nishimura, Y.V., ..., & Nabeshima, Y. (2005).
Ptf1a, a bHLH transcriptional gene, defines GABAergic neuronal fates in cerebellum. Neuron, 47(2), 201-13. [PubMed:16039563] [WorldCat] [DOI] - ↑ 21.0 21.1
Seto, Y., Nakatani, T., Masuyama, N., Taya, S., Kumai, M., Minaki, Y., ..., & Hoshino, M. (2014).
Temporal identity transition from Purkinje cell progenitors to GABAergic interneuron progenitors in the cerebellum. Nature communications, 5, 3337. [PubMed:24535035] [PMC] [WorldCat] [DOI] - ↑
Zhao, Y., Kwan, K.M., Mailloux, C.M., Lee, W.K., Grinberg, A., Wurst, W., ..., & Westphal, H. (2007).
LIM-homeodomain proteins Lhx1 and Lhx5, and their cofactor Ldb1, control Purkinje cell differentiation in the developing cerebellum. Proceedings of the National Academy of Sciences of the United States of America, 104(32), 13182-6. [PubMed:17664423] [PMC] [WorldCat] [DOI] - ↑
Enderlin, S., Norman, A.W., & Celio, M.R. (1987).
Ontogeny of the calcium binding protein calbindin D-28k in the rat nervous system. Anatomy and embryology, 177(1), 15-28. [PubMed:3439634] [WorldCat] [DOI] - ↑
Minaki, Y., Nakatani, T., Mizuhara, E., Inoue, T., & Ono, Y. (2008).
Identification of a novel transcriptional corepressor, Corl2, as a cerebellar Purkinje cell-selective marker. Gene expression patterns : GEP, 8(6), 418-23. [PubMed:18522874] [WorldCat] [DOI] - ↑
Miyata, T., Nakajima, K., Aruga, J., Takahashi, S., Ikenaka, K., Mikoshiba, K., & Ogawa, M. (1996).
Distribution of a reeler gene-related antigen in the developing cerebellum: an immunohistochemical study with an allogeneic antibody CR-50 on normal and reeler mice. The Journal of comparative neurology, 372(2), 215-28. [PubMed:8863127] [WorldCat] [DOI] - ↑
Miyata, T., Ono, Y., Okamoto, M., Masaoka, M., Sakakibara, A., Kawaguchi, A., ..., & Ogawa, M. (2010).
Migration, early axonogenesis, and Reelin-dependent layer-forming behavior of early/posterior-born Purkinje cells in the developing mouse lateral cerebellum. Neural development, 5, 23. [PubMed:20809939] [PMC] [WorldCat] [DOI] - ↑ 27.0 27.1
Wang, V.Y., Rose, M.F., & Zoghbi, H.Y. (2005).
Math1 expression redefines the rhombic lip derivatives and reveals novel lineages within the brainstem and cerebellum. Neuron, 48(1), 31-43. [PubMed:16202707] [WorldCat] [DOI] - ↑ 28.0 28.1 28.2
Machold, R., & Fishell, G. (2005).
Math1 is expressed in temporally discrete pools of cerebellar rhombic-lip neural progenitors. Neuron, 48(1), 17-24. [PubMed:16202705] [WorldCat] [DOI] - ↑
Fink, A.J., Englund, C., Daza, R.A., Pham, D., Lau, C., Nivison, M., ..., & Hevner, R.F. (2006).
Development of the deep cerebellar nuclei: transcription factors and cell migration from the rhombic lip. The Journal of neuroscience : the official journal of the Society for Neuroscience, 26(11), 3066-76. [PubMed:16540585] [PMC] [WorldCat] [DOI] - ↑
Chizhikov, V.V., Lindgren, A.G., Mishima, Y., Roberts, R.W., Aldinger, K.A., Miesegaes, G.R., ..., & Millen, K.J. (2010).
Lmx1a regulates fates and location of cells originating from the cerebellar rhombic lip and telencephalic cortical hem. Proceedings of the National Academy of Sciences of the United States of America, 107(23), 10725-30. [PubMed:20498066] [PMC] [WorldCat] [DOI] - ↑
Kita, Y., Kawakami, K., Takahashi, Y., & Murakami, F. (2013).
Development of cerebellar neurons and glias revealed by in utero electroporation: Golgi-like labeling of cerebellar neurons and glias. PloS one, 8(7), e70091. [PubMed:23894597] [PMC] [WorldCat] [DOI] - ↑
Galas, L., Bénard, M., Lebon, A., Komuro, Y., Schapman, D., Vaudry, H., ..., & Komuro, H. (2017).
Postnatal Migration of Cerebellar Interneurons. Brain sciences, 7(6). [PubMed:28587295] [PMC] [WorldCat] [DOI] - ↑
Wechsler-Reya, R.J., & Scott, M.P. (1999).
Control of neuronal precursor proliferation in the cerebellum by Sonic Hedgehog. Neuron, 22(1), 103-14. [PubMed:10027293] [WorldCat] [DOI] - ↑
Ayrault, O., Zhao, H., Zindy, F., Qu, C., Sherr, C.J., & Roussel, M.F. (2010).
Atoh1 inhibits neuronal differentiation and collaborates with Gli1 to generate medulloblastoma-initiating cells. Cancer research, 70(13), 5618-27. [PubMed:20516124] [PMC] [WorldCat] [DOI] - ↑
Komuro, H., & Yacubova, E. (2003).
Recent advances in cerebellar granule cell migration. Cellular and molecular life sciences : CMLS, 60(6), 1084-98. [PubMed:12861377] [WorldCat] [DOI] - ↑
Schüller, U., Kho, A.T., Zhao, Q., Ma, Q., & Rowitch, D.H. (2006).
Cerebellar 'transcriptome' reveals cell-type and stage-specific expression during postnatal development and tumorigenesis. Molecular and cellular neurosciences, 33(3), 247-59. [PubMed:16962790] [WorldCat] [DOI] - ↑ 37.0 37.1
Englund, C., Kowalczyk, T., Daza, R.A., Dagan, A., Lau, C., Rose, M.F., & Hevner, R.F. (2006).
Unipolar brush cells of the cerebellum are produced in the rhombic lip and migrate through developing white matter. The Journal of neuroscience : the official journal of the Society for Neuroscience, 26(36), 9184-95. [PubMed:16957075] [PMC] [WorldCat] [DOI] - ↑ 38.0 38.1
Sudarov, A., Turnbull, R.K., Kim, E.J., Lebel-Potter, M., Guillemot, F., & Joyner, A.L. (2011).
Ascl1 genetics reveals insights into cerebellum local circuit assembly. The Journal of neuroscience : the official journal of the Society for Neuroscience, 31(30), 11055-69. [PubMed:21795554] [PMC] [WorldCat] [DOI] - ↑ 39.0 39.1
Grimaldi, P., Parras, C., Guillemot, F., Rossi, F., & Wassef, M. (2009).
Origins and control of the differentiation of inhibitory interneurons and glia in the cerebellum. Developmental biology, 328(2), 422-33. [PubMed:19217896] [WorldCat] [DOI] - ↑
Mecklenburg, N., Garcia-López, R., Puelles, E., Sotelo, C., & Martinez, S. (2011).
Cerebellar oligodendroglial cells have a mesencephalic origin. Glia, 59(12), 1946-57. [PubMed:21901755] [WorldCat] [DOI] - ↑
Yuasa, S. (1996).
Bergmann glial development in the mouse cerebellum as revealed by tenascin expression. Anatomy and embryology, 194(3), 223-34. [PubMed:8849669] [WorldCat] [DOI] - ↑
Eiraku, M., Tohgo, A., Ono, K., Kaneko, M., Fujishima, K., Hirano, T., & Kengaku, M. (2005).
DNER acts as a neuron-specific Notch ligand during Bergmann glial development. Nature neuroscience, 8(7), 873-80. [PubMed:15965470] [WorldCat] [DOI] - ↑
Komine, O., Nagaoka, M., Watase, K., Gutmann, D.H., Tanigaki, K., Honjo, T., ..., & Tanaka, K. (2007).
The monolayer formation of Bergmann glial cells is regulated by Notch/RBP-J signaling. Developmental biology, 311(1), 238-50. [PubMed:17915208] [WorldCat] [DOI] - ↑ 44.0 44.1
Rahimi-Balaei, M., Afsharinezhad, P., Bailey, K., Buchok, M., Yeganeh, B., & Marzban, H. (2015).
Embryonic stages in cerebellar afferent development. Cerebellum & ataxias, 2, 7. [PubMed:26331050] [PMC] [WorldCat] [DOI] - ↑ SFARI Gene
- ↑
Yu, T., Meiners, L.C., Danielsen, K., Wong, M.T., Bowler, T., Reinberg, D., ..., & Basson, M.A. (2013).
Deregulated FGF and homeotic gene expression underlies cerebellar vermis hypoplasia in CHARGE syndrome. eLife, 2, e01305. [PubMed:24368733] [PMC] [WorldCat] [DOI] - ↑
Whittaker, D.E., Riegman, K.L., Kasah, S., Mohan, C., Yu, T., Pijuan-Sala, B., ..., & Basson, M.A. (2017).
The chromatin remodeling factor CHD7 controls cerebellar development by regulating reelin expression. The Journal of clinical investigation, 127(3), 874-887. [PubMed:28165338] [PMC] [WorldCat] [DOI] - ↑
Feng, W., Kawauchi, D., Körkel-Qu, H., Deng, H., Serger, E., Sieber, L., ..., & Liu, H.K. (2017).
Chd7 is indispensable for mammalian brain development through activation of a neuronal differentiation programme. Nature communications, 8, 14758. [PubMed:28317875] [PMC] [WorldCat] [DOI] - ↑
Northcott, P.A., Buchhalter, I., Morrissy, A.S., Hovestadt, V., Weischenfeldt, J., Ehrenberger, T., ..., & Lichter, P. (2017).
The whole-genome landscape of medulloblastoma subtypes. Nature, 547(7663), 311-317. [PubMed:28726821] [PMC] [WorldCat] [DOI] - ↑
Kool, M., Jones, D.T., Jäger, N., Northcott, P.A., Pugh, T.J., Hovestadt, V., ..., & ICGC PedBrain Tumor Project (2014).
Genome sequencing of SHH medulloblastoma predicts genotype-related response to smoothened inhibition. Cancer cell, 25(3), 393-405. [PubMed:24651015] [PMC] [WorldCat] [DOI] - ↑
Nomura, M., Mukasa, A., Nagae, G., Yamamoto, S., Tatsuno, K., Ueda, H., ..., & Saito, N. (2017).
Distinct molecular profile of diffuse cerebellar gliomas. Acta neuropathologica, 134(6), 941-956. [PubMed:28852847] [PMC] [WorldCat] [DOI] - ↑
Jones, D.T., Hutter, B., Jäger, N., Korshunov, A., Kool, M., Warnatz, H.J., ..., & International Cancer Genome Consortium PedBrain Tumor Project (2013).
Recurrent somatic alterations of FGFR1 and NTRK2 in pilocytic astrocytoma. Nature genetics, 45(8), 927-32. [PubMed:23817572] [PMC] [WorldCat] [DOI] - ↑ St. Jude Cloud PeCan
- ↑ The Cancer Genome Atlas
- ↑
Roussel, M.F., & Hatten, M.E. (2011).
Cerebellum development and medulloblastoma. Current topics in developmental biology, 94, 235-82. [PubMed:21295689] [PMC] [WorldCat] [DOI] - ↑
Kratochvill, F., Neale, G., Haverkamp, J.M., Van de Velde, L.A., Smith, A.M., Kawauchi, D., ..., & Murray, P.J. (2015).
TNF Counterbalances the Emergence of M2 Tumor Macrophages. Cell reports, 12(11), 1902-14. [PubMed:26365184] [PMC] [WorldCat] [DOI] - ↑
Kawauchi, D., Ogg, R.J., Liu, L., Shih, D.J.H., Finkelstein, D., Murphy, B.L., ..., & Roussel, M.F. (2017).
Novel MYC-driven medulloblastoma models from multiple embryonic cerebellar cells. Oncogene, 36(37), 5231-5242. [PubMed:28504719] [PMC] [WorldCat] [DOI]