神経誘導
笹井 紀明
奈良先端科学技術大学院大学
DOI:10.14931/bsd.2114 原稿受付日:2017年2月3日 原稿完成日:2017年4月23日
担当編集委員:村上 富士夫(大阪大学 大学院生命機能研究科)
英語名:neural induction 独:neuronale Induktion 仏:induction de la neurulation
神経誘導とは、動物の初期発生の段階において、形成体(organizer)と呼ばれる胚の一領域が未分化外胚葉に作用して、神経組織という性質を付与する(神経に運命決定する)現象のことである。
神経誘導と神経誘導因子の発見
受精卵は、最初は増殖を繰り返して未分化な細胞の塊を形成するが、原腸形成期(マウスでは受精6日前後、アフリカツメガエルでは温度にもよるが12-14時間程度)になると細胞が外胚葉、中胚葉、内胚葉の3つの胚葉に分類され、細胞それぞれの性質が大まかに特徴付けられるようになる。
このうち外胚葉の一部は神経組織へと分化し、神経板を形成するが、その運命決定は、背側中胚葉(カエルでは原口背唇部(dorsal lip)、マウスやニワトリでは結節(node))から分泌されるシグナル因子(神経誘導因子)に依存する。
一般に「誘導(induction)」とは、1つの組織が別の組織に作用してふるまいを制御する現象のことをいい、神経誘導はこのような誘導現象の1つである[1] [2]。
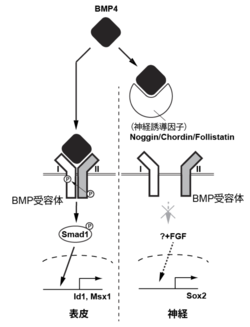
未分化外胚葉細胞でBMPシグナルが活性化されると細胞内でSmad1がリン酸化され、下流遺伝子の遺伝子発現が誘導され、表皮へと分化する。一方、BMPシグナルが遮断された細胞は神経に分化する。[3] [4][5]を参考にして作成。図中のBMP受容体のうち、I, IIとあるのはそれぞれタイプ1、タイプ2の意味。Pはリン酸化を示す。
外胚葉から神経組織への運命決定、すなわち細胞の神経化(neuralization)は脊椎動物の胚発生において最も初期に起こる現象の1つである。したがって神経誘導の研究は、初期胚が比較的大きく発生が母胎外で起きる両生類胚(イモリ、カエルなど)を中心に進展してきた。
1924年、ドイツの生物学者Hans SpemannとHilde Mangoldはイモリの原口背唇部(背側中胚葉を含む部分)を別の個体に移植する実験を行い、移植された胚に2次軸(体軸:背骨の原基(脊策)を含む頭尾軸に沿った細長い構造)が形成され、さらにその周辺部に神経組織が誘導されることを発見した[6]。これは、移植した原口背唇部が移植先の組織に影響を及ぼし、結果として胚の形態形成を制御したことを意味する。そこで、Spemannらはこの領域を「形態形成を支配する領域」という意味で「形成体(organizer)」と命名した[6] [7]。
その後、この現象を制御する分泌性の因子(神経誘導因子(neural inducer))を特定する試みが長く行われてきたが、背側中胚葉はサイズ的に小さいために、そこに存在するタンパク質を生化学的に特定することは困難であった。しかし、分子生物学的手法が発達するにつれて遺伝子解析が可能となり、1990年代にはその分子実体が次々と明らかになった。
Richard M HarlandとWilliam C Smithは、発現スクリーニング(背側中胚葉に発現する遺伝子のmRNAの中で神経誘導活性を持つ分画を細分化する方法)によりノギン (noggin)を[8]、Edward M De Robertisと笹井芳樹は、ディファレンシャルスクリーニング(発現が背側中胚葉に限局する遺伝子を単離する方法)によってコーディン (chordin)を[9]それぞれ単離し、それらが神経誘導因子であることを証明した。また、Douglas A Meltonと Ali Hemmati-Brivanlou は、上野直人らがすでに単離していた卵胞刺激ホルモンの阻害因子フォリスタチン (follistatin)に神経誘導活性があることを見いだした[10] [11]。
さらなる研究の結果、これらの神経誘導因子はいずれもTGFβスーパーファミリーの一種BMP4と結合し、BMP4とBMP受容体の相互作用を阻害することによって細胞を神経化することが明らかとなった(図1)[12] [13] [4]。実際にBMPの強制発現により細胞は神経化が抑制されて表皮に分化し[14]、逆にドミナントネガティブBMP受容体を用いてBMPシグナルを遮断すると細胞が神経化する[15]。したがって、BMPシグナルの存在・非存在が未分化外胚葉の運命(表皮か神経か)の二者択一(binary decision)を行うと言える[12]。
なお、follistatinはBMP4のほかにアクチビン (activin)(TGFβの一種で中胚葉誘導因子)とも結合してその活性を抑制する。このことはfollistatinが中胚葉分化抑制と神経誘導の活性を併せ持つことを意味する[11] [16]。
その後アフリカツメガエルにおいて、noggin、chordin、follistatinは互いにリダンダント(いずれかの機能を阻害しても、残りの因子が神経誘導活性を補償する)であり、3つの遺伝子の機能を同時に阻害して初めて神経誘導が抑制されることが示された[17]。
Instructiveとpermissiveな誘導様式
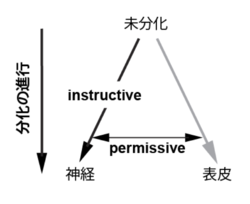
Howard Holtzer[18]は、細胞の分化誘導には2つの様式が存在することを提唱した[19](図2)。
1つは、誘導因子が分化方向を決定しながら、分化そのものも進行させるというものである。この誘導様式はinstructive(細胞を「教育する」意味)と呼ばれ、レチノイン酸によるホメオボックス遺伝子の発現誘導はその一例である[20]。
一方、分化そのものは誘導因子の存在と独立して進行し、誘導因子は分化方向のみを決定するような誘導様式のことをpermissive(一定方向に向かうことを「許容する」意味)という。
ここで議論する神経誘導因子は、未分化外胚葉を神経化する役割を持つが、神経誘導因子を受けない細胞は表皮に分化するため、分化の進行自体は誘導因子の有無に依存しない。したがって、noggin, chordin, follistatinは神経誘導においてpermissiveな役割を果たすものと言える。
神経デフォルト説と細胞のコンピテンス
アフリカツメガエルのアニマルキャップ(初期胚の未分化細胞からなる細胞集団)をバラバラにして細胞同士の相互作用を失くすと細胞は神経化する[1] [21]。これはBMPシグナルが薄まったからだと推測される。この実験事実から、未分化外胚葉細胞は外部から何もシグナルを受け取らなければ神経化するという仮説「神経デフォルト説」が提唱されるようになった[1] [22] [23]。
しかしその後の研究から、原腸形成期の外胚葉細胞では神経誘導因子の作用を受ける時期に細胞内でERK(MAPキナーゼ)があらかじめ活性化されており、このことが神経化に必須であることが明らかとなった[21] [24]。実際にFGF8が原腸形成期に発現している[24] [25]。FGF/ERKシグナルが活性化している細胞は神経以外にも分化するため、FGF/ERKシグナルは直接細胞を神経化する因子というわけではないが、細胞に神経化する能力(反応場)を持たせるという意味では重要である[24] [26]。
また、原腸形成期の細胞があらかじめ発現している遺伝子の組み合わせも神経化に重要である[27]。このように、神経誘導因子を受けて神経化するためには細胞に一定の条件、つまり「誘導因子に対する反応能」が必要であり、この細胞の特質のことを「コンピテンス(competence)」と呼ぶ[28] [29]。したがって、「神経デフォルト説」はこのコンピテンスの成立が前提となっている。
一般に特定の細胞運命決定には、周辺組織からの「誘導(induction:誘導因子による細胞外部からの制御)」と、受け手細胞の「コンピテンス(competence:細胞の内部状態)」が一致しなければならない。神経誘導の場合、両条件が一致するのは発生期では原腸形成期前後のみであり、これが、神経誘導が胚発生の一時期にしか起こらないことの理由である[28]。
ショウジョウバエの神経誘導
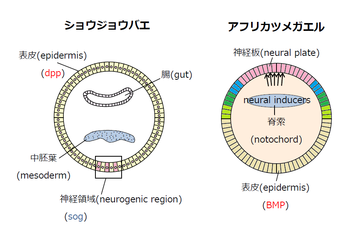
ショウジョウバエにおいては、神経芽細胞(neuroblast)は胚の腹側で生じる[30]。
この神経分化に必須の役割を果たすのは、short gastrulation(sog)である。Sogは胚の腹側から背側にかけて濃度勾配を形成し[31]、そのタンパク質はchordin同様にシステインに富むモチーフを4つ持ち、機能的にはchordinと類似する(つまり、sogをアフリカツメガエルで強制発現すると2次軸が形成され、外胚葉は神経化する)[32]。また、sogの変異を脊椎動物のnogginで補償できることからも、sogが脊椎動物の神経誘導因子と同じ機能を持つことが推察できる[33]。
一方、decapentaplegic(dpp)は胚の背側に発現して脊椎動物のBMP4と同等の機能を持ち[34]、sogと直接結合して互いの機能を阻害し合う(図3)。
この点で、sogとdppの関係は、脊椎動物のchordin/noggin とBMPの関係に対応している[33] [35]。このことから、脊椎動物と無脊椎動物では神経誘導の分子メカニズムが類似していることが示されただけでなく、進化の過程で胚の背腹軸が反転し、そこに発現する因子も同様に反転していることも示唆された[30]。
羊膜動物における神経誘導
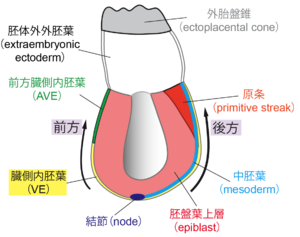
この時期にはエピブラスト(epiblast)と呼ばれる、比較的未分化な細胞が、中胚葉や内胚葉からのシグナルに応答して、神経を含め様々な細胞へと分化して行く。原条(primitive streak)は胚の後方でエピブラストが陥入して生じる構造で、この構造を通過する細胞は中胚葉または内胚葉に分化する。[36][37][38]を参考にして作成。
羊膜動物(ニワトリやマウスなど)の胚において、両生類の形成体に相当する部分は「結節(node)」である(図4)。
イギリスの生物学者Conrad H Waddingtonは、ニワトリ胚のヘンゼン結節(Hensen’s node)をほかの鳥類胚に移植すると2次軸を形成することを発見し、この領域が両生類の原口背唇部の相同領域であることを証明した[39] [40]。
両生類で単離された神経誘導因子はニワトリやマウスにおいてもこの領域(結節)に発現している[41] [42] [43] [44]。しかし、ニワトリにおける実験では、BMPシグナルを阻害するだけでは未分化細胞(エピブラスト)を神経化することはできない[42]。このことから、noggin, chordin, follistatin以外に誘導因子(または神経化する条件)が存在することが示唆され、その候補因子としてWntやFGFに関連するものが想定されている[45] [46]。
マウスでは、神経誘導因子の胚発生における役割が主に遺伝子破壊法(ノックアウト)を用いて解析されてきた。その結果、noggin、chordin、follistatinはいずれも単独の遺伝子破壊では神経誘導自体に対する影響は大きくないが、いったん細胞が神経化した後の分化の過程で必要であることや、中胚葉(体節など)の分化に必須であることが示されている[44] [47] [48]。
一方、chordinとnogginのダブルノックアウトマウスでは、体幹部神経の分化異常は比較的弱いものの、前脳が形成されないことが明らかになった[44] [49]。この結果はマウスの神経誘導に関して重要な知見である。マウスでは、結節(chordinとnogginが発現する領域)は体幹部(脊髄領域など)の神経分化を誘導し、前脳はそれとは独立に前方臓側内胚葉(anterior visceral endoderm; AVE)から誘導される可能性が示唆されてきた[50]。しかしこのノックアウトマウスでは、AVEは正常に形成されるものの前脳分化が著しく抑制されていた。このことは、結節が前脳の形成にも関与することを意味している。つまり、結節は全身の神経誘導に対して直接的または間接的に関与している。(なお現在、AVEは前脳のパターン形成や細胞移動を制御するなど、多くの機能を持っていることが明らかになっている[50][51])。
このように、noggin, chordin, follistatinが主要な神経誘導因子として羊膜動物でも神経分化に役割を持つが、その働き方のメカニズムや発生における必要性は種ごとに少しずつ異なると考えられている。ただしこの違いは、動物による実験方法の違いによる(たとえば両生類でよく使われる遺伝子の顕微注入法(効率的な強制発現)はマウス胚では実行が難しく、マウスで多用される遺伝学的方法は両生類では難しい)という議論もある[27]。
神経前駆細胞を個性づける遺伝子の発現機構
Sox2は、脊椎動物の神経化した細胞で最初に発現する転写因子の1つであり、神経化した細胞のマーカーとして多用されるだけでなくSox2自体も細胞の前駆性を維持する働きを持つ[52] [53] [54]。したがって、Sox2のエンハンサー解析を行うことにより、未分化細胞が神経化する細胞内のメカニズムが明らかになると思われる。
Sox2は神経前駆細胞以外にも発現するため、その制御領域はSox2のコーディング領域の前後それぞれ50kbにわたって散在するが、このうち神経前駆細胞での発現に関与する制御領域が2つ見つかっている[53]。これらの領域はFGFとWntに反応するシーケンスをするDNA配列を含んでおり、その活性はBMPシグナルによって不活化される(つまりBMPシグナルが遮断されることが細胞の神経化に必要であるにより活性化される)。
さらに、この領域は中胚葉分化を促進する転写因子Tbx6によっても負に制御される[55] [56]。このことは、未分化細胞が神経外胚葉細胞に分化する過程において、一時的に神経中胚葉(neuromesoderm)と呼ばれる分化段階が存在することを意味する[57] [58]。
また、その発現のタイミングはエピゲノム的な制御によることも明らかになっている[59] [60]。したがって、Sox2の当該エンハンサー領域のクロマチン状態が転写因子を受け付ける状態になり、さらにFGFやWntシグナルを仲介する転写因子が結合したときにSox2の発現が始まるものと考えられる。
幹細胞からの神経分化
マウスやヒトでは、再生医学への展望もあるために、胚性幹細胞(ES細胞)や人工多能性幹細胞(iPS細胞)を神経化する方法論についての研究が進んでいる。
これらの幹細胞をシャーレ上でできるだけ純粋に神経前駆細胞に分化させるには、マウス[61] [62][63]、ヒト[64] [65]ともに、シグナル因子の添加を最小限にした(特に血清に含まれる不特定多数の因子を最小限にした)培地に栄養因子やFGFを加えて単層培養する[66]。この方法により、マウスでは2日程度、ヒトでは5−6日程度で神経前駆細胞が出現する。
視細胞、運動神経、介在ニューロンなど、特定の機能的神経細胞を得たい場合には、この時期から領域決定を促す因子(Wnt、ソニック・ヘッジホッグ、レチノイン酸など)を加えてさらに培養を続ける[67] [68] [69] [70] [71]。
さらに成熟し、さまざまな細胞種からなる機能体を作出したい場合には、神経分化させると同時にembryoid body(幹細胞の細胞塊)を形成させる[72] [73] [74]。
近年この方法を応用し、眼や脳などの完全な機能体「オルガノイド(organoid)」が作り出されるようになった[75] [76]。オルガノイドは、移植医療はもちろんのこと、創薬における薬効の検証系、疾患の試験管内再現など幅広い応用が期待されている。
参考文献
- ↑ 1.0 1.1 1.2
Muñoz-Sanjuán, I., & Brivanlou, A.H. (2002).
Neural induction, the default model and embryonic stem cells. Nature reviews. Neuroscience, 3(4), 271-80. [PubMed:11967557] [WorldCat] [DOI] - ↑
Ozair, M.Z., Kintner, C., & Brivanlou, A.H. (2013).
Neural induction and early patterning in vertebrates. Wiley interdisciplinary reviews. Developmental biology, 2(4), 479-98. [PubMed:24014419] [WorldCat] [DOI] - ↑
Suzuki, A., Ueno, N., & Hemmati-Brivanlou, A. (1997).
Xenopus msx1 mediates epidermal induction and neural inhibition by BMP4. Development (Cambridge, England), 124(16), 3037-44. [PubMed:9272945] [WorldCat] - ↑ 4.0 4.1
Piccolo, S., Sasai, Y., Lu, B., & De Robertis, E.M. (1996).
Dorsoventral patterning in Xenopus: inhibition of ventral signals by direct binding of chordin to BMP-4. Cell, 86(4), 589-98. [PubMed:8752213] [PMC] [WorldCat] [DOI] - ↑
Uchikawa, M., Takemoto, T., Kamachi, Y., & Kondoh, H. (2004).
Efficient identification of regulatory sequences in the chicken genome by a powerful combination of embryo electroporation and genome comparison. Mechanisms of development, 121(9), 1145-58. [PubMed:15296978] [WorldCat] [DOI] - ↑ 6.0 6.1
Sander, K., & Faessler, P.E. (2001).
Introducing the Spemann-Mangold organizer: experiments and insights that generated a key concept in developmental biology. The International journal of developmental biology, 45(1), 1-11. [PubMed:11291840] [WorldCat] - ↑
De Robertis, E.M. (2006).
Spemann's organizer and self-regulation in amphibian embryos. Nature reviews. Molecular cell biology, 7(4), 296-302. [PubMed:16482093] [PMC] [WorldCat] [DOI] - ↑
Smith, W.C., & Harland, R.M. (1992).
Expression cloning of noggin, a new dorsalizing factor localized to the Spemann organizer in Xenopus embryos. Cell, 70(5), 829-40. [PubMed:1339313] [WorldCat] [DOI] - ↑
Sasai, Y., Lu, B., Steinbeisser, H., Geissert, D., Gont, L.K., & De Robertis, E.M. (1994).
Xenopus chordin: a novel dorsalizing factor activated by organizer-specific homeobox genes. Cell, 79(5), 779-90. [PubMed:8001117] [PMC] [WorldCat] [DOI] - ↑
Ueno, N., Ling, N., Ying, S.Y., Esch, F., Shimasaki, S., & Guillemin, R. (1987).
Isolation and partial characterization of follistatin: a single-chain Mr 35,000 monomeric protein that inhibits the release of follicle-stimulating hormone. Proceedings of the National Academy of Sciences of the United States of America, 84(23), 8282-6. [PubMed:3120188] [PMC] [WorldCat] [DOI] - ↑ 11.0 11.1
Hemmati-Brivanlou, A., Kelly, O.G., & Melton, D.A. (1994).
Follistatin, an antagonist of activin, is expressed in the Spemann organizer and displays direct neuralizing activity. Cell, 77(2), 283-95. [PubMed:8168135] [WorldCat] [DOI] - ↑ 12.0 12.1
Sasai, Y., Lu, B., Steinbeisser, H., & De Robertis, E.M. (1995).
Regulation of neural induction by the Chd and Bmp-4 antagonistic patterning signals in Xenopus. Nature, 376(6538), 333-6. [PubMed:7630399] [WorldCat] [DOI] - ↑
Zimmerman, L.B., De Jesús-Escobar, J.M., & Harland, R.M. (1996).
The Spemann organizer signal noggin binds and inactivates bone morphogenetic protein 4. Cell, 86(4), 599-606. [PubMed:8752214] [WorldCat] [DOI] - ↑
Wilson, P.A., & Hemmati-Brivanlou, A. (1995).
Induction of epidermis and inhibition of neural fate by Bmp-4. Nature, 376(6538), 331-3. [PubMed:7630398] [WorldCat] [DOI] - ↑
Suzuki, A., Thies, R.S., Yamaji, N., Song, J.J., Wozney, J.M., Murakami, K., & Ueno, N. (1994).
A truncated bone morphogenetic protein receptor affects dorsal-ventral patterning in the early Xenopus embryo. Proceedings of the National Academy of Sciences of the United States of America, 91(22), 10255-9. [PubMed:7937936] [PMC] [WorldCat] [DOI] - ↑
Fainsod, A., Deissler, K., Yelin, R., Marom, K., Epstein, M., Pillemer, G., ..., & Blum, M. (1997).
The dorsalizing and neural inducing gene follistatin is an antagonist of BMP-4. Mechanisms of development, 63(1), 39-50. [PubMed:9178255] [WorldCat] [DOI] - ↑
Khokha, M.K., Yeh, J., Grammer, T.C., & Harland, R.M. (2005).
Depletion of three BMP antagonists from Spemann's organizer leads to a catastrophic loss of dorsal structures. Developmental cell, 8(3), 401-11. [PubMed:15737935] [WorldCat] [DOI] - ↑
Stockdale, F.E., Sanger, J.W., & Emerson, C.P. (2015).
Howard Holtzer -- developmental and cell biologist 1922-2014. Developmental biology, 401(2), 185-7. [PubMed:26146752] [WorldCat] [DOI] - ↑ Holtzer, H.
A concept in terms of mechanisms. Epithelial-Mesenchymal Interactions.
in R. Gleischmajer and R. E. Billingham (eds.), 152-164 (1968). - ↑
Duester, G. (2008).
Retinoic acid synthesis and signaling during early organogenesis. Cell, 134(6), 921-31. [PubMed:18805086] [PMC] [WorldCat] [DOI] - ↑ 21.0 21.1
Kuroda, H., Fuentealba, L., Ikeda, A., Reversade, B., & De Robertis, E.M. (2005).
Default neural induction: neuralization of dissociated Xenopus cells is mediated by Ras/MAPK activation. Genes & development, 19(9), 1022-7. [PubMed:15879552] [PMC] [WorldCat] [DOI] - ↑
Hemmati-Brivanlou, A., & Melton, D. (1997).
Vertebrate embryonic cells will become nerve cells unless told otherwise. Cell, 88(1), 13-7. [PubMed:9019398] [WorldCat] [DOI] - ↑
Wilson, S.I., & Edlund, T. (2001).
Neural induction: toward a unifying mechanism. Nature neuroscience, 4 Suppl, 1161-8. [PubMed:11687825] [WorldCat] [DOI] - ↑ 24.0 24.1 24.2
Delaune, E., Lemaire, P., & Kodjabachian, L. (2005).
Neural induction in Xenopus requires early FGF signalling in addition to BMP inhibition. Development (Cambridge, England), 132(2), 299-310. [PubMed:15590738] [WorldCat] [DOI] - ↑
Pera, E.M., Ikeda, A., Eivers, E., & De Robertis, E.M. (2003).
Integration of IGF, FGF, and anti-BMP signals via Smad1 phosphorylation in neural induction. Genes & development, 17(24), 3023-8. [PubMed:14701872] [PMC] [WorldCat] [DOI] - ↑
Dorey, K., & Amaya, E. (2010).
FGF signalling: diverse roles during early vertebrate embryogenesis. Development (Cambridge, England), 137(22), 3731-42. [PubMed:20978071] [PMC] [WorldCat] [DOI] - ↑ 27.0 27.1
Stern, C.D. (2006).
Neural induction: 10 years on since the 'default model'. Current opinion in cell biology, 18(6), 692-7. [PubMed:17045790] [WorldCat] [DOI] - ↑ 28.0 28.1
Dawid, I.B. (2004).
Organizing the vertebrate embryo--a balance of induction and competence. PLoS biology, 2(5), E127. [PubMed:15138497] [PMC] [WorldCat] [DOI] - ↑ Waddington, C. H.
Organisers and Genes.
Cambridge University Press, 1940, 41-55. - ↑ 30.0 30.1
De Robertis, E.M., & Sasai, Y. (1996).
A common plan for dorsoventral patterning in Bilateria. Nature, 380(6569), 37-40. [PubMed:8598900] [WorldCat] [DOI] - ↑
Srinivasan, S., Rashka, K.E., & Bier, E. (2002).
Creation of a Sog morphogen gradient in the Drosophila embryo. Developmental cell, 2(1), 91-101. [PubMed:11782317] [WorldCat] - ↑
Holley, S.A., Jackson, P.D., Sasai, Y., Lu, B., De Robertis, E.M., Hoffmann, F.M., & Ferguson, E.L. (1995).
A conserved system for dorsal-ventral patterning in insects and vertebrates involving sog and chordin. Nature, 376(6537), 249-53. [PubMed:7617035] [WorldCat] [DOI] - ↑ 33.0 33.1
Holley, S.A., Neul, J.L., Attisano, L., Wrana, J.L., Sasai, Y., O'Connor, M.B., ..., & Ferguson, E.L. (1996).
The Xenopus dorsalizing factor noggin ventralizes Drosophila embryos by preventing DPP from activating its receptor. Cell, 86(4), 607-17. [PubMed:8752215] [WorldCat] [DOI] - ↑
O'Connor, M.B., Umulis, D., Othmer, H.G., & Blair, S.S. (2006).
Shaping BMP morphogen gradients in the Drosophila embryo and pupal wing. Development (Cambridge, England), 133(2), 183-93. [PubMed:16368928] [PMC] [WorldCat] [DOI] - ↑
Marqués, G., Musacchio, M., Shimell, M.J., Wünnenberg-Stapleton, K., Cho, K.W., & O'Connor, M.B. (1997).
Production of a DPP activity gradient in the early Drosophila embryo through the opposing actions of the SOG and TLD proteins. Cell, 91(3), 417-26. [PubMed:9363950] [WorldCat] [DOI] - ↑
Stern, C.D. (2001).
Initial patterning of the central nervous system: how many organizers? Nature reviews. Neuroscience, 2(2), 92-8. [PubMed:11252999] [WorldCat] [DOI] - ↑
Tam, P.P., & Loebel, D.A. (2007).
Gene function in mouse embryogenesis: get set for gastrulation. Nature reviews. Genetics, 8(5), 368-81. [PubMed:17387317] [WorldCat] [DOI] - ↑
Arnold, S.J., & Robertson, E.J. (2009).
Making a commitment: cell lineage allocation and axis patterning in the early mouse embryo. Nature reviews. Molecular cell biology, 10(2), 91-103. [PubMed:19129791] [WorldCat] [DOI] - ↑
Boettger, T., Knoetgen, H., Wittler, L., & Kessel, M. (2001).
The avian organizer. The International journal of developmental biology, 45(1), 281-7. [PubMed:11291858] [WorldCat] - ↑
Stern, C.D. (2000).
Conrad H. Waddington's contributions to avian and mammalian development, 1930-1940. The International journal of developmental biology, 44(1), 15-22. [PubMed:10761841] [WorldCat] - ↑
Connolly, D.J., Patel, K., & Cooke, J. (1997).
Chick noggin is expressed in the organizer and neural plate during axial development, but offers no evidence of involvement in primary axis formation. The International journal of developmental biology, 41(2), 389-96. [PubMed:9184349] [WorldCat] - ↑ 42.0 42.1
Streit, A., Lee, K.J., Woo, I., Roberts, C., Jessell, T.M., & Stern, C.D. (1998).
Chordin regulates primitive streak development and the stability of induced neural cells, but is not sufficient for neural induction in the chick embryo. Development (Cambridge, England), 125(3), 507-19. [PubMed:9425145] [WorldCat] - ↑
Towers, P., Patel, K., Withington, S., Isaac, A., & Cooke, J. (1999).
Flik, a chick follistatin-related gene, functions in gastrular dorsalisation/neural induction and in subsequent maintenance of midline Sonic hedgehog signalling. Developmental biology, 214(2), 298-317. [PubMed:10525336] [WorldCat] [DOI] - ↑ 44.0 44.1 44.2
Bachiller, D., Klingensmith, J., Kemp, C., Belo, J.A., Anderson, R.M., May, S.R., ..., & De Robertis, E.M. (2000).
The organizer factors Chordin and Noggin are required for mouse forebrain development. Nature, 403(6770), 658-61. [PubMed:10688202] [WorldCat] [DOI] - ↑
Wilson, S.I., Rydström, A., Trimborn, T., Willert, K., Nusse, R., Jessell, T.M., & Edlund, T. (2001).
The status of Wnt signalling regulates neural and epidermal fates in the chick embryo. Nature, 411(6835), 325-30. [PubMed:11357137] [WorldCat] [DOI] - ↑
Linker, C., & Stern, C.D. (2004).
Neural induction requires BMP inhibition only as a late step, and involves signals other than FGF and Wnt antagonists. Development (Cambridge, England), 131(22), 5671-81. [PubMed:15509767] [WorldCat] [DOI] - ↑
Matzuk, M.M., Lu, N., Vogel, H., Sellheyer, K., Roop, D.R., & Bradley, A. (1995).
Multiple defects and perinatal death in mice deficient in follistatin. Nature, 374(6520), 360-3. [PubMed:7885475] [WorldCat] [DOI] - ↑
McMahon, J.A., Takada, S., Zimmerman, L.B., Fan, C.M., Harland, R.M., & McMahon, A.P. (1998).
Noggin-mediated antagonism of BMP signaling is required for growth and patterning of the neural tube and somite. Genes & development, 12(10), 1438-52. [PubMed:9585504] [PMC] [WorldCat] [DOI] - ↑
Anderson, R.M., Lawrence, A.R., Stottmann, R.W., Bachiller, D., & Klingensmith, J. (2002).
Chordin and noggin promote organizing centers of forebrain development in the mouse. Development (Cambridge, England), 129(21), 4975-87. [PubMed:12397106] [WorldCat] - ↑ 50.0 50.1
Beddington, R.S., & Robertson, E.J. (1999).
Axis development and early asymmetry in mammals. Cell, 96(2), 195-209. [PubMed:9988215] [WorldCat] [DOI] - ↑
Stower, M.J., & Srinivas, S. (2014).
Heading forwards: anterior visceral endoderm migration in patterning the mouse embryo. Philosophical transactions of the Royal Society of London. Series B, Biological sciences, 369(1657). [PubMed:25349454] [PMC] [WorldCat] [DOI] - ↑
Mizuseki, K., Kishi, M., Matsui, M., Nakanishi, S., & Sasai, Y. (1998).
Xenopus Zic-related-1 and Sox-2, two factors induced by chordin, have distinct activities in the initiation of neural induction. Development (Cambridge, England), 125(4), 579-87. [PubMed:9435279] [WorldCat] - ↑ 53.0 53.1
Uchikawa, M., Ishida, Y., Takemoto, T., Kamachi, Y., & Kondoh, H. (2003).
Functional analysis of chicken Sox2 enhancers highlights an array of diverse regulatory elements that are conserved in mammals. Developmental cell, 4(4), 509-19. [PubMed:12689590] [WorldCat] - ↑
Graham, V., Khudyakov, J., Ellis, P., & Pevny, L. (2003).
SOX2 functions to maintain neural progenitor identity. Neuron, 39(5), 749-65. [PubMed:12948443] [WorldCat] [DOI] - ↑
Takemoto, T., Uchikawa, M., Kamachi, Y., & Kondoh, H. (2006).
Convergence of Wnt and FGF signals in the genesis of posterior neural plate through activation of the Sox2 enhancer N-1. Development (Cambridge, England), 133(2), 297-306. [PubMed:16354715] [WorldCat] [DOI] - ↑
Takemoto, T., Uchikawa, M., Yoshida, M., Bell, D.M., Lovell-Badge, R., Papaioannou, V.E., & Kondoh, H. (2011).
Tbx6-dependent Sox2 regulation determines neural or mesodermal fate in axial stem cells. Nature, 470(7334), 394-8. [PubMed:21331042] [PMC] [WorldCat] [DOI] - ↑
Henrique, D., Abranches, E., Verrier, L., & Storey, K.G. (2015).
Neuromesodermal progenitors and the making of the spinal cord. Development (Cambridge, England), 142(17), 2864-75. [PubMed:26329597] [PMC] [WorldCat] [DOI] - ↑
Gouti, M., Metzis, V., & Briscoe, J. (2015).
The route to spinal cord cell types: a tale of signals and switches. Trends in genetics : TIG, 31(6), 282-9. [PubMed:25823696] [WorldCat] [DOI] - ↑
Papanayotou, C., Mey, A., Birot, A.M., Saka, Y., Boast, S., Smith, J.C., ..., & Stern, C.D. (2008).
A mechanism regulating the onset of Sox2 expression in the embryonic neural plate. PLoS biology, 6(1), e2. [PubMed:18184035] [PMC] [WorldCat] [DOI] - ↑
Bouzas, S.O., Marini, M.S., Torres Zelada, E., Buzzi, A.L., Morales Vicente, D.A., & Strobl-Mazzulla, P.H. (2016).
Epigenetic activation of Sox2 gene in the developing vertebrate neural plate. Molecular biology of the cell, 27(12), 1921-7. [PubMed:27099369] [PMC] [WorldCat] [DOI] - ↑
Ying, Q.L., Stavridis, M., Griffiths, D., Li, M., & Smith, A. (2003).
Conversion of embryonic stem cells into neuroectodermal precursors in adherent monoculture. Nature biotechnology, 21(2), 183-6. [PubMed:12524553] [WorldCat] [DOI] - ↑
Wataya, T., Ando, S., Muguruma, K., Ikeda, H., Watanabe, K., Eiraku, M., ..., & Sasai, Y. (2008).
Minimization of exogenous signals in ES cell culture induces rostral hypothalamic differentiation. Proceedings of the National Academy of Sciences of the United States of America, 105(33), 11796-801. [PubMed:18697938] [PMC] [WorldCat] [DOI] - ↑
Kawasaki, H., Mizuseki, K., Nishikawa, S., Kaneko, S., Kuwana, Y., Nakanishi, S., ..., & Sasai, Y. (2000).
Induction of midbrain dopaminergic neurons from ES cells by stromal cell-derived inducing activity. Neuron, 28(1), 31-40. [PubMed:11086981] [WorldCat] [DOI] - ↑
Zhang, S.C., Wernig, M., Duncan, I.D., Brüstle, O., & Thomson, J.A. (2001).
In vitro differentiation of transplantable neural precursors from human embryonic stem cells. Nature biotechnology, 19(12), 1129-33. [PubMed:11731781] [WorldCat] [DOI] - ↑
Hu, B.Y., Weick, J.P., Yu, J., Ma, L.X., Zhang, X.Q., Thomson, J.A., & Zhang, S.C. (2010).
Neural differentiation of human induced pluripotent stem cells follows developmental principles but with variable potency. Proceedings of the National Academy of Sciences of the United States of America, 107(9), 4335-40. [PubMed:20160098] [PMC] [WorldCat] [DOI] - ↑
Mertens, J., Marchetto, M.C., Bardy, C., & Gage, F.H. (2016).
Evaluating cell reprogramming, differentiation and conversion technologies in neuroscience. Nature reviews. Neuroscience, 17(7), 424-37. [PubMed:27194476] [PMC] [WorldCat] [DOI] - ↑
Wichterle, H., Lieberam, I., Porter, J.A., & Jessell, T.M. (2002).
Directed differentiation of embryonic stem cells into motor neurons. Cell, 110(3), 385-97. [PubMed:12176325] [WorldCat] [DOI] - ↑
Gouti, M., Tsakiridis, A., Wymeersch, F.J., Huang, Y., Kleinjung, J., Wilson, V., & Briscoe, J. (2014).
In vitro generation of neuromesodermal progenitors reveals distinct roles for wnt signalling in the specification of spinal cord and paraxial mesoderm identity. PLoS biology, 12(8), e1001937. [PubMed:25157815] [PMC] [WorldCat] [DOI] - ↑
Kutejova, E., Sasai, N., Shah, A., Gouti, M., & Briscoe, J. (2016).
Neural Progenitors Adopt Specific Identities by Directly Repressing All Alternative Progenitor Transcriptional Programs. Developmental cell, 36(6), 639-53. [PubMed:26972603] [PMC] [WorldCat] [DOI] - ↑
Ikeda, H., Osakada, F., Watanabe, K., Mizuseki, K., Haraguchi, T., Miyoshi, H., ..., & Sasai, Y. (2005).
Generation of Rx+/Pax6+ neural retinal precursors from embryonic stem cells. Proceedings of the National Academy of Sciences of the United States of America, 102(32), 11331-6. [PubMed:16076961] [PMC] [WorldCat] [DOI] - ↑
Lamba, D.A., Karl, M.O., Ware, C.B., & Reh, T.A. (2006).
Efficient generation of retinal progenitor cells from human embryonic stem cells. Proceedings of the National Academy of Sciences of the United States of America, 103(34), 12769-74. [PubMed:16908856] [PMC] [WorldCat] [DOI] - ↑
Watanabe, K., Kamiya, D., Nishiyama, A., Katayama, T., Nozaki, S., Kawasaki, H., ..., & Sasai, Y. (2005).
Directed differentiation of telencephalic precursors from embryonic stem cells. Nature neuroscience, 8(3), 288-96. [PubMed:15696161] [WorldCat] [DOI] - ↑
Watanabe, K., Ueno, M., Kamiya, D., Nishiyama, A., Matsumura, M., Wataya, T., ..., & Sasai, Y. (2007).
A ROCK inhibitor permits survival of dissociated human embryonic stem cells. Nature biotechnology, 25(6), 681-6. [PubMed:17529971] [WorldCat] [DOI] - ↑
Kurosawa, H. (2007).
Methods for inducing embryoid body formation: in vitro differentiation system of embryonic stem cells. Journal of bioscience and bioengineering, 103(5), 389-98. [PubMed:17609152] [WorldCat] [DOI] - ↑
Eiraku, M., Takata, N., Ishibashi, H., Kawada, M., Sakakura, E., Okuda, S., ..., & Sasai, Y. (2011).
Self-organizing optic-cup morphogenesis in three-dimensional culture. Nature, 472(7341), 51-6. [PubMed:21475194] [WorldCat] [DOI] - ↑
Qian, X., Nguyen, H.N., Song, M.M., Hadiono, C., Ogden, S.C., Hammack, C., ..., & Ming, G.L. (2016).
Brain-Region-Specific Organoids Using Mini-bioreactors for Modeling ZIKV Exposure. Cell, 165(5), 1238-1254. [PubMed:27118425] [PMC] [WorldCat] [DOI]