グルコーストランスポーター
大槻 純男
熊本大学大学院 生命科学研究部
DOI:10.14931/bsd.11524 原稿受付日:2026年3月11日 原稿完成日:2026年3月30日
担当編集委員:古屋敷 智之(東京科学大学大学院 医歯学総合研究科 薬理学分野)
英語名:glucose transporter
英略語:GLUT
グルコーストランスポーターは中枢神経系の主要なエネルギー源であるグルコースを輸送基質とする膜輸送タンパク質である。GLUT1は脳毛細血管内皮細胞とアストロサイト、GLUT3は神経細胞、GLUT4は特定の神経細胞に発現し、グルコースの血中から脳への供給や脳内での分配に重要な役割を果たしている。GLUT2は細胞外のグルコースを感知する糖センサーとして役割を果たしている。これらトランスポーターの発現や機能異常は中枢エネルギー恒常性を乱すためさまざまな中枢疾患との関連が報告されている。
グルコーストランスポーターについて
脳は安静時においても全身エネルギー消費の約20%を担う高代謝臓器であり、グルコースはその中枢神経活動の主要なエネルギー源である[1]。グルコースは体循環から血液脳関門を介して脳へ供給された後に脳内の各細胞に分配される。しかし、水溶性化合物であるグルコースは生体膜を受動拡散で透過することができない。そのため膜輸送タンパク質であるグルコーストランスポーターがグルコースの膜輸送を担い、中枢へのグルコース供給と分配に重要な役割を担っている[2]。
グルコースを輸送するトランスポーターには、グルコーストランスポーター(GLUT/SLC2)とナトリウム・グルコース共役輸送体(SGLT/SLC5)がある[3]。グルコーストランスポーターはグルコースを濃度勾配に従って輸送する促進拡散を担う。一方でナトリウム・グルコース共役輸送体は、ナトリウムイオンの濃度勾配を駆動力としてグルコースの能動輸送を担う。本項においては脳におけるグルコース輸送に関わるグルコーストランスポーターを概説する。なお、ナトリウム・グルコース共役輸送体は小腸におけるグルコース吸収や腎尿細管におけるグルコース再吸収に関わっている。
グルコーストランスポーターファミリーには14種類の分子が存在している。その中で中枢神経系で発現する主な分子として、GLUT1/SLC2A1、GLUT2/SLC2A2、GLUT3/SLC2A3、GLUT4/SLC2A4が知られている。
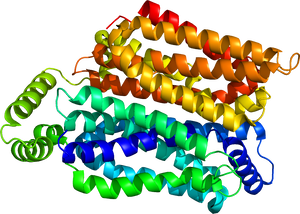
内向き開状態のGLUT1を示す。PDB: 6THAより。
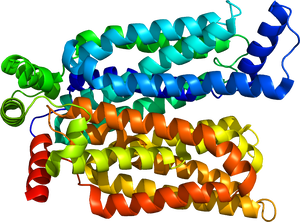
D-glucoseと結合した外向き開状態のGLUT3を示す。PDB: 4ZW9より。
構造
グルコーストランスポーターは、細胞膜を貫通する膜輸送タンパク質であり、12本の膜貫通αヘリックスから構成されている。これらの膜貫通領域はN末端側とC末端側にそれぞれ6本ずつ配置され、両末端は細胞質側に存在する(図1, 2)。膜貫通領域によって形成される中央の空間がグルコース結合部位および輸送経路として機能し、細胞外側と細胞内側のいずれか一方に開いた状態をとることでグルコースを輸送する[4][5]。GLUT1には糖鎖付加型である55kDa型と非糖鎖付加型である45kDa型が存在する[6]。
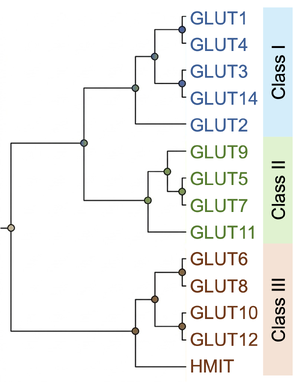
サブファミリー
主に3つのサブファミリー(クラスI、II、III)に分類され、14種類のメンバー(GLUT1-14/SLC2A1-14)で構成される[7](図3)。中枢神経系においてはGLUT1が主に脳毛細血管に発現し、GLUT3が主に神経細胞に発現している。また、インスリン応答性であるGLUT4も特定の神経細胞での発現が報告されている。GLUT2は視床下部弓状核や孤束核などの特定領域の細胞に発現している。GLUT1、GLUT2、GLUT3、GLUT4はクラスIに属している。
発現
GLUT1
多くの組織で広範に発現しているが、赤血球で高発現している。また、血液脳関門などの関門組織の内皮細胞においても高発現している。中枢神経系では、血液脳関門を構成する脳毛細血管内皮細胞の細胞膜(55kDa型)とアストロサイトの細胞膜(45kDa型)に発現する[6]。脳毛細血管内皮細胞においては血液側と脳実質側の両方の細胞膜に発現している[2]。
脳毛細血管のGLUT1の発現は出生直後には低く、成長と共に高くなる。一方でケトン体を輸送するモノカルボン酸トランスポーター1(MCT1/SLC16A1)の脳毛細血管の発現は出生直後に高く、成長と共に低くなる[8][9]。この発現変化は中枢神経系に供給するエネルギーがケトン体からグルコースに変化することに関与していると考えられている。
GLUT2
主に肝臓肝細胞、膵臓β細胞、小腸上皮細胞、腎尿細管上皮細胞に発現している。中枢神経系では、視床下部弓状核のアストロサイトや神経細胞、孤束核のグリア細胞や神経細胞、第三脳室のタニサイトなどに発現している[10]。これらの細胞において、グルコース供給というより細胞外のグルコース濃度を感知する糖センサーとして機能している。
GLUT3
主に神経細胞と胎盤に発現している。神経細胞では主要なグルコーストランスポーターであり、主に樹状突起や軸索末端などの細胞膜に発現している[11]。神経活動により細胞膜への提示が制御されることから、神経活動に伴うエネルギー需要の充足に関わっていると考えられる[12]。
GLUT4
主に骨格筋や脂肪細胞にインスリン応答性グルコーストランスポーターとして発現している。中枢神経系では特定の神経細胞集団に発現しており、ラット脳では海馬や視床下部の神経細胞や小脳プルキンエ細胞などで発現が報告されている[13]。細胞内では主に細胞内小胞に局在している。培養神経細胞では、インスリン刺激や神経活動によって細胞膜に移行し、細胞へのグルコース取込みが増加することが報告されている[14][15]。
機能
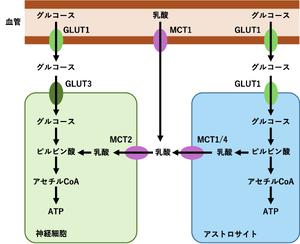
脳内のエネルギー供給については、アストロサイト‐ニューロン乳酸シャトル(ANLS)仮説が提唱されている[16](図4)。血液脳関門のGLUT1により血液から脳へグルコースが供給される。その後、グルコースはアストロサイトに取り込まれ乳酸へ代謝され、その乳酸が神経細胞に供給される。また、血液脳関門のGLUT1により供給されたグルコースの一部はGLUT3により神経細胞に直接取り込まれる[17](図4)。GLUT3によるグルコースの直接供給は神経細胞の基礎代謝を維持し、アストロサイト‐ニューロン乳酸シャトルによるエネルギー供給は急激なエネルギー需要増大への対応や局所的な代謝の安定化を担っていると考えられている。
GLUT1
D-グルコースを主要な基質とするが、D-ガラクトース、D-マンノース、D-グルコサミンも基質とする[18]。血液脳関門を構成する脳毛細血管内皮細胞に発現し、循環血から脳へのグルコースの供給を担っている。また、酸化型ビタミンCであるデヒドロアスコルビン酸も基質とし、血液脳関門を介した循環血から脳へのビタミンCの供給経路となっている[19][20]。
GLUT2
D-グルコースを主要な基質とするが、D-ガラクトース、D-マンノース、D-フルクトースも基質とする[21]。GLUT1やGLUT3と比較して低親和性であり、高容量の輸送活性をもつ。低親和性であるため、細胞内へのグルコース輸送速度が細胞外濃度に比例することにより、糖センサーとして機能する。第三脳室のタニサイトは脳脊髄液中のグルコース濃度を感知して近接する神経核へのシグナルを伝達する役割を担っている。孤束核においてはGLUT2発現細胞が低血糖状態を感知してグルカゴン分泌を促進するための交感神経活動を惹起するセンサーとして機能することが示唆されている。視床下部では糖の報酬価値や探索行動を制御する回路の一部として機能し、海馬においては記憶の調節に関与している可能性が示唆されている[22][21]。
GLUT3
D-グルコースを主要な基質とするが、D-ガラクトース、D-マンノース、キシロース、デヒドロアスコルビン酸も基質とする[18][20]。GLUT1やGLUT4と比較するとグルコースの親和性が高く、かつ高い輸送能を有しており、間液中の低濃度のグルコースを効率よく神経細胞に取り込むと考えられている[11]。また、神経活動に応じてトランスロケーションにより細胞膜上のGLUT3が増加し、ATP産生が増強されることや、記憶・学習との関連が報告されている[23][12]。
GLUT4
D-グルコースを主要な基質とし、親和性はGLUT1と同程度である。主に細胞内小胞に局在し、インスリン刺激や神経活動に応じて細胞膜へ移行することが機能的特徴である。この特徴から、特定の状況において局所的にグルコースの供給を増強する役割を果たしていると考えられる。シナプス活動の亢進時にGLUT4が軸索終末の細胞膜へ移動し、局所的なグルコース取り込みを増強することで、シナプス伝達やシナプス小胞リサイクリングを維持していると報告されている[14][15]。
疾患との関わり
中枢へのグルコース供給の異常は中枢エネルギー恒常性を乱すことから、下記のとおり多数の疾患との関連が報告されている[17]。
- てんかん・発達障害におけるエネルギー需給の破綻
- アルツハイマー病などの神経変性疾患における糖代謝低下
- 脳虚血・低酸素におけるエネルギー供給と代謝の破綻
- 糖尿病・インスリン抵抗性と脳内代謝シグナルの変化
上記のような疾患環境では、グルコース供給を含む血液脳関門としての脳血管機能が変化する。一方で、多数の要因が複雑に影響するため、グルコーストランスポーターと病態との因果関係は各疾患ごとに異なり、注意深く検証する必要がある。
GLUT1欠損症候群
指定難病248
SLC2A1遺伝子のヘテロ接合体変異により血液脳関門から脳内へのグルコースの供給が障害され、乳児期発症のてんかん性脳症、発達遅滞、痙性麻痺、運動失調、不随意運動などの神経症状が引き起こされる疾患であり、髄液糖の減少を特徴とする[24]。てんかんは抗てんかん薬による治療抵抗性である。ケトン食療法が治療として有効であり、てんかん発作を抑制し、知的能力や運動能力を向上させる[25]。2025年7月からアデノ随伴ウイルスベクターを用いた遺伝子治療の臨床試験が開始された[26](https://plaza.umin.ac.jp/~glut1/index.html)。
関連語
参考文献
- ↑
Attwell, D., & Laughlin, S.B. (2001).
An energy budget for signaling in the grey matter of the brain. Journal of cerebral blood flow and metabolism : official journal of the International Society of Cerebral Blood Flow and Metabolism, 21(10), 1133-45. [PubMed:11598490] [WorldCat] [DOI] - ↑ 2.0 2.1
Simpson, I.A., Carruthers, A., & Vannucci, S.J. (2007).
Supply and demand in cerebral energy metabolism: the role of nutrient transporters. Journal of cerebral blood flow and metabolism : official journal of the International Society of Cerebral Blood Flow and Metabolism, 27(11), 1766-91. [PubMed:17579656] [PMC] [WorldCat] [DOI] - ↑
Deng, D., Sun, P., Yan, C., Ke, M., Jiang, X., Xiong, L., ..., & Yan, N. (2015).
Molecular basis of ligand recognition and transport by glucose transporters. Nature, 526(7573), 391-6. [PubMed:26176916] [WorldCat] [DOI] - ↑
Deng, D., Xu, C., Sun, P., Wu, J., Yan, C., Hu, M., & Yan, N. (2014).
Crystal structure of the human glucose transporter GLUT1. Nature, 510(7503), 121-5. [PubMed:24847886] [WorldCat] [DOI] - ↑ 6.0 6.1
Kumagai, A.K., Dwyer, K.J., & Pardridge, W.M. (1994).
Differential glycosylation of the GLUT1 glucose transporter in brain capillaries and choroid plexus. Biochimica et biophysica acta, 1193(1), 24-30. [PubMed:8038191] [WorldCat] [DOI] - ↑
Ismail, A., & Tanasova, M. (2022).
Importance of GLUT Transporters in Disease Diagnosis and Treatment. International journal of molecular sciences, 23(15). [PubMed:35955833] [PMC] [WorldCat] [DOI] - ↑
Hamada, Y., Ogata, S., Masuda, T., Ito, S., & Ohtsuki, S. (2023).
Development of a method for isolating brain capillaries from a single neonatal mouse brain and comparison of proteomic profiles between neonatal and adult brain capillaries. Fluids and barriers of the CNS, 20(1), 50. [PubMed:37353852] [PMC] [WorldCat] [DOI] - ↑
Ito, K., Uchida, Y., Ohtsuki, S., Aizawa, S., Kawakami, H., Katsukura, Y., ..., & Terasaki, T. (2011).
Quantitative membrane protein expression at the blood-brain barrier of adult and younger cynomolgus monkeys. Journal of pharmaceutical sciences, 100(9), 3939-50. [PubMed:21254069] [WorldCat] [DOI] - ↑
Koepsell, H. (2020).
Glucose transporters in brain in health and disease. Pflugers Archiv : European journal of physiology, 472(9), 1299-1343. [PubMed:32789766] [PMC] [WorldCat] [DOI] - ↑ 11.0 11.1
Simpson, I.A., Dwyer, D., Malide, D., Moley, K.H., Travis, A., & Vannucci, S.J. (2008).
The facilitative glucose transporter GLUT3: 20 years of distinction. American journal of physiology. Endocrinology and metabolism, 295(2), E242-53. [PubMed:18577699] [PMC] [WorldCat] [DOI] - ↑ 12.0 12.1
Wei, X.Y., Zou, Z.M., Yao, Z.X., Teng, S.W., Wei, X.Y., Tang, W.J., ..., & Chen, Z.Y. (2025).
Neuronal activity-induced GLUT3 plasma translocation supports energy demands for memory acquisition. Communications biology, 8(1), 1716. [PubMed:41315759] [PMC] [WorldCat] [DOI] - ↑
El Messari, S., Leloup, C., Quignon, M., Brisorgueil, M.J., Penicaud, L., & Arluison, M. (1998).
Immunocytochemical localization of the insulin-responsive glucose transporter 4 (Glut4) in the rat central nervous system. The Journal of comparative neurology, 399(4), 492-512. [PubMed:9741479] [WorldCat] [DOI] - ↑ 14.0 14.1
Ashrafi, G., Wu, Z., Farrell, R.J., & Ryan, T.A. (2017).
GLUT4 Mobilization Supports Energetic Demands of Active Synapses. Neuron, 93(3), 606-615.e3. [PubMed:28111082] [PMC] [WorldCat] [DOI] - ↑ 15.0 15.1
Bakirtzi, K., Belfort, G., Lopez-Coviella, I., Kuruppu, D., Cao, L., Abel, E.D., ..., & Kandror, K.V. (2009).
Cerebellar neurons possess a vesicular compartment structurally and functionally similar to Glut4-storage vesicles from peripheral insulin-sensitive tissues. The Journal of neuroscience : the official journal of the Society for Neuroscience, 29(16), 5193-201. [PubMed:19386915] [PMC] [WorldCat] [DOI] - ↑
Magistretti, P.J., & Allaman, I. (2018).
Lactate in the brain: from metabolic end-product to signalling molecule. Nature reviews. Neuroscience, 19(4), 235-249. [PubMed:29515192] [WorldCat] [DOI] - ↑ 17.0 17.1
Li, X., Yang, M., Wang, T., Liu, S., Han, H., & Dong, P. (2025).
GLUT1 and GLUT3 in brain glucose metabolism: mechanisms, regulation, and implications for metabolic disorders. Metabolic brain disease, 41(1), 3. [PubMed:41405816] [WorldCat] [DOI] - ↑ 18.0 18.1
Mueckler, M., & Thorens, B. (2013).
The SLC2 (GLUT) family of membrane transporters. Molecular aspects of medicine, 34(2-3), 121-38. [PubMed:23506862] [PMC] [WorldCat] [DOI] - ↑
Agus, D.B., Gambhir, S.S., Pardridge, W.M., Spielholz, C., Baselga, J., Vera, J.C., & Golde, D.W. (1997).
Vitamin C crosses the blood-brain barrier in the oxidized form through the glucose transporters. The Journal of clinical investigation, 100(11), 2842-8. [PubMed:9389750] [PMC] [WorldCat] [DOI] - ↑ 20.0 20.1
Vera, J.C., Rivas, C.I., Fischbarg, J., & Golde, D.W. (1993).
Mammalian facilitative hexose transporters mediate the transport of dehydroascorbic acid. Nature, 364(6432), 79-82. [PubMed:8316303] [WorldCat] [DOI] - ↑ 21.0 21.1
Sun, B., Chen, H., Xue, J., Li, P., & Fu, X. (2023).
The role of GLUT2 in glucose metabolism in multiple organs and tissues. Molecular biology reports, 50(8), 6963-6974. [PubMed:37358764] [PMC] [WorldCat] [DOI] - ↑
Elizondo-Vega, R.J., Recabal, A., & Oyarce, K. (2019).
Nutrient Sensing by Hypothalamic Tanycytes. Frontiers in endocrinology, 10, 244. [PubMed:31040827] [PMC] [WorldCat] [DOI] - ↑
Li, H., Guglielmetti, C., Sei, Y.J., Zilberter, M., Le Page, L.M., Shields, L., ..., & Nakamura, K. (2023).
Neurons require glucose uptake and glycolysis in vivo. Cell reports, 42(4), 112335. [PubMed:37027294] [PMC] [WorldCat] [DOI] - ↑
De Vivo, D.C., Trifiletti, R.R., Jacobson, R.I., Ronen, G.M., Behmand, R.A., & Harik, S.I. (1991).
Defective glucose transport across the blood-brain barrier as a cause of persistent hypoglycorrhachia, seizures, and developmental delay. The New England journal of medicine, 325(10), 703-9. [PubMed:1714544] [WorldCat] [DOI] - ↑
Leen, W.G., Klepper, J., Verbeek, M.M., Leferink, M., Hofste, T., van Engelen, B.G., ..., & Willemsen, M.A. (2010).
Glucose transporter-1 deficiency syndrome: the expanding clinical and genetic spectrum of a treatable disorder. Brain : a journal of neurology, 133(Pt 3), 655-70. [PubMed:20129935] [WorldCat] [DOI] - ↑
Nakamura, S., Muramatsu, S.I., Takino, N., Ito, M., Jimbo, E.F., Shimazaki, K., ..., & Osaka, H. (2018).
Gene therapy for Glut1-deficient mouse using an adeno-associated virus vector with the human intrinsic GLUT1 promoter. The journal of gene medicine, 20(4), e3013. [PubMed:29624790] [WorldCat] [DOI]