「長期抑圧」の版間の差分
細編集の要約なし |
細 →分子機構 |
||
| (2人の利用者による、間の6版が非表示) | |||
| 2行目: | 2行目: | ||
<font size="+1">[http://researchmap.jp/read0164591 松田 信爾]</font><br> | <font size="+1">[http://researchmap.jp/read0164591 松田 信爾]</font><br> | ||
''電気通信大学大学院 情報理工学研究科 先進理工学専攻''<br> | ''電気通信大学大学院 情報理工学研究科 先進理工学専攻''<br> | ||
DOI:<selfdoi /> | DOI:<selfdoi /> 原稿受付日:2015年7月17日 原稿完成日:2015年月日<br> | ||
担当編集委員:[http://researchmap.jp/michisukeyuzaki 柚崎 通介](慶應義塾大学 医学部生理学)<br> | 担当編集委員:[http://researchmap.jp/michisukeyuzaki 柚崎 通介](慶應義塾大学 医学部生理学)<br> | ||
</div> | </div> | ||
| 16行目: | 16行目: | ||
[[image:長期抑圧1.png|thumb|350px|'''図1.小脳長期抑圧の分子機構''']] | [[image:長期抑圧1.png|thumb|350px|'''図1.小脳長期抑圧の分子機構''']] | ||
[[小脳]]の長期抑圧は小脳皮質の[[平行線維]]と[[プルキンエ細胞]]間の[[シナプス]] | [[小脳]]の長期抑圧は小脳皮質の[[平行線維]]と[[プルキンエ細胞]]間の[[シナプス]]の伝達効率が長期(数十分間以上)に渡って低下する現象である。プルキンエ細胞への2つの興奮性の入力である平行線維と[[登上線維]]を同時に刺激することで引き起こされる。この際、平行線維と途上繊維の活性化のタイミングが重要であることが知られている<ref name=Finch2012><pubmed>21975855</pubmed></ref>。平行線維の活性化の2~300ミリ秒以内に登上線維が活性化した場合に長期抑圧が起こりやすいことが報告されている。また、平行線維の活動が比較的弱い場合は、長期抑圧は活性化した平行線維シナプスでのみ引き起こされるが、活動の程度が強い場合は付近の活性化されていない平行線維シナプスにおいても長期抑圧が誘導されることも知られている。 | ||
小脳長期抑圧の分子実体は、シナプス後部における[[AMPA型グルタミン酸受容体]](AMPA受容体)の数の減少であると考えられている。このAMPA受容体の数の減少は次の2つのステップを経て引き起こされる。まずAMPA受容体がアンカータンパク質(受容体をシナプス後部につなぎ止めるタンパク質)から解離する(ステップ1)。その後、側方拡散によってendocytic zoneに運ばれ[[エンドサイトーシス]]によって細胞内へ取り込まれる(ステップ2)<ref name=ref1><pubmed>20559335</pubmed></ref>('''図1''')という2つのステップである。 | 小脳長期抑圧の分子実体は、シナプス後部における[[AMPA型グルタミン酸受容体]](AMPA受容体)の数の減少であると考えられている。このAMPA受容体の数の減少は次の2つのステップを経て引き起こされる。まずAMPA受容体がアンカータンパク質(受容体をシナプス後部につなぎ止めるタンパク質)から解離する(ステップ1)。その後、側方拡散によってendocytic zoneに運ばれ[[エンドサイトーシス]]によって細胞内へ取り込まれる(ステップ2)<ref name=ref1><pubmed>20559335</pubmed></ref>('''図1''')という2つのステップである。 | ||
| 24行目: | 24行目: | ||
GRIPから解離したAMPA受容体はステップ2の側方拡散と[[クラスリン]]依存性のエンドサイトーシスによって細胞内へ取り込まれ、細胞表面の数が減少すると考えられている<ref name=ref3><pubmed>12805550</pubmed></ref>。このAMPA受容体のクラスリン依存性のエンドサイトーシスにはAMPA受容体と強固に結合するタンパク質である[[TARP]] ([[Transmembrane AMPA receptor Regulatory Protein]])の脱リン酸化が必須であることが報告されている<ref name=Nomura2012><pubmed>22239345</pubmed></ref>。またリン酸化されたGluA2が[[PICK1]]と結合することも重要であると報告されている<ref name=ref3><pubmed>12805550</pubmed></ref>。 | GRIPから解離したAMPA受容体はステップ2の側方拡散と[[クラスリン]]依存性のエンドサイトーシスによって細胞内へ取り込まれ、細胞表面の数が減少すると考えられている<ref name=ref3><pubmed>12805550</pubmed></ref>。このAMPA受容体のクラスリン依存性のエンドサイトーシスにはAMPA受容体と強固に結合するタンパク質である[[TARP]] ([[Transmembrane AMPA receptor Regulatory Protein]])の脱リン酸化が必須であることが報告されている<ref name=Nomura2012><pubmed>22239345</pubmed></ref>。またリン酸化されたGluA2が[[PICK1]]と結合することも重要であると報告されている<ref name=ref3><pubmed>12805550</pubmed></ref>。 | ||
以上が小脳長期抑圧を司る中核分子の機能であるが、これらの分子の機能を調節する様々な補助分子も報告されている。例えば、プルキンエ細胞に存在する[[δ2グルタミン酸受容体| | 以上が小脳長期抑圧を司る中核分子の機能であるが、これらの分子の機能を調節する様々な補助分子も報告されている。例えば、プルキンエ細胞に存在する[[δ2グルタミン酸受容体|δ<sub>2</sub>グルタミン酸受容体]]を欠損したマウスでは長期抑圧が引き起こされない<ref name=ref4><pubmed>7736576</pubmed></ref>ため、この受容体も長期抑圧に必須の働きを持っていることが知られている。δ<sub>2</sub>グルタミン酸受容体は[[チロシン脱リン酸化酵素]][[PTPMEG]]を介してAMPA受容体GluA2サブユニットの[[チロシン]]のリン酸化状態を制御して小脳長期抑圧に関与していることが報告されている<ref name=ref5><pubmed>23431139</pubmed></ref>。 | ||
さらに[[顆粒細胞]]から放出される[[Cbln1]]というタンパク質<ref name=ref6><pubmed>16234806</pubmed></ref>や[[一酸化窒素]]([[NO]])<ref name=ref7><pubmed>7646893</pubmed></ref>の重要性も指摘されている。NOは[[cGMP]]の合成を促進することで[[cGMP依存性タンパク質リン酸化酵素]] ([[protein kinase G]], [[PKG]])を活性化する。このPKGの活性化も小脳長期抑圧の誘導に重要であると報告されている<ref name=Feil2003><pubmed>14568994</pubmed></ref>。PKGのよりリン酸化されるタンパク質として[[G-substrate]]がよく知られており、このG-substrateは小脳プルキンエ細胞に強く発現していることから、長期抑圧に関与する可能性が考えられるが、G-substrateの欠損マウスの小脳長期抑圧はほぼ正常である<ref name=Endo2009><pubmed>19218432</pubmed></ref>。NOは平行線維―プルキンエ細胞間の[[長期増強]]に必須であるとの報告もあり<ref name=Kakegawa2005><pubmed>16303868</pubmed></ref>、LTD/LTPのバランス制御に関与している可能性がある。 | さらに[[顆粒細胞]]から放出される[[Cbln1]]というタンパク質<ref name=ref6><pubmed>16234806</pubmed></ref>や[[一酸化窒素]]([[NO]])<ref name=ref7><pubmed>7646893</pubmed></ref>の重要性も指摘されている。NOは[[cGMP]]の合成を促進することで[[cGMP依存性タンパク質リン酸化酵素]] ([[protein kinase G]], [[PKG]])を活性化する。このPKGの活性化も小脳長期抑圧の誘導に重要であると報告されている<ref name=Feil2003><pubmed>14568994</pubmed></ref>。PKGのよりリン酸化されるタンパク質として[[G-substrate]]がよく知られており、このG-substrateは小脳プルキンエ細胞に強く発現していることから、長期抑圧に関与する可能性が考えられるが、G-substrateの欠損マウスの小脳長期抑圧はほぼ正常である<ref name=Endo2009><pubmed>19218432</pubmed></ref>。NOは平行線維―プルキンエ細胞間の[[長期増強]]に必須であるとの報告もあり<ref name=Kakegawa2005><pubmed>16303868</pubmed></ref>、LTD/LTPのバランス制御に関与している可能性がある。 | ||
===生理的機能=== | ===生理的機能=== | ||
小脳長期抑圧は意図した運動と実際に起こっている運動とのずれを、末梢からの[[フィードバック]]を利用して補正することで[[運動学習]]に重要な働きを持っていると考えられている。多くの長期抑圧の誘導に異常のある[[遺伝子改変マウス]] | 小脳長期抑圧は意図した運動と実際に起こっている運動とのずれを、末梢からの[[フィードバック]]を利用して補正することで[[運動学習]]に重要な働きを持っていると考えられている。多くの長期抑圧の誘導に異常のある[[遺伝子改変マウス]]では実際に運動学習が障害されている。たとえば上述のδ<sub>2</sub>グルタミン酸受容体を欠損したマウスでは、小脳長期抑圧は誘導されず、同時に[[瞬目反射条件づけ]]が阻害されていることが知られている<ref name=ref4 />。またプルキンエ細胞特異的にPKCの阻害ペプチドを発現させたマウスでも、長期抑圧の誘導が阻害されるのと同時に運動学習の1つである[[前庭動眼反射]]が引き起こされないことも知られている<ref name=ref8><pubmed>9539124</pubmed></ref>。これらのことから小脳長期抑圧はある種の運動学習の基盤となるメカニズムであると考えられている。 | ||
一方、長期抑圧が引き起こされない[[遺伝子改変動物]]でも運動学習が可能であることも報告されており<ref name=ref9><pubmed>21482355</pubmed></ref>、更なる研究が待たれる状況である。さらに小脳は、[[注意欠陥多動性障害]]、[[自閉症]]、[[統合失調症]]、[[読字障害]]等の疾患との関係性も報告されており<ref name=Phillips2015><pubmed>26000269</pubmed></ref> <ref name=Piochon2015><pubmed>25625889</pubmed></ref> <ref name=Stoodley2013><pubmed>22851215</pubmed></ref>、小脳長期抑圧がこれらの疾患に関与する可能性もある。 | 一方、長期抑圧が引き起こされない[[遺伝子改変動物]]でも運動学習が可能であることも報告されており<ref name=ref9><pubmed>21482355</pubmed></ref>、更なる研究が待たれる状況である。さらに小脳は、[[注意欠陥多動性障害]]、[[自閉症]]、[[統合失調症]]、[[読字障害]]等の疾患との関係性も報告されており<ref name=Phillips2015><pubmed>26000269</pubmed></ref> <ref name=Piochon2015><pubmed>25625889</pubmed></ref> <ref name=Stoodley2013><pubmed>22851215</pubmed></ref>、小脳長期抑圧がこれらの疾患に関与する可能性もある。 | ||
| 37行目: | 37行目: | ||
[[image:長期抑圧2.png|thumb|350px|'''図2.NMDA受容体依存型の海馬長期抑圧の分子機構''']] | [[image:長期抑圧2.png|thumb|350px|'''図2.NMDA受容体依存型の海馬長期抑圧の分子機構''']] | ||
[[海馬]]における長期抑圧は小脳と同様に代謝型グルタミン酸受容体の依存するものと[[NMDA型グルタミン酸受容体]](NMDA受容体)に依存するものが存在する。どちらの場合も、AMPA受容体がアンカータンパク質から解離した後、側方拡散によってendocytic | [[海馬]]における長期抑圧は小脳と同様に代謝型グルタミン酸受容体の依存するものと[[NMDA型グルタミン酸受容体]](NMDA受容体)に依存するものが存在する。どちらの場合も、AMPA受容体がアンカータンパク質から解離した後、側方拡散によってendocytic zoneに運ばれエンドサイトーシスによって細胞内へ取り込まれるという2つのステップを経てシナプス後部におけるAMPA受容体の数が減少することがその分子 実体である点では小脳と共通である。しかし、その分子メカニズムについては共通な点とそうでない点がある。 | ||
==== NMDA受容体依存型長期抑圧 ==== | ==== NMDA受容体依存型長期抑圧 ==== | ||
NMDA受容体依存型の長期抑圧はAMPA受容体がアンカータンパク質からの解離メカニズムは、小脳の場合と異なっている可能性がある。小脳長期抑圧に必須であったGluA2サブユニットのser880のリン酸化やPICK1との結合、さらにはPKCの活性化がNMDA依存型の長期抑圧には必要でないことが報告されている<ref name=Collingridge2010><pubmed>20559335</pubmed></ref>。アンカータンパク質からの解離はむしろTARPの[[脱リン酸化]]によるところが大きいと考えられる。NMDA受容体からCa<sup>2+</sup>が流入すると脱リン酸化酵素である[[カルシニューリン]]が活性化される。この活性化されたカルシニューリンがTARPを脱リン酸化する。この脱リン酸化によりTARPはそのアンカータンパク質である[[PSD-95]]から解離し[12]、側方拡散によってendocytic zoneに運ばれ、エンドサイトーシスによって細胞内へ取り込まれる。 | |||
このエンドサイトーシス過程には、カルシニューリン、TARP、[[ホスファチジルイノシトール|ホスファチジルイノシトール2リン酸]]([[ホスファチジルイノシトール|PIP<sub>2</sub>]])を合成する酵素である[[PIP5Kγ]]が必須の働きを持っていることが知られている[1] [10] [11](図2)。NMDA受容体からCa<sup>2+</sup>が流入することにより活性化されたカルシニューリンはTARPと共にPIP5Kγを脱リン酸化する。脱リン酸化されたPIP5Kγは活性化され細胞膜上にPIP2を合成する。このPIP<sub>2</sub>はクラスリン依存性のエンドサイトーシスに必須の脂質であり、PIP<sub>2</sub>に引き寄せられる形でまずアダプタータンパク質複合体の1つである[[AP-2]]が細胞膜上に集積し、このAP-2に引き寄せられてクラスリンが集積しクラスリン被覆ピットが形成されて、エンドサイトーシスが誘導される[11]。また脱リン酸化されたTARPはAP-2に結合性を持っているため、クラスリン被覆ピットに集積し効率的にエンドサイトーシスによって細胞内へと取り込まれていく。エンドサイトーシスによって細胞内へ取り込まれたAMPA受容体は、脱リン酸化TARPと[[AP-3]]との結合により、[[リソソーム]]へと輸送されることで細胞表面へとリサイクルされることなく、長期にわたって細胞表面のAMPA受容体の数が減少すると考えられている[10]。TARPの脱リン酸化は小脳長期抑圧にも必須の現象であるため、このタンパク質が関与する過程は小脳長期抑圧と共通である可能性が高い。一方、AMPA受容体のGluA1のser845のリン酸化状態がAMPA受容体のリサイクリングを制御するという報告もある<ref name=Ehlers2000><pubmed>11144360</pubmed></ref>。TARPとAMPA受容体のリン酸化がそれぞれどのようにLTDに関与しているのかは今後の研究が待たれるところである。 | |||
さらにNMDA受容体依存的な海馬の長期抑圧誘導時に[[樹状突起]]上の[[スパイン]]のサイズや数がカルシニューリン依存的に減少することも知られている<ref name=BoschHayashi2012><pubmed>21963169</pubmed></ref> <ref name=Zhou2004><pubmed>15572107</pubmed></ref>。このスパインのサイズの減少は[[シナプス後膜肥厚]] ([[postsynaptic density]], [[PSD]])の主要なタンパク質である[[アクチン]]のダイナミクスにより引き起こされる。[[細胞骨格]]である[[アクチン|線維状アクチン]] ([[アクチン|F-アクチン]])はスパインの形態やサイズの維持に必須であり、また様々なPSDタンパク質の足場として機能しているが、長期抑圧誘導刺激によりこのF-アクチンが[[アクチン|球状アクチン]] ([[アクチン|G-アクチン]])へと脱重合するため、スパインが縮小するものと考えられている<ref name=Okamoto2004><pubmed>15361876</pubmed></ref>。海馬長期抑圧誘導時に見られるこのスパインサイズの減少は小脳長期抑圧では見られないということが報告されている<ref name=SdrullaLinden2007><pubmed>17435753</pubmed></ref>。一方で、運動学習を繰り返すと小脳プルキンエ細胞のスパインの数が減少するという報告もあり<ref name=Aziz2014><pubmed>24367076</pubmed></ref>、小脳における長期抑圧とスパインの数や形態の変化との関連性については不明な点が多く残されている。 | |||
==== 代謝型グルタミン酸受容体依存型長期抑圧 ==== | ==== 代謝型グルタミン酸受容体依存型長期抑圧 ==== | ||
代謝型グルタミン酸受容体依存性の長期抑圧はNMDA依存性の長期抑圧とは異なり、PKCの活性化<ref name=Oliet1997><pubmed>9208864</pubmed></ref>および、PICK1とGluA2との結合<ref name=Jo2008><pubmed>19109914</pubmed></ref>を必要としていることから小脳長期抑圧とより共通点が多いものと考えられる。また、代謝型グルタミン酸受容体依存性長期抑圧は低分子量Gタンパク質のARF6およびその活性化因子(GEF)であるBRAG2が重要な働きをしていることが報告されている[13]が、これらのタンパク質が小脳長期抑圧に必要か否かは明らかではなく、こちらもさらなる研究が必要とされている。 | |||
また、海馬の長期抑圧はシナプス前部からのグルタミン酸の放出量の低下によって引き起こされる場合もある。この現象はシナプス後部から放出される[[逆行性シグナル]]によって引き起こされる。NDMA受容体依存型の長期抑圧では一酸化窒素 | また、海馬の長期抑圧はシナプス前部からのグルタミン酸の放出量の低下によって引き起こされる場合もある。この現象はシナプス後部から放出される[[逆行性シグナル]]によって引き起こされる。NDMA受容体依存型の長期抑圧では一酸化窒素[14]が、代謝型グルタミン酸受容体依存性の長期抑圧では[[リポキシゲナーゼ]]が逆行性シグナルとして機能し[15]、グルタミン酸の放出量を減少させることが報告されている。 | ||
===生理的機能=== | ===生理的機能=== | ||
海馬における長期抑圧は海馬依存的な[[記憶]] | 海馬における長期抑圧は海馬依存的な[[記憶]]および行動の柔軟性に寄与していると考えられている。例えば、NMDA型グルタミン酸受容体が欠損した海馬の[[CA1]][[錘体細胞]]ではNMDA受容型依存的な長期抑圧が阻害されており、このマウスで[[モリス水迷路テスト]]等の海馬依存的な記憶・学習タスクに異常が見られることが報告されている<ref name=ref16><pubmed>20357110</pubmed></ref>。また、前脳特異的にカルシニューリンが欠損したマウスの海馬ではLTDが障害されており、また[[八方迷路テスト]]等の海馬依存的な記憶に異常が見られることが報告されている<ref name=ref17><pubmed>11733061</pubmed></ref>。さらに前脳で[[プロテインホスファターゼ2A]](PP2A)の活性を阻害した[[トランスジェニックマウス]](SV40のT抗原断片のトランスジェニックマウス)ではNMDA受容体依存的長期抑圧が特異的に阻害されているが、このマウスでは一度記憶した内容を変更する能力が低下していることが明らかになった<ref name=ref18><pubmed>18400167</pubmed></ref>。具体的には水迷路テスト等において一度学習したプラットフォームの位置を変更すると、野生型マウスに比べてトランスジェニックマウスでは新しい位置を覚える能力が低下していた。このことからNMDA依存的長期抑圧は行動の柔軟性に重要な働きを持っていると考えられている。一方、海馬においても小脳と同様にシナプス可塑性と記憶・学習との関連性は不明な点も多い。例えばGluA1欠損マウスでは、海馬における代表的なシナプス可塑性であるシャーファー側枝とCA1錘体細胞間の長期増強が引き起こされないが、上述の水迷路テストでは異常が見られない。このようにシナプス可塑性が個体行動レベルの記憶や学習のどの側面を担っているのかについては海馬も小脳と同様に不明な点が多く、今後も研究が必要である。 | ||
== 関連項目 == | == 関連項目 == | ||
2015年9月4日 (金) 08:40時点における版
松田 信爾
電気通信大学大学院 情報理工学研究科 先進理工学専攻
DOI:10.14931/bsd.6195 原稿受付日:2015年7月17日 原稿完成日:2015年月日
担当編集委員:柚崎 通介(慶應義塾大学 医学部生理学)
英語名:Long Term Depression 英略語:LTD
神経活動に依存してシナプスにおける神経細胞間の情報伝達効率が変化するシナプス可塑性の1種である。長期抑圧が誘導されたシナプスでは神経細胞間の情報伝達効率が長期に渡って低下する。記憶や学習といった高次脳機能の細胞レベルでの基盤ではないかと考えられている。そのメカニズムはプレシナプス(シナプスの軸索側)からの伝達物質の放出量が低下する場合と、シナプス後部(シナプスの樹状突起側)の神経伝達物質受容体のイオン透過性やその数が減少する場合がある。1977年に海馬で[1]、1988年に小脳[2]で報告された現象であるが、他の領域にも広く存在する。
小脳長期抑圧
分子機構
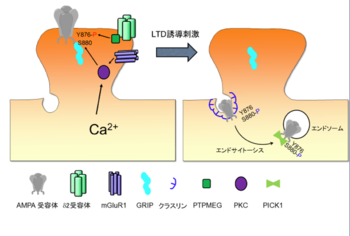
小脳の長期抑圧は小脳皮質の平行線維とプルキンエ細胞間のシナプスの伝達効率が長期(数十分間以上)に渡って低下する現象である。プルキンエ細胞への2つの興奮性の入力である平行線維と登上線維を同時に刺激することで引き起こされる。この際、平行線維と途上繊維の活性化のタイミングが重要であることが知られている[3]。平行線維の活性化の2~300ミリ秒以内に登上線維が活性化した場合に長期抑圧が起こりやすいことが報告されている。また、平行線維の活動が比較的弱い場合は、長期抑圧は活性化した平行線維シナプスでのみ引き起こされるが、活動の程度が強い場合は付近の活性化されていない平行線維シナプスにおいても長期抑圧が誘導されることも知られている。
小脳長期抑圧の分子実体は、シナプス後部におけるAMPA型グルタミン酸受容体(AMPA受容体)の数の減少であると考えられている。このAMPA受容体の数の減少は次の2つのステップを経て引き起こされる。まずAMPA受容体がアンカータンパク質(受容体をシナプス後部につなぎ止めるタンパク質)から解離する(ステップ1)。その後、側方拡散によってendocytic zoneに運ばれエンドサイトーシスによって細胞内へ取り込まれる(ステップ2)[4](図1)という2つのステップである。
ステップ1では細胞内カルシウム濃度の上昇とAMPA受容体のリン酸化が必須の働きをしている。平行線維からの入力による代謝型グルタミン酸受容体mGuR1の活性化されると小胞体からカルシウムが放出される。一方、登上線維からの入力による脱分極により電位依存性カルシウムチャネルからカルシウムが流入する。これらの2つの系統によりプルキンエ細胞内のカルシウム濃度が上昇し、Ca2+/リン脂質依存性タンパク質リン酸化酵素 (Cキナーゼ、PKCが活性化する。活性化されたPKCはAMPA受容体のGluA2サブユニットのC末細胞内領域のセリン残基(S880)をリン酸化し、このリン酸化によってAMPA受容体はアンカータンパク質であるGRIPから解離する[5]。このPKCの活性化はPKC-MAPKのポジティブフィードバック経路により、数十分にわたって継続しうる[6]。
GRIPから解離したAMPA受容体はステップ2の側方拡散とクラスリン依存性のエンドサイトーシスによって細胞内へ取り込まれ、細胞表面の数が減少すると考えられている[7]。このAMPA受容体のクラスリン依存性のエンドサイトーシスにはAMPA受容体と強固に結合するタンパク質であるTARP (Transmembrane AMPA receptor Regulatory Protein)の脱リン酸化が必須であることが報告されている[8]。またリン酸化されたGluA2がPICK1と結合することも重要であると報告されている[7]。
以上が小脳長期抑圧を司る中核分子の機能であるが、これらの分子の機能を調節する様々な補助分子も報告されている。例えば、プルキンエ細胞に存在するδ2グルタミン酸受容体を欠損したマウスでは長期抑圧が引き起こされない[9]ため、この受容体も長期抑圧に必須の働きを持っていることが知られている。δ2グルタミン酸受容体はチロシン脱リン酸化酵素PTPMEGを介してAMPA受容体GluA2サブユニットのチロシンのリン酸化状態を制御して小脳長期抑圧に関与していることが報告されている[10]。
さらに顆粒細胞から放出されるCbln1というタンパク質[11]や一酸化窒素(NO)[12]の重要性も指摘されている。NOはcGMPの合成を促進することでcGMP依存性タンパク質リン酸化酵素 (protein kinase G, PKG)を活性化する。このPKGの活性化も小脳長期抑圧の誘導に重要であると報告されている[13]。PKGのよりリン酸化されるタンパク質としてG-substrateがよく知られており、このG-substrateは小脳プルキンエ細胞に強く発現していることから、長期抑圧に関与する可能性が考えられるが、G-substrateの欠損マウスの小脳長期抑圧はほぼ正常である[14]。NOは平行線維―プルキンエ細胞間の長期増強に必須であるとの報告もあり[15]、LTD/LTPのバランス制御に関与している可能性がある。
生理的機能
小脳長期抑圧は意図した運動と実際に起こっている運動とのずれを、末梢からのフィードバックを利用して補正することで運動学習に重要な働きを持っていると考えられている。多くの長期抑圧の誘導に異常のある遺伝子改変マウスでは実際に運動学習が障害されている。たとえば上述のδ2グルタミン酸受容体を欠損したマウスでは、小脳長期抑圧は誘導されず、同時に瞬目反射条件づけが阻害されていることが知られている[9]。またプルキンエ細胞特異的にPKCの阻害ペプチドを発現させたマウスでも、長期抑圧の誘導が阻害されるのと同時に運動学習の1つである前庭動眼反射が引き起こされないことも知られている[16]。これらのことから小脳長期抑圧はある種の運動学習の基盤となるメカニズムであると考えられている。
一方、長期抑圧が引き起こされない遺伝子改変動物でも運動学習が可能であることも報告されており[17]、更なる研究が待たれる状況である。さらに小脳は、注意欠陥多動性障害、自閉症、統合失調症、読字障害等の疾患との関係性も報告されており[18] [19] [20]、小脳長期抑圧がこれらの疾患に関与する可能性もある。
海馬長期抑圧
分子機構
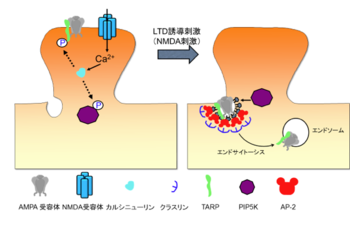
海馬における長期抑圧は小脳と同様に代謝型グルタミン酸受容体の依存するものとNMDA型グルタミン酸受容体(NMDA受容体)に依存するものが存在する。どちらの場合も、AMPA受容体がアンカータンパク質から解離した後、側方拡散によってendocytic zoneに運ばれエンドサイトーシスによって細胞内へ取り込まれるという2つのステップを経てシナプス後部におけるAMPA受容体の数が減少することがその分子 実体である点では小脳と共通である。しかし、その分子メカニズムについては共通な点とそうでない点がある。
NMDA受容体依存型長期抑圧
NMDA受容体依存型の長期抑圧はAMPA受容体がアンカータンパク質からの解離メカニズムは、小脳の場合と異なっている可能性がある。小脳長期抑圧に必須であったGluA2サブユニットのser880のリン酸化やPICK1との結合、さらにはPKCの活性化がNMDA依存型の長期抑圧には必要でないことが報告されている[21]。アンカータンパク質からの解離はむしろTARPの脱リン酸化によるところが大きいと考えられる。NMDA受容体からCa2+が流入すると脱リン酸化酵素であるカルシニューリンが活性化される。この活性化されたカルシニューリンがTARPを脱リン酸化する。この脱リン酸化によりTARPはそのアンカータンパク質であるPSD-95から解離し[12]、側方拡散によってendocytic zoneに運ばれ、エンドサイトーシスによって細胞内へ取り込まれる。
このエンドサイトーシス過程には、カルシニューリン、TARP、ホスファチジルイノシトール2リン酸(PIP2)を合成する酵素であるPIP5Kγが必須の働きを持っていることが知られている[1] [10] [11](図2)。NMDA受容体からCa2+が流入することにより活性化されたカルシニューリンはTARPと共にPIP5Kγを脱リン酸化する。脱リン酸化されたPIP5Kγは活性化され細胞膜上にPIP2を合成する。このPIP2はクラスリン依存性のエンドサイトーシスに必須の脂質であり、PIP2に引き寄せられる形でまずアダプタータンパク質複合体の1つであるAP-2が細胞膜上に集積し、このAP-2に引き寄せられてクラスリンが集積しクラスリン被覆ピットが形成されて、エンドサイトーシスが誘導される[11]。また脱リン酸化されたTARPはAP-2に結合性を持っているため、クラスリン被覆ピットに集積し効率的にエンドサイトーシスによって細胞内へと取り込まれていく。エンドサイトーシスによって細胞内へ取り込まれたAMPA受容体は、脱リン酸化TARPとAP-3との結合により、リソソームへと輸送されることで細胞表面へとリサイクルされることなく、長期にわたって細胞表面のAMPA受容体の数が減少すると考えられている[10]。TARPの脱リン酸化は小脳長期抑圧にも必須の現象であるため、このタンパク質が関与する過程は小脳長期抑圧と共通である可能性が高い。一方、AMPA受容体のGluA1のser845のリン酸化状態がAMPA受容体のリサイクリングを制御するという報告もある[22]。TARPとAMPA受容体のリン酸化がそれぞれどのようにLTDに関与しているのかは今後の研究が待たれるところである。
さらにNMDA受容体依存的な海馬の長期抑圧誘導時に樹状突起上のスパインのサイズや数がカルシニューリン依存的に減少することも知られている[23] [24]。このスパインのサイズの減少はシナプス後膜肥厚 (postsynaptic density, PSD)の主要なタンパク質であるアクチンのダイナミクスにより引き起こされる。細胞骨格である線維状アクチン (F-アクチン)はスパインの形態やサイズの維持に必須であり、また様々なPSDタンパク質の足場として機能しているが、長期抑圧誘導刺激によりこのF-アクチンが球状アクチン (G-アクチン)へと脱重合するため、スパインが縮小するものと考えられている[25]。海馬長期抑圧誘導時に見られるこのスパインサイズの減少は小脳長期抑圧では見られないということが報告されている[26]。一方で、運動学習を繰り返すと小脳プルキンエ細胞のスパインの数が減少するという報告もあり[27]、小脳における長期抑圧とスパインの数や形態の変化との関連性については不明な点が多く残されている。
代謝型グルタミン酸受容体依存型長期抑圧
代謝型グルタミン酸受容体依存性の長期抑圧はNMDA依存性の長期抑圧とは異なり、PKCの活性化[28]および、PICK1とGluA2との結合[29]を必要としていることから小脳長期抑圧とより共通点が多いものと考えられる。また、代謝型グルタミン酸受容体依存性長期抑圧は低分子量Gタンパク質のARF6およびその活性化因子(GEF)であるBRAG2が重要な働きをしていることが報告されている[13]が、これらのタンパク質が小脳長期抑圧に必要か否かは明らかではなく、こちらもさらなる研究が必要とされている。
また、海馬の長期抑圧はシナプス前部からのグルタミン酸の放出量の低下によって引き起こされる場合もある。この現象はシナプス後部から放出される逆行性シグナルによって引き起こされる。NDMA受容体依存型の長期抑圧では一酸化窒素[14]が、代謝型グルタミン酸受容体依存性の長期抑圧ではリポキシゲナーゼが逆行性シグナルとして機能し[15]、グルタミン酸の放出量を減少させることが報告されている。
生理的機能
海馬における長期抑圧は海馬依存的な記憶および行動の柔軟性に寄与していると考えられている。例えば、NMDA型グルタミン酸受容体が欠損した海馬のCA1錘体細胞ではNMDA受容型依存的な長期抑圧が阻害されており、このマウスでモリス水迷路テスト等の海馬依存的な記憶・学習タスクに異常が見られることが報告されている[30]。また、前脳特異的にカルシニューリンが欠損したマウスの海馬ではLTDが障害されており、また八方迷路テスト等の海馬依存的な記憶に異常が見られることが報告されている[31]。さらに前脳でプロテインホスファターゼ2A(PP2A)の活性を阻害したトランスジェニックマウス(SV40のT抗原断片のトランスジェニックマウス)ではNMDA受容体依存的長期抑圧が特異的に阻害されているが、このマウスでは一度記憶した内容を変更する能力が低下していることが明らかになった[32]。具体的には水迷路テスト等において一度学習したプラットフォームの位置を変更すると、野生型マウスに比べてトランスジェニックマウスでは新しい位置を覚える能力が低下していた。このことからNMDA依存的長期抑圧は行動の柔軟性に重要な働きを持っていると考えられている。一方、海馬においても小脳と同様にシナプス可塑性と記憶・学習との関連性は不明な点も多い。例えばGluA1欠損マウスでは、海馬における代表的なシナプス可塑性であるシャーファー側枝とCA1錘体細胞間の長期増強が引き起こされないが、上述の水迷路テストでは異常が見られない。このようにシナプス可塑性が個体行動レベルの記憶や学習のどの側面を担っているのかについては海馬も小脳と同様に不明な点が多く、今後も研究が必要である。
関連項目
参考文献
- ↑
Lynch, G.S., Dunwiddie, T., & Gribkoff, V. (1977).
Heterosynaptic depression: a postsynaptic correlate of long-term potentiation. Nature, 266(5604), 737-9. [PubMed:195211] [WorldCat] [DOI] - ↑
Ito, M., & Kano, M. (1982).
Long-lasting depression of parallel fiber-Purkinje cell transmission induced by conjunctive stimulation of parallel fibers and climbing fibers in the cerebellar cortex. Neuroscience letters, 33(3), 253-8. [PubMed:6298664] [WorldCat] [DOI] - ↑
Finch, E.A., Tanaka, K., & Augustine, G.J. (2012).
Calcium as a trigger for cerebellar long-term synaptic depression. Cerebellum (London, England), 11(3), 706-17. [PubMed:21975855] [WorldCat] [DOI] - ↑
Collingridge, G.L., Peineau, S., Howland, J.G., & Wang, Y.T. (2010).
Long-term depression in the CNS. Nature reviews. Neuroscience, 11(7), 459-73. [PubMed:20559335] [WorldCat] [DOI] - ↑
Matsuda, S., Launey, T., Mikawa, S., & Hirai, H. (2000).
Disruption of AMPA receptor GluR2 clusters following long-term depression induction in cerebellar Purkinje neurons. The EMBO journal, 19(12), 2765-74. [PubMed:10856222] [PMC] [WorldCat] [DOI] - ↑
Tanaka, K., & Augustine, G.J. (2008).
A positive feedback signal transduction loop determines timing of cerebellar long-term depression. Neuron, 59(4), 608-20. [PubMed:18760697] [PMC] [WorldCat] [DOI] - ↑ 7.0 7.1
Chung, H.J., Steinberg, J.P., Huganir, R.L., & Linden, D.J. (2003).
Requirement of AMPA receptor GluR2 phosphorylation for cerebellar long-term depression. Science (New York, N.Y.), 300(5626), 1751-5. [PubMed:12805550] [WorldCat] [DOI] - ↑
Nomura, T., Kakegawa, W., Matsuda, S., Kohda, K., Nishiyama, J., Takahashi, T., & Yuzaki, M. (2012).
Cerebellar long-term depression requires dephosphorylation of TARP in Purkinje cells. The European journal of neuroscience, 35(3), 402-10. [PubMed:22239345] [WorldCat] [DOI] - ↑ 9.0 9.1
Kashiwabuchi, N., Ikeda, K., Araki, K., Hirano, T., Shibuki, K., Takayama, C., ..., & Kang, Y. (1995).
Impairment of motor coordination, Purkinje cell synapse formation, and cerebellar long-term depression in GluR delta 2 mutant mice. Cell, 81(2), 245-52. [PubMed:7736576] [WorldCat] [DOI] - ↑
Kohda, K., Kakegawa, W., Matsuda, S., Yamamoto, T., Hirano, H., & Yuzaki, M. (2013).
The δ2 glutamate receptor gates long-term depression by coordinating interactions between two AMPA receptor phosphorylation sites. Proceedings of the National Academy of Sciences of the United States of America, 110(10), E948-57. [PubMed:23431139] [PMC] [WorldCat] [DOI] - ↑
Hirai, H., Pang, Z., Bao, D., Miyazaki, T., Li, L., Miura, E., ..., & Morgan, J.I. (2005).
Cbln1 is essential for synaptic integrity and plasticity in the cerebellum. Nature neuroscience, 8(11), 1534-41. [PubMed:16234806] [WorldCat] [DOI] - ↑
Lev-Ram, V., Makings, L.R., Keitz, P.F., Kao, J.P., & Tsien, R.Y. (1995).
Long-term depression in cerebellar Purkinje neurons results from coincidence of nitric oxide and depolarization-induced Ca2+ transients. Neuron, 15(2), 407-15. [PubMed:7646893] [WorldCat] [DOI] - ↑
Feil, R., Hartmann, J., Luo, C., Wolfsgruber, W., Schilling, K., Feil, S., ..., & Hofmann, F. (2003).
Impairment of LTD and cerebellar learning by Purkinje cell-specific ablation of cGMP-dependent protein kinase I. The Journal of cell biology, 163(2), 295-302. [PubMed:14568994] [PMC] [WorldCat] [DOI] - ↑
Endo, S., Shutoh, F., Dinh, T.L., Okamoto, T., Ikeda, T., Suzuki, M., ..., & Ito, M. (2009).
Dual involvement of G-substrate in motor learning revealed by gene deletion. Proceedings of the National Academy of Sciences of the United States of America, 106(9), 3525-30. [PubMed:19218432] [PMC] [WorldCat] [DOI] - ↑
Kakegawa, W., & Yuzaki, M. (2005).
A mechanism underlying AMPA receptor trafficking during cerebellar long-term potentiation. Proceedings of the National Academy of Sciences of the United States of America, 102(49), 17846-51. [PubMed:16303868] [PMC] [WorldCat] [DOI] - ↑
De Zeeuw, C.I., Hansel, C., Bian, F., Koekkoek, S.K., van Alphen, A.M., Linden, D.J., & Oberdick, J. (1998).
Expression of a protein kinase C inhibitor in Purkinje cells blocks cerebellar LTD and adaptation of the vestibulo-ocular reflex. Neuron, 20(3), 495-508. [PubMed:9539124] [WorldCat] [DOI] - ↑
Schonewille, M., Gao, Z., Boele, H.J., Veloz, M.F., Amerika, W.E., Simek, A.A., ..., & De Zeeuw, C.I. (2011).
Reevaluating the role of LTD in cerebellar motor learning. Neuron, 70(1), 43-50. [PubMed:21482355] [PMC] [WorldCat] [DOI] - ↑
Phillips, J.R., Hewedi, D.H., Eissa, A.M., & Moustafa, A.A. (2015).
The cerebellum and psychiatric disorders. Frontiers in public health, 3, 66. [PubMed:26000269] [PMC] [WorldCat] [DOI] - ↑
Piochon, C., Kloth, A.D., Grasselli, G., Titley, H.K., Nakayama, H., Hashimoto, K., ..., & Hansel, C. (2015).
Corrigendum: Cerebellar plasticity and motor learning deficits in a copy-number variation mouse model of autism. Nature communications, 6, 6014. [PubMed:25625889] [WorldCat] [DOI] - ↑
Stoodley, C.J., & Stein, J.F. (2013).
Cerebellar function in developmental dyslexia. Cerebellum (London, England), 12(2), 267-76. [PubMed:22851215] [WorldCat] [DOI] - ↑
Collingridge, G.L., Peineau, S., Howland, J.G., & Wang, Y.T. (2010).
Long-term depression in the CNS. Nature reviews. Neuroscience, 11(7), 459-73. [PubMed:20559335] [WorldCat] [DOI] - ↑
Ehlers, M.D. (2000).
Reinsertion or degradation of AMPA receptors determined by activity-dependent endocytic sorting. Neuron, 28(2), 511-25. [PubMed:11144360] [WorldCat] [DOI] - ↑
Bosch, M., & Hayashi, Y. (2012).
Structural plasticity of dendritic spines. Current opinion in neurobiology, 22(3), 383-8. [PubMed:21963169] [PMC] [WorldCat] [DOI] - ↑
Zhou, Q., Homma, K.J., & Poo, M.M. (2004).
Shrinkage of dendritic spines associated with long-term depression of hippocampal synapses. Neuron, 44(5), 749-57. [PubMed:15572107] [WorldCat] [DOI] - ↑
Okamoto, K., Nagai, T., Miyawaki, A., & Hayashi, Y. (2004).
Rapid and persistent modulation of actin dynamics regulates postsynaptic reorganization underlying bidirectional plasticity. Nature neuroscience, 7(10), 1104-12. [PubMed:15361876] [WorldCat] [DOI] - ↑
Sdrulla, A.D., & Linden, D.J. (2007).
Double dissociation between long-term depression and dendritic spine morphology in cerebellar Purkinje cells. Nature neuroscience, 10(5), 546-8. [PubMed:17435753] [WorldCat] [DOI] - ↑
Aziz, W., Wang, W., Kesaf, S., Mohamed, A.A., Fukazawa, Y., & Shigemoto, R. (2014).
Distinct kinetics of synaptic structural plasticity, memory formation, and memory decay in massed and spaced learning. Proceedings of the National Academy of Sciences of the United States of America, 111(1), E194-202. [PubMed:24367076] [PMC] [WorldCat] [DOI] - ↑
Oliet, S.H., Malenka, R.C., & Nicoll, R.A. (1997).
Two distinct forms of long-term depression coexist in CA1 hippocampal pyramidal cells. Neuron, 18(6), 969-82. [PubMed:9208864] [WorldCat] [DOI] - ↑
Jo, J., Heon, S., Kim, M.J., Son, G.H., Park, Y., Henley, J.M., ..., & Cho, K. (2008).
Metabotropic glutamate receptor-mediated LTD involves two interacting Ca(2+) sensors, NCS-1 and PICK1. Neuron, 60(6), 1095-111. [PubMed:19109914] [PMC] [WorldCat] [DOI] - ↑
Brigman, J.L., Wright, T., Talani, G., Prasad-Mulcare, S., Jinde, S., Seabold, G.K., ..., & Holmes, A. (2010).
Loss of GluN2B-containing NMDA receptors in CA1 hippocampus and cortex impairs long-term depression, reduces dendritic spine density, and disrupts learning. The Journal of neuroscience : the official journal of the Society for Neuroscience, 30(13), 4590-600. [PubMed:20357110] [PMC] [WorldCat] [DOI] - ↑
Zeng, H., Chattarji, S., Barbarosie, M., Rondi-Reig, L., Philpot, B.D., Miyakawa, T., ..., & Tonegawa, S. (2001).
Forebrain-specific calcineurin knockout selectively impairs bidirectional synaptic plasticity and working/episodic-like memory. Cell, 107(5), 617-29. [PubMed:11733061] [WorldCat] [DOI] - ↑
Nicholls, R.E., Alarcon, J.M., Malleret, G., Carroll, R.C., Grody, M., Vronskaya, S., & Kandel, E.R. (2008).
Transgenic mice lacking NMDAR-dependent LTD exhibit deficits in behavioral flexibility. Neuron, 58(1), 104-17. [PubMed:18400167] [WorldCat] [DOI]