「シナプス形成」の版間の差分
細編集の要約なし |
|||
| (同じ利用者による、間の2版が非表示) | |||
| 6行目: | 6行目: | ||
</div> | </div> | ||
英:synapse formation, | 英:synapse formation, synaptogenesis 独:Synapsenbildung 仏:formation de synapses | ||
{{box|text= 神経細胞とその相手の細胞(神経細胞、筋肉など)は、シナプスという特殊化した細胞接着構造で結合している。シナプス形成とは、神経回路形成において、機能するシナプスができあがるまでの過程である。化学シナプスの形成には、1) シナプス前部(通常は軸索)が、シナプス後部(神経細胞の樹状突起、筋肉など)となる適切な標的細胞の適切な細胞上の適切な位置に結合すること(シナプス特異性)と、2) | {{box|text= 神経細胞とその相手の細胞(神経細胞、筋肉など)は、シナプスという特殊化した細胞接着構造で結合している。シナプス形成とは、神経回路形成において、機能するシナプスができあがるまでの過程である。化学シナプスの形成には、1) シナプス前部(通常は軸索)が、シナプス後部(神経細胞の樹状突起、筋肉など)となる適切な標的細胞の適切な細胞上の適切な位置に結合すること(シナプス特異性)と、2) シナプス前部と後部がシナプス間隙を介して同じ場所に配向して、シナプス前部にシナプス小胞や分泌装置の蓄積、シナプス後部に神経伝達物質受容体の集合やシナプス後肥厚が生じるということ(シナプス分化)がある。シナプス形成は、シナプス前部とシナプス後部の間の相互作用によって制御されており、このような細胞間相互作用を担うシナプス接着分子、細胞外マトリックス分子、更に分泌性因子が同定されている(シナプスオーガナイザー)。また、グリア細胞など神経細胞以外のプレーヤーの関与も重要である。}} | ||
==はじめに== | ==はじめに== | ||
| 52行目: | 52行目: | ||
==中枢神経系== | ==中枢神経系== | ||
[[中枢神経系]]のシナプスの形成も神経筋接合部のシナプス形成と類似した点が多い。中枢シナプスにおけるシナプス前部とシナプス後部の間の相互作用は、基本的に予め合成されたシナプス構成要素の位置を制御し合うことで、お互いの分化を制御しシナプスを形成すると考えられる<ref name=ref4><pubmed>2655146</pubmed></ref><ref><pubmed>14556707</pubmed></ref><ref><pubmed>17417940</pubmed></ref><ref><pubmed>27462810</pubmed></ref><ref><pubmed>29096080</pubmed></ref><ref name=ref3><pubmed>30359597</pubmed></ref>。そこでは、神経筋接合部のシナプス核のように転写レベルで局所的にシナプス構成要素の生合成を制御することはないが、シナプス近辺での局所的なmRNA翻訳や分解の制御はありうる<ref><pubmed>30861464</pubmed></ref>。その結果、中枢シナプスでも、神経筋接合部と同じように、神経伝達物質の受容体がシナプス後膜に集中し<ref name=ref9><pubmed>22046028</pubmed></ref>、神経伝達物質の違いはあるもののシナプス前部におけるシナプス小胞の分子的な成り立ちも基本的には同じであるように見える<ref name=ref8><pubmed>22794257</pubmed></ref> | [[中枢神経系]]のシナプスの形成も神経筋接合部のシナプス形成と類似した点が多い。中枢シナプスにおけるシナプス前部とシナプス後部の間の相互作用は、基本的に予め合成されたシナプス構成要素の位置を制御し合うことで、お互いの分化を制御しシナプスを形成すると考えられる<ref name=ref4><pubmed>2655146</pubmed></ref><ref><pubmed>14556707</pubmed></ref><ref><pubmed>17417940</pubmed></ref><ref><pubmed>27462810</pubmed></ref><ref><pubmed>29096080</pubmed></ref><ref name=ref3><pubmed>30359597</pubmed></ref>。そこでは、神経筋接合部のシナプス核のように転写レベルで局所的にシナプス構成要素の生合成を制御することはないが、シナプス近辺での局所的なmRNA翻訳や分解の制御はありうる<ref><pubmed>30861464</pubmed></ref>。その結果、中枢シナプスでも、神経筋接合部と同じように、神経伝達物質の受容体がシナプス後膜に集中し<ref name=ref9><pubmed>22046028</pubmed></ref>、神経伝達物質の違いはあるもののシナプス前部におけるシナプス小胞の分子的な成り立ちも基本的には同じであるように見える<ref name=ref8><pubmed>22794257</pubmed></ref>('''図1B''')。 | ||
しかし、中枢シナプスの後部は、神経伝達物質受容体の分子種も異なり、その足場となる分子種も神経筋接合部とは大きく異なっている。特に、神経筋接合部では基底膜という[[細胞外マトリックス]]であったシナプス間隙(約50nm)の様相は中枢シナプスでは全く異なっており典型的な細胞外マトリックスは存在しない。中枢シナプスでは、約20nmのシナプス間隙で直接接触するシナプス前膜とシナプス後膜の間に存在する[[細胞間接着]]がその相互作用の中心であると考えられている<ref><pubmed>14519398</pubmed></ref><ref><pubmed>22278667</pubmed></ref><ref><pubmed>3492943</pubmed></ref><ref><pubmed>20832286</pubmed></ref><ref name=ref3><pubmed>30359597</pubmed></ref><ref name=ref1><pubmed>32359437</pubmed></ref> | しかし、中枢シナプスの後部は、神経伝達物質受容体の分子種も異なり、その足場となる分子種も神経筋接合部とは大きく異なっている。特に、神経筋接合部では基底膜という[[細胞外マトリックス]]であったシナプス間隙(約50nm)の様相は中枢シナプスでは全く異なっており典型的な細胞外マトリックスは存在しない。中枢シナプスでは、約20nmのシナプス間隙で直接接触するシナプス前膜とシナプス後膜の間に存在する[[細胞間接着]]がその相互作用の中心であると考えられている<ref><pubmed>14519398</pubmed></ref><ref><pubmed>22278667</pubmed></ref><ref><pubmed>3492943</pubmed></ref><ref><pubmed>20832286</pubmed></ref><ref name=ref3><pubmed>30359597</pubmed></ref><ref name=ref1><pubmed>32359437</pubmed></ref>('''図1B''')。 | ||
===中枢シナプス形成のオーガナイザー=== | ===中枢シナプス形成のオーガナイザー=== | ||
| 63行目: | 63行目: | ||
一方、[[抑制性シナプス]]のシナプス後部では、[[ゲフィリン]]([[gephyrin]])が重要な足場分子として機能する<ref><pubmed>24552784</pubmed></ref><ref><pubmed>28460365</pubmed></ref>。 | 一方、[[抑制性シナプス]]のシナプス後部では、[[ゲフィリン]]([[gephyrin]])が重要な足場分子として機能する<ref><pubmed>24552784</pubmed></ref><ref><pubmed>28460365</pubmed></ref>。 | ||
4種類あるニューロリギンのうち、[[ニューロリギン1]]は[[グルタミン酸]] | 4種類あるニューロリギンのうち、[[ニューロリギン1]]は[[グルタミン酸]]作動性シナプス、[[ニューロリギン2]]は[[GABA]]作動性シナプス、[[ニューロリギン3]]はグルタミン酸とGABA作動性シナプスの両者、そして[[ニューロリギン4]]は[[グリシン]]作動性シナプスに局在している<ref><pubmed>26209464</pubmed></ref><ref><pubmed>15540461</pubmed></ref><ref><pubmed>17897391</pubmed></ref><ref><pubmed>21282647</pubmed></ref>。培養系の実験では、ニューロリギン1,3,4はグルタミン酸レセプターのクラスタリングを引き起こすが、ニューロリギン2はグルタミン酸レセプターとGABA<sub>A</sub>レセプターのクラスタリングを引き起こす<ref name=ref5><pubmed>15620359</pubmed></ref>。 | ||
しかしながら、ニューレキシンやニューロリギンの遺伝子欠失動物では、予想に反して、シナプスの大きさや数にほとんど影響が見られない<ref><pubmed>12827191</pubmed></ref><ref><pubmed>16982420</pubmed></ref><ref><pubmed>28472659</pubmed></ref>ことから、これらの分子の存在が中枢シナプス形成にどの程度の意味を持っているのかは、実は明らかではない。ニューレキシンやニューロリギンの他にも、シナプス接着分子はシナプス分化の誘発能を持つものやニューレキシンに結合するものも含めて多数報告されてきており<ref><pubmed>29100073</pubmed></ref><ref name=ref3><pubmed>30359597</pubmed></ref><ref name=ref1><pubmed>32359437</pubmed></ref>、冗長性、補償性の高い相互作用システムの一部分である可能性が高い([[シナプス接着因子]]の項参考)。また、同様な証拠から、シナプスオーガナイザーとして知られている[[FGF]]ファミリーや[[Wnt]]ファミリーといった分泌性の因子なども、この冗長な分子ネットワークの一部であると考えられる<ref><pubmed>20646052</pubmed></ref><ref><pubmed>24105999</pubmed></ref><ref><pubmed>29166241</pubmed></ref>。[[線虫]]や[[ショウジョウバエ]]では、変異体スクリーニングなどから、シナプス形成に関わるとされる遺伝子が多く同定されている<ref><pubmed>31037336</pubmed></ref><ref><pubmed>30986749</pubmed></ref><ref><pubmed>32741370</pubmed></ref>。このことからも、[[哺乳類]]の中枢シナプスに関わる分子機構も実際には更に複雑であることが予想される。 | しかしながら、ニューレキシンやニューロリギンの遺伝子欠失動物では、予想に反して、シナプスの大きさや数にほとんど影響が見られない<ref><pubmed>12827191</pubmed></ref><ref><pubmed>16982420</pubmed></ref><ref><pubmed>28472659</pubmed></ref>ことから、これらの分子の存在が中枢シナプス形成にどの程度の意味を持っているのかは、実は明らかではない。ニューレキシンやニューロリギンの他にも、シナプス接着分子はシナプス分化の誘発能を持つものやニューレキシンに結合するものも含めて多数報告されてきており<ref><pubmed>29100073</pubmed></ref><ref name=ref3><pubmed>30359597</pubmed></ref><ref name=ref1><pubmed>32359437</pubmed></ref>、冗長性、補償性の高い相互作用システムの一部分である可能性が高い([[シナプス接着因子]]の項参考)。また、同様な証拠から、シナプスオーガナイザーとして知られている[[FGF]]ファミリーや[[Wnt]]ファミリーといった分泌性の因子なども、この冗長な分子ネットワークの一部であると考えられる<ref><pubmed>20646052</pubmed></ref><ref><pubmed>24105999</pubmed></ref><ref><pubmed>29166241</pubmed></ref>。[[線虫]]や[[ショウジョウバエ]]では、変異体スクリーニングなどから、シナプス形成に関わるとされる遺伝子が多く同定されている<ref><pubmed>31037336</pubmed></ref><ref><pubmed>30986749</pubmed></ref><ref><pubmed>32741370</pubmed></ref>。このことからも、[[哺乳類]]の中枢シナプスに関わる分子機構も実際には更に複雑であることが予想される。 | ||
2020年10月24日 (土) 16:41時点における最新版
山形方人
Harvard University
DOI:10.14931/bsd.9090 原稿受付日:2020年10月22日 原稿完成日:2020年10月24日
担当編集委員:河崎 洋志(金沢大学 医学系 脳神経医学教室)
英:synapse formation, synaptogenesis 独:Synapsenbildung 仏:formation de synapses
神経細胞とその相手の細胞(神経細胞、筋肉など)は、シナプスという特殊化した細胞接着構造で結合している。シナプス形成とは、神経回路形成において、機能するシナプスができあがるまでの過程である。化学シナプスの形成には、1) シナプス前部(通常は軸索)が、シナプス後部(神経細胞の樹状突起、筋肉など)となる適切な標的細胞の適切な細胞上の適切な位置に結合すること(シナプス特異性)と、2) シナプス前部と後部がシナプス間隙を介して同じ場所に配向して、シナプス前部にシナプス小胞や分泌装置の蓄積、シナプス後部に神経伝達物質受容体の集合やシナプス後肥厚が生じるということ(シナプス分化)がある。シナプス形成は、シナプス前部とシナプス後部の間の相互作用によって制御されており、このような細胞間相互作用を担うシナプス接着分子、細胞外マトリックス分子、更に分泌性因子が同定されている(シナプスオーガナイザー)。また、グリア細胞など神経細胞以外のプレーヤーの関与も重要である。
はじめに
神経細胞は、シナプスで適切に結合、情報伝達し、情報処理ユニットとして機能している。シナプス形成は、神経細胞の間で適切な場所で生じるシナプスの構造構築から機能発現までの過程であるが、正常の発生だけでなく、再生や可塑性でも見られ、正常発生でのシナプス形成と基本的には共通するものであると考えられる。しかし、シナプス形成といった場合、発生における化学シナプスの構造構築について議論されることが多いので、本項目もそれを中心に扱う。また、化学シナプスの形成とは本質的に構造の異なる電気シナプス(ギャップジャンクション)の形成については、化学シナプス形成との関係性もあると考えられる[1][2][3]が、本項目では扱わない。
シナプス形成の3ステップ
ステップ1:シナプス特異性
軸索は軸索ガイダンスにより、標的細胞近辺に到達する。軸索は特定の標的細胞と特異的にシナプス結合することで、情報を処理できる機能的回路を作る(cellular specificity)。また、シナプスはシナプス後細胞上の特定の部位に形成される(subcellular specificity)[4][5][6]。この初期のステップについては、「標的認識」の項を参考にされたい。神経伝達物質や標的細胞が持つ受容体などのシナプスの神経化学的形質は、遺伝子にプログラムされて発生していく神経系の細胞に内在的なものと大方考えられているが、シナプス形成後の誘導により変換するケースもあるかもしれない[7]。
ステップ2:シナプス分化
次に、標的細胞と接触する軸索の一部分はシナプス小胞やアクティブゾーンを伴うシナプス前終末へと分化し(presynaptic differentiation)、軸索と接触した標的細胞では局所的に神経伝達物質受容体や細胞内足場タンパク質が集積しシナプス後部へと分化する(postsynaptic differentiation)。シナプス前部とシナプス後部の特殊化は、軸索と標的細胞の間の相互作用で制御される。
この細胞間相互作用についての多くの原理的知見は、運動神経細胞からの軸索が骨格筋線維上で作る巨大で単純なシナプスである神経筋接合部(neuromuscular junction, NMJ)についての20世紀に行われた研究から得られてきた[8]。21世紀になって、小さく多様な中枢神経系でのシナプス形成や無脊椎動物モデル動物のシナプス形成についての分子的な理解が進んでいる[9]。本項目では、特にこのステップについて、原理的な観点から概説する。
ステップ3:シナプス再編成
シナプス形成後は、シナプスの成熟や神経回路の再編成が観察される。発達期においては、シナプス形成は過剰に行われ、神経活動などの影響により過剰なシナプスは除去される[10][11][12][13]。シナプスの除去(synapse elimination)は、神経細胞死と同様に、神経回路を再編する重要な過程であるが、これについては「シナプス刈り込み」の項を参考されたい。シナプス形成は、個体発生の過程だけでなく、成体におけるシナプスの新生や構造変化は、学習と記憶にも重要な役割をし、シナプス形成の異常は、自閉症、精神疾患、認知症などの原因になると考えられている[14][15]。。
神経筋接合部
脊髄動物の神経筋接合部は、脊髄にある運動神経細胞から伸長した軸索終末(シナプス前終末)、筋線維、シュワン細胞の3つの細胞要素からなり、それぞれ神経筋接合部で特徴的に分化している(図1A)。シナプス形成は、運動神経の軸索が、軸索ガイダンスを経て、発生中の筋線維に接近して開始される。成長円錐が神経終末に変化し始めると、神経終末と反対側の筋表面の一部が特殊化し始める。発生が進むと、シナプス間隙(synaptic cleft)を介したシナプス前部とシナプス後部の構造的な特徴が明確になり、最終的に筋線維表面のわずか1000分の1の面積を占める成熟した神経筋接合部となる(図1A)。このように、シナプス前部は、シナプス後部と同じ場所で配向し、シナプス前部では、シナプス小胞、アクティブゾーンなど神経伝達物質(アセチルコリン)の分泌装置や電位依存性カルシウムチャネルなどが集積する。一方、シナプス後部では、効率的なシナプス伝達のために、神経伝達物質受容体(アセチルコリン受容体)とシグナル伝達装置や足場構造が集合する[8][16][17][18]。
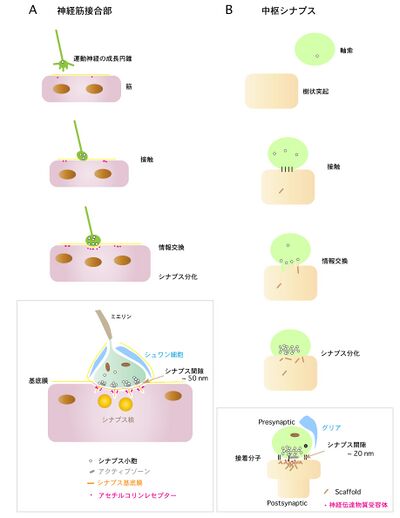
A. 脊椎動物の神経筋接合部。運動神経細胞から伸長した軸索末端が多核の筋線維に接触することで、情報交換が始まる。シナプス前部ではシナプス小胞が集積し、シナプス後部では神経伝達物質受容体であるニコチン性アセチルコリン受容体が集まり始める。成熟した神経筋接合部ではシナプス前部にはシナプス小胞、アクティブゾーンが形成される。シナプス間隙には、シナプス領域で特化したシナプス基底膜が存在し、そこには、アセチルコリンエステラーゼに加え、アグリンやβ2ラミニンなどのシナプスオーガナイザー活性を持つ分子も局在する。シナプス後部には、アセチルコリン受容体が集積し、Rapsynなどの足場分子やMuSK, Lrp4などのシグナル分子も集まる。シナプスの直下では、核も特殊化しており、アセチルコリン受容体遺伝子を強く発現している(本文参考)。Sanes & Lichtman (1999) [8]などを参考にした。
B. 中枢シナプス形成。Vaughn (1989) [19]の形態学的モデルをもとに、神経筋接合部のシナプス形成と対比させた。ここでも、シナプス前部と後部の情報交換により、シナプス分化が開始される。中枢シナプスのシナプス間隙には神経筋接合部とは異なり、基底膜は存在せず、前部と後部の直接的な接着が相互作用の中心であり、シナプス小胞や神経伝達物質受容体が、前部と後部にそれぞれ集積する。興奮性シナプスでは顕著なシナプス後肥厚が形成される。
シナプスオーガナイザー
運動神経細胞と筋線維は、それぞれ独立してシナプス前部とシナプス後部に対応するシナプス構成要素を合成し、自立的に集合させることが可能である。つまり、運動軸索では、筋線維がない状態でもシナプス小胞が見られ、軸索中に保持することができる。一方、筋線維は神経伝達物質受容体であるアセチルコリン受容体を合成し、神経がない状態でも、細胞表面上に多数のアセチルコリン受容体からなる巨大集合構造を作ることができる(クラスタリング、clustering)。したがって、シナプス形成を制御する細胞間相互作用は、シナプス小胞の形成や受容体クラスタリングそのものの誘発因子というより、むしろそれらの位置を決め配向させる指令因子(オーガナイザー、organizer)としての役割が大きい。また、軸索中のシナプス小胞の集積は、ポリリジン被覆ビーズなどとの接触でも容易に引き起こされることから、オーガナイザーとしての役割もAll or nothingといった絶対的なものではなく促進的なものである[20]。しかし、以下に記述するように、シナプス後部やシナプス前部の分化が、それぞれの接触によって誘発、促進される可能性があることを示す証拠もある。これらの証拠のいくつかは、神経筋接合部の再生を利用することで得られた。
シナプス後部の分化
シナプス後部の分化に積極的に関わる分子として想定されたのがアグリン(agrin)である[21]。筋線維は、細胞外マトリックスである基底膜(basement membrane, basal lamina)に包まれている。基底膜の成分は、通常、IV型コラーゲン、ヘパラン硫酸プロテオグリカン(パールカン、perlecan)、ラミニン(laminin)などであるが[22]、神経筋接合部の基底膜(シナプス基底膜 synaptic basement membrane)には、シナプス形成に関わる重要な因子であるヘパラン硫酸プロテオグリカンのアグリン(agrin)が存在する。損傷した筋組織の基底膜を再生する筋肉に接触させると、シナプス後部の特徴を誘導することができる。つまり、基底膜にはアセチルコリン受容体のクラスタリングに関わる因子が存在することが想定され、アグリンは生化学的に精製された(図2A)。
選択的スプライシングによる特殊エクソン由来配列を含むために、強力な受容体クラスタリング能を持つアグリンは運動神経細胞側で発現し、運動神経を通じて末梢に運搬され、神経筋接合部の基底膜に保持される。アグリン欠損マウスでは、神経筋接合部が乱れており、神経筋接合部におけるアセチルコリン受容体クラスターの数、大きさ、密度が減少している[23]。 このことから、アグリンはシナプス後部の分化に関わる神経由来の因子であると考えられる。アグリンは、筋特異的チロシンキナーゼ(MuSK)やLRP4を含むいくつかの受容体に結合して、アダプタータンパク質(Dok7)や細胞骨格タンパク質(Rapsyn)とともに、アセチルコリン受容体のクラスタリングにつながる一連の情報伝達系に影響を与える[24][17][25][26][27][28]。
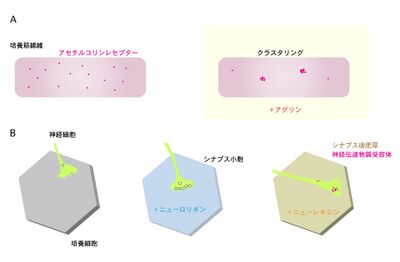
A. 培養下の筋線維に、アグリンを加えると、アセチルコリン受容体がクラスタリングする。アグリン欠損マウスでは、神経筋接合部におけるアセチルコリン受容体クラスターの数、大きさ、密度が減少する[29]。
B. 培養細胞(293細胞など)に、ニューロリギン(通常、シナプス後部の神経細胞で発現)を強制発現させ、その上で神経細胞を培養し神経突起を伸長させると、シナプス小胞の蓄積が観察される[30]。また、ニューレキシン(通常、シナプス前部の神経細胞で発現)を強制発現させると、その上では神経突起にシナプス後肥厚やある種の神経伝達物質受容体が集積する[31]。これらの活性から、これらの分子がシナプス前部や後部の分化と配向に関わるシナプスオーガナイザーであると推定された。
シナプス前部の分化
シナプス前部の分化に関わる分子として同定されたものには、神経筋接合部特異的ラミニンのアイソフォームがある。再生神経の軸索が筋線維に到達すると、基底膜に最初に接触する。この際、筋線維を死滅させ、基底膜を抜け殻のように残したままでも、再生神経は正確に元の神経筋接合部の基底膜上でシナプス前部の分化を起こした[32]。つまり、神経筋接合部のシナプス基底膜には、シナプス前部の分化を指示する因子があると想定され、その後、そのような分子が同定されている。
最もよく研究されているのは、細胞外マトリックス分子ラミニンのアイソフォームである。ラミニンはすべての基底膜の構成分子であり、ラミニンは、α鎖、β鎖、γ鎖のヘテロ3量体であり、少なくとも5本のα鎖、4本のβ鎖、3本のγ鎖のファミリーからなっている。筋線維は複数のラミニンアイソフォームを合成し基底膜に取り込む。シナプス外の通常の筋基底膜にはβ1鎖を含むラミニンが存在するが、神経筋接合部のシナプス間隙の基底膜にはβ2鎖を持つアイソフォームが見られる(ラミニンの系統的命名法ではlaminin-121と呼ばれる)[33]。In vitroでは、β2ラミニンに運動神経の軸索が接触すると伸長を停止し、シナプス小胞を蓄積し、神経伝達物質を放出するようになる。β2ラミニンを欠く変異マウスでは、シナプス前終末およびシュワン細胞の発達に異常が生じる[34]。
シナプス核
中枢シナプスと違う神経筋接合部の際立った特徴は、筋線維が多数の細胞が融合した多核細胞(syncytial muscle; multinucleated muscle)であり、神経筋接合部の直下にはシナプス核(synaptic nucleus)と呼ばれる特殊化した細胞核が存在することである[35](図1A)。シナプス核ではアセチルコリン受容体遺伝子の転写が強く、シナプスから離れた核では転写が低く、アセチルコリン受容体mRNAを局在化させ、神経筋接合部の近辺でアセチルコリン受容体が集まる要因にもなっている。これは、神経が、アセチルコリンを使って、アセチルコリン受容体遺伝子のシナプス外での発現を抑制すると同時に、軸索から放出されるニューレギュリン(neuregulin, ARIA = Acetylcholine Receptor Inducing Activityとも呼ばれた)が、アセチルコリン受容体遺伝子の転写活性化につながるシグナリング分子となっている[36]。
また、発生途中では、アセチルコリン受容体の組成も変化する。幼若期に特有なδサブユニット遺伝子からε遺伝子への発現の変換がおこる[37]。生体で見られる発生初期のアセチルコリン受容体のクラスターは単純なプラーク型であるが、最終的には複雑なプレッツェル型になり、神経筋接合部のひだも形成され、シナプス前終末もそれに対応して成熟する[38]。
中枢神経系
中枢神経系のシナプスの形成も神経筋接合部のシナプス形成と類似した点が多い。中枢シナプスにおけるシナプス前部とシナプス後部の間の相互作用は、基本的に予め合成されたシナプス構成要素の位置を制御し合うことで、お互いの分化を制御しシナプスを形成すると考えられる[19][39][40][41][42][9]。そこでは、神経筋接合部のシナプス核のように転写レベルで局所的にシナプス構成要素の生合成を制御することはないが、シナプス近辺での局所的なmRNA翻訳や分解の制御はありうる[43]。その結果、中枢シナプスでも、神経筋接合部と同じように、神経伝達物質の受容体がシナプス後膜に集中し[44]、神経伝達物質の違いはあるもののシナプス前部におけるシナプス小胞の分子的な成り立ちも基本的には同じであるように見える[45](図1B)。
しかし、中枢シナプスの後部は、神経伝達物質受容体の分子種も異なり、その足場となる分子種も神経筋接合部とは大きく異なっている。特に、神経筋接合部では基底膜という細胞外マトリックスであったシナプス間隙(約50nm)の様相は中枢シナプスでは全く異なっており典型的な細胞外マトリックスは存在しない。中枢シナプスでは、約20nmのシナプス間隙で直接接触するシナプス前膜とシナプス後膜の間に存在する細胞間接着がその相互作用の中心であると考えられている[46][47][48][49][9][6](図1B)。
中枢シナプス形成のオーガナイザー
シナプス前部とシナプス後部をつなぐ細胞接着分子は多数ある(シナプス接着因子の項参考)。それらを代表するものの1つは、シナプス後部の膜に存在するタンパク質であるニューロリギン(neuroligin)である。それに対応するシナプス前膜上の主要なリガンドはニューレキシン(neurexin)である。細胞表面のニューロリギンが、軸索上にシナプス小胞を集積させる能力は、ニューロリギンを強制発現する非神経細胞の上で、神経細胞を培養するin vitroアッセイ系を用いることによって初めて明らかになった[30](図2B)。しかし、in vitroアッセイ系で見られるニューロリギンなどのシナプス接着分子の作用には、非神経細胞上にデフォールトで発現しているカドヘリンのような別の接着分子の存在が前提になるようである[50]。また、RIM、RIM-BP、liprin、Munc13、ELKSを含むいくつかのタンパク質ファミリーが、シナプス前部の重要な足場分子として同定されており[45]、シナプス前膜のLAR-RPTPs(受容体型膜貫通チロシンホスファターゼ)を通じてアクティブゾーンの形成に預かる[51]。
一方、シナプス後部の樹状突起内の一部の神経伝達物質受容体や足場分子は、ニューロリギンのリガンドであるニューレキシンを発現させた非神経細胞と接触する部位で凝集する[31](図2B)。このような神経伝達物質受容体とそのシグナル伝達タンパク質の一部は、アクチン細胞骨格との直接的および間接的な相互作用を介して固定されている。特に、興奮性シナプスで顕著なシナプス後肥厚(postsynaptic density)においては、複数のPDZドメインを持ったPSD95などの細胞内タンパク質が、PDZドメイン結合モチーフを持つニューロリギンなどの膜貫通型接着分子、神経伝達物質受容体、イオンチャネルと複数結合することで、シナプス後部の構成要素をつなぐ足場分子として機能し、ShankやHomerなどの他の足場分子とともに、シナプス構造の構築に関与すると考えられる[44][52][53]。
一方、抑制性シナプスのシナプス後部では、ゲフィリン(gephyrin)が重要な足場分子として機能する[54][55]。
4種類あるニューロリギンのうち、ニューロリギン1はグルタミン酸作動性シナプス、ニューロリギン2はGABA作動性シナプス、ニューロリギン3はグルタミン酸とGABA作動性シナプスの両者、そしてニューロリギン4はグリシン作動性シナプスに局在している[56][57][58][59]。培養系の実験では、ニューロリギン1,3,4はグルタミン酸レセプターのクラスタリングを引き起こすが、ニューロリギン2はグルタミン酸レセプターとGABAAレセプターのクラスタリングを引き起こす[31]。
しかしながら、ニューレキシンやニューロリギンの遺伝子欠失動物では、予想に反して、シナプスの大きさや数にほとんど影響が見られない[60][61][62]ことから、これらの分子の存在が中枢シナプス形成にどの程度の意味を持っているのかは、実は明らかではない。ニューレキシンやニューロリギンの他にも、シナプス接着分子はシナプス分化の誘発能を持つものやニューレキシンに結合するものも含めて多数報告されてきており[63][9][6]、冗長性、補償性の高い相互作用システムの一部分である可能性が高い(シナプス接着因子の項参考)。また、同様な証拠から、シナプスオーガナイザーとして知られているFGFファミリーやWntファミリーといった分泌性の因子なども、この冗長な分子ネットワークの一部であると考えられる[64][65][66]。線虫やショウジョウバエでは、変異体スクリーニングなどから、シナプス形成に関わるとされる遺伝子が多く同定されている[67][68][69]。このことからも、哺乳類の中枢シナプスに関わる分子機構も実際には更に複雑であることが予想される。
中枢神経系の神経細胞の周りには、シナプス部位を囲むようにペリニューロナルネット(perineuronal nets)と呼ばれるプロテオグリカンやヒアルロナンなどを構成要素とする細胞外マトリックスが存在しており、臨界期などでのシナプス形成の制御にも関わっていると考えられている[70][71]。
グリア細胞の役割
これまでシナプス前部とシナプス後部の接点のみに焦点を当ててきたが、シナプス形成には第3の細胞要素であるグリア細胞も関与している[72][9][73]。シュワン細胞は神経筋接合部のグリア細胞であり、アストロサイトは中枢シナプスのグリア細胞である。シュワン細胞がシナプス形成や維持に与える影響については、シュワン細胞を除去した動物での神経筋接合部の異常から考察されている[74]。
グリア細胞の細胞表面にある分子と外部に分泌される分子の両方がシナプス形成に必要である。巨大な細胞外マトリックス分子であるトロンボスポンジン(thrombospondin) [75]、脂質であるコレステロール[76]、ヘヴィン(hevin) [77]などである。アストロサイトから分泌されるヘヴィンは、通常は相互作用しない細胞接着分子であるニューレキシンとニューロリギンの一部のアイソフォームを架橋することにより、シナプス形成を促進する[78]。アストロサイト上のグリピカン(glypican)は、シナプス前終末からAMPA型グルタミン酸受容体クラスタリング因子ペントラキシン1(pentraxin 1)の放出を誘発する[79][80]。また、シナプス形成に拮抗するSPARCなどのシナプスの負の調節因子も知られている[81]。またミクログリアは、シナプス刈り込みに関与することで、神経回路の再編に関与する[82]。
関連項目
参考文献
- ↑
Belousov, A.B., & Fontes, J.D. (2013).
Neuronal gap junctions: making and breaking connections during development and injury. Trends in neurosciences, 36(4), 227-36. [PubMed:23237660] [PMC] [WorldCat] [DOI] - ↑
Miller, A.C., & Pereda, A.E. (2017).
The electrical synapse: Molecular complexities at the gap and beyond. Developmental neurobiology, 77(5), 562-574. [PubMed:28170151] [PMC] [WorldCat] [DOI] - ↑
Jin, E.J., Park, S., Lyu, X., & Jin, Y. (2020).
Gap junctions: historical discoveries and new findings in the Caenorhabditiselegans nervous system. Biology open, 9(8). [PubMed:32883654] [PMC] [WorldCat] [DOI] - ↑
Sanes, J.R., & Yamagata, M. (2009).
Many paths to synaptic specificity. Annual review of cell and developmental biology, 25, 161-95. [PubMed:19575668] [WorldCat] [DOI] - ↑
de Wit, J., & Ghosh, A. (2016).
Specification of synaptic connectivity by cell surface interactions. Nature reviews. Neuroscience, 17(1), 22-35. [PubMed:26656254] [WorldCat] [DOI] - ↑ 6.0 6.1 6.2
Sanes, J.R., & Zipursky, S.L. (2020).
Synaptic Specificity, Recognition Molecules, and Assembly of Neural Circuits. Cell, 181(3), 536-556. [PubMed:32359437] [WorldCat] [DOI] - ↑
Francis, N.J., & Landis, S.C. (1999).
Cellular and molecular determinants of sympathetic neuron development. Annual review of neuroscience, 22, 541-66. [PubMed:10202548] [WorldCat] [DOI] - ↑ 8.0 8.1 8.2
Sanes, J.R., & Lichtman, J.W. (1999).
Development of the vertebrate neuromuscular junction. Annual review of neuroscience, 22, 389-442. [PubMed:10202544] [WorldCat] [DOI] - ↑ 9.0 9.1 9.2 9.3 9.4
Südhof, T.C. (2018).
Towards an Understanding of Synapse Formation. Neuron, 100(2), 276-293. [PubMed:30359597] [PMC] [WorldCat] [DOI] - ↑
Lichtman, J.W., & Colman, H. (2000).
Synapse elimination and indelible memory. Neuron, 25(2), 269-78. [PubMed:10719884] [WorldCat] [DOI] - ↑
Riccomagno, M.M., & Kolodkin, A.L. (2015).
Sculpting neural circuits by axon and dendrite pruning. Annual review of cell and developmental biology, 31, 779-805. [PubMed:26436703] [PMC] [WorldCat] [DOI] - ↑
Stein, I.S., & Zito, K. (2019).
Dendritic Spine Elimination: Molecular Mechanisms and Implications. The Neuroscientist : a review journal bringing neurobiology, neurology and psychiatry, 25(1), 27-47. [PubMed:29716431] [PMC] [WorldCat] [DOI] - ↑
Kano, M., & Watanabe, T. (2019).
Developmental synapse remodeling in the cerebellum and visual thalamus. F1000Research, 8. [PubMed:31372212] [PMC] [WorldCat] [DOI] - ↑
Zoghbi, H.Y., & Bear, M.F. (2012).
Synaptic dysfunction in neurodevelopmental disorders associated with autism and intellectual disabilities. Cold Spring Harbor perspectives in biology, 4(3). [PubMed:22258914] [PMC] [WorldCat] [DOI] - ↑
Ting, J.T., Peça, J., & Feng, G. (2012).
Functional consequences of mutations in postsynaptic scaffolding proteins and relevance to psychiatric disorders. Annual review of neuroscience, 35, 49-71. [PubMed:22540979] [WorldCat] [DOI] - ↑
Darabid, H., Perez-Gonzalez, A.P., & Robitaille, R. (2014).
Neuromuscular synaptogenesis: coordinating partners with multiple functions. Nature reviews. Neuroscience, 15(11), 703-18. [PubMed:25493308] [WorldCat] - ↑ 17.0 17.1
Burden, S.J., Huijbers, M.G., & Remedio, L. (2018).
Fundamental Molecules and Mechanisms for Forming and Maintaining Neuromuscular Synapses. International journal of molecular sciences, 19(2). [PubMed:29415504] [PMC] [WorldCat] [DOI] - ↑
Li, L., Xiong, W.C., & Mei, L. (2018).
Neuromuscular Junction Formation, Aging, and Disorders. Annual review of physiology, 80, 159-188. [PubMed:29195055] [WorldCat] [DOI] - ↑ 19.0 19.1
Vaughn, J.E. (1989).
Fine structure of synaptogenesis in the vertebrate central nervous system. Synapse (New York, N.Y.), 3(3), 255-85. [PubMed:2655146] [WorldCat] [DOI] - ↑
Burry, R.W. (1982).
Development of apparent presynaptic elements formed in response to polylysine coated surfaces. Brain research, 247(1), 1-16. [PubMed:7127105] [WorldCat] [DOI] - ↑
McMahan, U.J. (1990).
The agrin hypothesis. Cold Spring Harbor symposia on quantitative biology, 55, 407-18. [PubMed:1966767] [WorldCat] [DOI] - ↑
Sanes, J.R. (2003).
The basement membrane/basal lamina of skeletal muscle. The Journal of biological chemistry, 278(15), 12601-4. [PubMed:12556454] [WorldCat] [DOI] - ↑
Gautam, M., Noakes, P.G., Moscoso, L., Rupp, F., Scheller, R.H., Merlie, J.P., & Sanes, J.R. (1996).
Defective neuromuscular synaptogenesis in agrin-deficient mutant mice. Cell, 85(4), 525-35. [PubMed:8653788] [WorldCat] [DOI] - ↑
Wu, H., Xiong, W.C., & Mei, L. (2010).
To build a synapse: signaling pathways in neuromuscular junction assembly. Development (Cambridge, England), 137(7), 1017-33. [PubMed:20215342] [PMC] [WorldCat] [DOI] - ↑
DeChiara, T.M., Bowen, D.C., Valenzuela, D.M., Simmons, M.V., Poueymirou, W.T., Thomas, S., ..., & Yancopoulos, G.D. (1996).
The receptor tyrosine kinase MuSK is required for neuromuscular junction formation in vivo. Cell, 85(4), 501-12. [PubMed:8653786] [WorldCat] [DOI] - ↑
Glass, D.J., Bowen, D.C., Stitt, T.N., Radziejewski, C., Bruno, J., Ryan, T.E., ..., & Yancopoulos, G.D. (1996).
Agrin acts via a MuSK receptor complex. Cell, 85(4), 513-23. [PubMed:8653787] [WorldCat] [DOI] - ↑
Okada, K., Inoue, A., Okada, M., Murata, Y., Kakuta, S., Jigami, T., ..., & Yamanashi, Y. (2006).
The muscle protein Dok-7 is essential for neuromuscular synaptogenesis. Science (New York, N.Y.), 312(5781), 1802-5. [PubMed:16794080] [WorldCat] [DOI] - ↑
Gautam, M., Noakes, P.G., Mudd, J., Nichol, M., Chu, G.C., Sanes, J.R., & Merlie, J.P. (1995).
Failure of postsynaptic specialization to develop at neuromuscular junctions of rapsyn-deficient mice. Nature, 377(6546), 232-6. [PubMed:7675108] [WorldCat] [DOI] - ↑
Gautam, M., Noakes, P.G., Moscoso, L., Rupp, F., Scheller, R.H., Merlie, J.P., & Sanes, J.R. (1996).
Defective neuromuscular synaptogenesis in agrin-deficient mutant mice. Cell, 85(4), 525-35. [PubMed:8653788] [WorldCat] [DOI] - ↑ 30.0 30.1
Scheiffele, P., Fan, J., Choih, J., Fetter, R., & Serafini, T. (2000).
Neuroligin expressed in nonneuronal cells triggers presynaptic development in contacting axons. Cell, 101(6), 657-69. [PubMed:10892652] [WorldCat] [DOI] - ↑ 31.0 31.1 31.2
Graf, E.R., Zhang, X., Jin, S.X., Linhoff, M.W., & Craig, A.M. (2004).
Neurexins induce differentiation of GABA and glutamate postsynaptic specializations via neuroligins. Cell, 119(7), 1013-26. [PubMed:15620359] [PMC] [WorldCat] [DOI] - ↑
Sanes, J.R., Marshall, L.M., & McMahan, U.J. (1978).
Reinnervation of muscle fiber basal lamina after removal of myofibers. Differentiation of regenerating axons at original synaptic sites. The Journal of cell biology, 78(1), 176-98. [PubMed:307554] [PMC] [WorldCat] [DOI] - ↑
Hunter, D.D., Shah, V., Merlie, J.P., & Sanes, J.R. (1989).
A laminin-like adhesive protein concentrated in the synaptic cleft of the neuromuscular junction. Nature, 338(6212), 229-34. [PubMed:2922051] [WorldCat] [DOI] - ↑
Noakes, P.G., Gautam, M., Mudd, J., Sanes, J.R., & Merlie, J.P. (1995).
Aberrant differentiation of neuromuscular junctions in mice lacking s-laminin/laminin beta 2. Nature, 374(6519), 258-62. [PubMed:7885444] [WorldCat] [DOI] - ↑
Schaeffer, L., de Kerchove d'Exaerde, A., & Changeux, J.P. (2001).
Targeting transcription to the neuromuscular synapse. Neuron, 31(1), 15-22. [PubMed:11498047] [WorldCat] [DOI] - ↑
Fischbach, G.D., & Rosen, K.M. (1997).
ARIA: a neuromuscular junction neuregulin. Annual review of neuroscience, 20, 429-58. [PubMed:9056721] [WorldCat] [DOI] - ↑
Mishina, M., Takai, T., Imoto, K., Noda, M., Takahashi, T., Numa, S., ..., & Sakmann, B. (1986).
Molecular distinction between fetal and adult forms of muscle acetylcholine receptor. Nature, 321(6068), 406-11. [PubMed:2423878] [WorldCat] [DOI] - ↑
Lichtman, J.W., & Sanes, J.R. (2004).
Watching the neuromuscular junction. Journal of neurocytology, 32(5-8), 767-75. [PubMed:15034266] [WorldCat] [DOI] - ↑
Goda, Y., & Davis, G.W. (2003).
Mechanisms of synapse assembly and disassembly. Neuron, 40(2), 243-64. [PubMed:14556707] [WorldCat] [DOI] - ↑
McAllister, A.K. (2007).
Dynamic aspects of CNS synapse formation. Annual review of neuroscience, 30, 425-50. [PubMed:17417940] [PMC] [WorldCat] [DOI] - ↑
Tang, A.H., Chen, H., Li, T.P., Metzbower, S.R., MacGillavry, H.D., & Blanpied, T.A. (2016).
A trans-synaptic nanocolumn aligns neurotransmitter release to receptors. Nature, 536(7615), 210-4. [PubMed:27462810] [PMC] [WorldCat] [DOI] - ↑
Biederer, T., Kaeser, P.S., & Blanpied, T.A. (2017).
Transcellular Nanoalignment of Synaptic Function. Neuron, 96(3), 680-696. [PubMed:29096080] [PMC] [WorldCat] [DOI] - ↑
Biever, A., Donlin-Asp, P.G., & Schuman, E.M. (2019).
Local translation in neuronal processes. Current opinion in neurobiology, 57, 141-148. [PubMed:30861464] [WorldCat] [DOI] - ↑ 44.0 44.1
Sheng, M., & Kim, E. (2011).
The postsynaptic organization of synapses. Cold Spring Harbor perspectives in biology, 3(12). [PubMed:22046028] [PMC] [WorldCat] [DOI] - ↑ 45.0 45.1
Südhof, T.C. (2012).
The presynaptic active zone. Neuron, 75(1), 11-25. [PubMed:22794257] [PMC] [WorldCat] [DOI] - ↑
Yamagata, M., Sanes, J.R., & Weiner, J.A. (2003).
Synaptic adhesion molecules. Current opinion in cell biology, 15(5), 621-32. [PubMed:14519398] [WorldCat] [DOI] - ↑
Missler, M., Südhof, T.C., & Biederer, T. (2012).
Synaptic cell adhesion. Cold Spring Harbor perspectives in biology, 4(4), a005694. [PubMed:22278667] [PMC] [WorldCat] [DOI] - ↑
Heikkilä, H., Jalonen, J., Arola, M., Hovi-Viander, M., & Laaksonen, V. (1987).
Low-dose enflurane as adjunct to high-dose fentanyl in patients undergoing coronary artery surgery: stable hemodynamics and maintained myocardial oxygen balance. Anesthesia and analgesia, 66(2), 111-6. [PubMed:3492943] [WorldCat] - ↑
Siddiqui, T.J., & Craig, A.M. (2011).
Synaptic organizing complexes. Current opinion in neurobiology, 21(1), 132-43. [PubMed:20832286] [PMC] [WorldCat] [DOI] - ↑
Yamagata, M., Duan, X., & Sanes, J.R. (2018).
Cadherins Interact With Synaptic Organizers to Promote Synaptic Differentiation. Frontiers in molecular neuroscience, 11, 142. [PubMed:29760652] [PMC] [WorldCat] [DOI] - ↑
Um, J.W., & Ko, J. (2013).
LAR-RPTPs: synaptic adhesion molecules that shape synapse development. Trends in cell biology, 23(10), 465-75. [PubMed:23916315] [WorldCat] [DOI] - ↑
Frank, R.A., & Grant, S.G. (2017).
Supramolecular organization of NMDA receptors and the postsynaptic density. Current opinion in neurobiology, 45, 139-147. [PubMed:28577431] [PMC] [WorldCat] [DOI] - ↑
Monteiro, P., & Feng, G. (2017).
SHANK proteins: roles at the synapse and in autism spectrum disorder. Nature reviews. Neuroscience, 18(3), 147-157. [PubMed:28179641] [WorldCat] [DOI] - ↑
Tyagarajan, S.K., & Fritschy, J.M. (2014).
Gephyrin: a master regulator of neuronal function? Nature reviews. Neuroscience, 15(3), 141-56. [PubMed:24552784] [WorldCat] [DOI] - ↑
Krueger-Burg, D., Papadopoulos, T., & Brose, N. (2017).
Organizers of inhibitory synapses come of age. Current opinion in neurobiology, 45, 66-77. [PubMed:28460365] [WorldCat] [DOI] - ↑
Bemben, M.A., Shipman, S.L., Nicoll, R.A., & Roche, K.W. (2015).
The cellular and molecular landscape of neuroligins. Trends in neurosciences, 38(8), 496-505. [PubMed:26209464] [WorldCat] [DOI] - ↑
Varoqueaux, F., Jamain, S., & Brose, N. (2004).
Neuroligin 2 is exclusively localized to inhibitory synapses. European journal of cell biology, 83(9), 449-56. [PubMed:15540461] [WorldCat] [DOI] - ↑
Budreck, E.C., & Scheiffele, P. (2007).
Neuroligin-3 is a neuronal adhesion protein at GABAergic and glutamatergic synapses. The European journal of neuroscience, 26(7), 1738-48. [PubMed:17897391] [WorldCat] [DOI] - ↑
Hoon, M., Soykan, T., Falkenburger, B., Hammer, M., Patrizi, A., Schmidt, K.F., ..., & Varoqueaux, F. (2011).
Neuroligin-4 is localized to glycinergic postsynapses and regulates inhibition in the retina. Proceedings of the National Academy of Sciences of the United States of America, 108(7), 3053-8. [PubMed:21282647] [PMC] [WorldCat] [DOI] - ↑
Missler, M., Zhang, W., Rohlmann, A., Kattenstroth, G., Hammer, R.E., Gottmann, K., & Südhof, T.C. (2003).
Alpha-neurexins couple Ca2+ channels to synaptic vesicle exocytosis. Nature, 423(6943), 939-48. [PubMed:12827191] [WorldCat] [DOI] - ↑
Varoqueaux, F., Aramuni, G., Rawson, R.L., Mohrmann, R., Missler, M., Gottmann, K., ..., & Brose, N. (2006).
Neuroligins determine synapse maturation and function. Neuron, 51(6), 741-54. [PubMed:16982420] [WorldCat] [DOI] - ↑
Chen, L.Y., Jiang, M., Zhang, B., Gokce, O., & Südhof, T.C. (2017).
Conditional Deletion of All Neurexins Defines Diversity of Essential Synaptic Organizer Functions for Neurexins. Neuron, 94(3), 611-625.e4. [PubMed:28472659] [PMC] [WorldCat] [DOI] - ↑
Südhof, T.C. (2017).
Synaptic Neurexin Complexes: A Molecular Code for the Logic of Neural Circuits. Cell, 171(4), 745-769. [PubMed:29100073] [PMC] [WorldCat] [DOI] - ↑
Johnson-Venkatesh, E.M., & Umemori, H. (2010).
Secreted factors as synaptic organizers. The European journal of neuroscience, 32(2), 181-90. [PubMed:20646052] [PMC] [WorldCat] [DOI] - ↑
Stamatakou, E., & Salinas, P.C. (2014).
Postsynaptic assembly: a role for Wnt signaling. Developmental neurobiology, 74(8), 818-27. [PubMed:24105999] [PMC] [WorldCat] [DOI] - ↑
Yuzaki, M. (2018).
Two Classes of Secreted Synaptic Organizers in the Central Nervous System. Annual review of physiology, 80, 243-262. [PubMed:29166241] [WorldCat] [DOI] - ↑
Hendi, A., Kurashina, M., & Mizumoto, K. (2019).
Intrinsic and extrinsic mechanisms of synapse formation and specificity in C. elegans. Cellular and molecular life sciences : CMLS, 76(14), 2719-2738. [PubMed:31037336] [WorldCat] [DOI] - ↑
Kurshan, P.T., & Shen, K. (2019).
Synaptogenic pathways. Current opinion in neurobiology, 57, 156-162. [PubMed:30986749] [WorldCat] [DOI] - ↑
Chou, V.T., Johnson, S.A., & Van Vactor, D. (2020).
Synapse development and maturation at the drosophila neuromuscular junction. Neural development, 15(1), 11. [PubMed:32741370] [PMC] [WorldCat] [DOI] - ↑
Sorg, B.A., Berretta, S., Blacktop, J.M., Fawcett, J.W., Kitagawa, H., Kwok, J.C., & Miquel, M. (2016).
Casting a Wide Net: Role of Perineuronal Nets in Neural Plasticity. The Journal of neuroscience : the official journal of the Society for Neuroscience, 36(45), 11459-11468. [PubMed:27911749] [PMC] [WorldCat] [DOI] - ↑
Fawcett, J.W., Oohashi, T., & Pizzorusso, T. (2019).
The roles of perineuronal nets and the perinodal extracellular matrix in neuronal function. Nature reviews. Neuroscience, 20(8), 451-465. [PubMed:31263252] [WorldCat] [DOI] - ↑
Allen, N.J., & Lyons, D.A. (2018).
Glia as architects of central nervous system formation and function. Science (New York, N.Y.), 362(6411), 181-185. [PubMed:30309945] [PMC] [WorldCat] [DOI] - ↑
Van Horn, M.R., & Ruthazer, E.S. (2019).
Glial regulation of synapse maturation and stabilization in the developing nervous system. Current opinion in neurobiology, 54, 113-119. [PubMed:30347385] [WorldCat] [DOI] - ↑
Barik, A., Li, L., Sathyamurthy, A., Xiong, W.C., & Mei, L. (2016).
Schwann Cells in Neuromuscular Junction Formation and Maintenance. The Journal of neuroscience : the official journal of the Society for Neuroscience, 36(38), 9770-81. [PubMed:27656017] [PMC] [WorldCat] [DOI] - ↑
Christopherson, K.S., Ullian, E.M., Stokes, C.C., Mullowney, C.E., Hell, J.W., Agah, A., ..., & Barres, B.A. (2005).
Thrombospondins are astrocyte-secreted proteins that promote CNS synaptogenesis. Cell, 120(3), 421-33. [PubMed:15707899] [WorldCat] [DOI] - ↑
Pfrieger, F.W. (2003).
Role of cholesterol in synapse formation and function. Biochimica et biophysica acta, 1610(2), 271-80. [PubMed:12648780] [WorldCat] [DOI] - ↑
Kucukdereli, H., Allen, N.J., Lee, A.T., Feng, A., Ozlu, M.I., Conatser, L.M., ..., & Eroglu, C. (2011).
Control of excitatory CNS synaptogenesis by astrocyte-secreted proteins Hevin and SPARC. Proceedings of the National Academy of Sciences of the United States of America, 108(32), E440-9. [PubMed:21788491] [PMC] [WorldCat] [DOI] - ↑
Singh, S.K., Stogsdill, J.A., Pulimood, N.S., Dingsdale, H., Kim, Y.H., Pilaz, L.J., ..., & Eroglu, C. (2016).
Astrocytes Assemble Thalamocortical Synapses by Bridging NRX1α and NL1 via Hevin. Cell, 164(1-2), 183-196. [PubMed:26771491] [PMC] [WorldCat] [DOI] - ↑
Farhy-Tselnicker, I., van Casteren, A.C.M., Lee, A., Chang, V.T., Aricescu, A.R., & Allen, N.J. (2017).
Astrocyte-Secreted Glypican 4 Regulates Release of Neuronal Pentraxin 1 from Axons to Induce Functional Synapse Formation. Neuron, 96(2), 428-445.e13. [PubMed:29024665] [PMC] [WorldCat] [DOI] - ↑
Lee, S.J., Wei, M., Zhang, C., Maxeiner, S., Pak, C., Calado Botelho, S., ..., & Südhof, T.C. (2017).
Presynaptic Neuronal Pentraxin Receptor Organizes Excitatory and Inhibitory Synapses. The Journal of neuroscience : the official journal of the Society for Neuroscience, 37(5), 1062-1080. [PubMed:27986928] [PMC] [WorldCat] [DOI] - ↑
Kucukdereli, H., Allen, N.J., Lee, A.T., Feng, A., Ozlu, M.I., Conatser, L.M., ..., & Eroglu, C. (2011).
Control of excitatory CNS synaptogenesis by astrocyte-secreted proteins Hevin and SPARC. Proceedings of the National Academy of Sciences of the United States of America, 108(32), E440-9. [PubMed:21788491] [PMC] [WorldCat] [DOI] - ↑
Wilton, D.K., Dissing-Olesen, L., & Stevens, B. (2019).
Neuron-Glia Signaling in Synapse Elimination. Annual review of neuroscience, 42, 107-127. [PubMed:31283900] [WorldCat] [DOI]