「成長円錐」の版間の差分
細編集の要約なし |
Tatsuyamori (トーク | 投稿記録) 細編集の要約なし |
||
| (3人の利用者による、間の26版が非表示) | |||
| 1行目: | 1行目: | ||
英語名: Growth cone 独:Wachstumskegel 仏:cône axonique、cône d'émergence de l'axone | |||
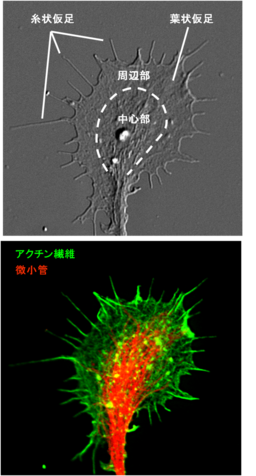
[[Image:成長円錐.png|thumb|256px|<b>図1. 培養したニワトリ胚DRG神経細胞の位相差顕微鏡像 (スケールバーをお願いいたします)</b>]] [[Image:成長円錐3.png|thumb|256x476px|<b>図2.ニワトリ胚DRG神経細胞の成長円錐の微分干渉顕微鏡像(上)とアクチン線維-微小管の二重蛍光顕微鏡像(下)</b>(スケールバーをお願いいたします)]] | |||
</ | |||
成長円錐は伸長中の[[神経突起]]の先端部に見られるアメーバ状の構造物である(図1)。19世紀にスペインの神経科学者[[wikipedia:ja: サンティアゴ・ラモン・イ・カハール|Ramón y Cajal]]により、固定染色した神経組織において[[神経軸索]]先端部に円錐状の構造が発見され、growth cone=成長円錐と名付けられた。2次元基質上で培養した場合は薄く扁平な形態をとり、多くが伸長中の神経軸索の先端に存在するが[[樹状突起]]の先端にも存在する。また、PC12細胞やN1E-115細胞のような[[細胞株|株化細胞]]から伸びる神経突起様構造物の先端にも見られる。軸索の成長円錐の場合、標的神経細胞の樹状突起や組織へと到達した後は形態変化を起こし[[シナプス前部]]となる。成長円錐は極めて高い運動性を示し、[[細胞骨格]]や[[接着分子]]、[[膜輸送]]経路の制御を通じて前方へと移動し、神経突起を牽引することで伸長させる。また、成長円錐の形質膜には[[軸索ガイダンス因子]]に対する受容体が多数発現しており、軸索の成長円錐は細胞外環境に存在する軸索ガイダンス因子に応じてその運動性と進行方向を変化させ、神経軸索を正しい標的細胞へと投射させる。 | 成長円錐は伸長中の[[神経突起]]の先端部に見られるアメーバ状の構造物である(図1)。19世紀にスペインの神経科学者[[wikipedia:ja: サンティアゴ・ラモン・イ・カハール|Ramón y Cajal]]により、固定染色した神経組織において[[神経軸索]]先端部に円錐状の構造が発見され、growth cone=成長円錐と名付けられた。2次元基質上で培養した場合は薄く扁平な形態をとり、多くが伸長中の神経軸索の先端に存在するが[[樹状突起]]の先端にも存在する。また、PC12細胞やN1E-115細胞のような[[細胞株|株化細胞]]から伸びる神経突起様構造物の先端にも見られる。軸索の成長円錐の場合、標的神経細胞の樹状突起や組織へと到達した後は形態変化を起こし[[シナプス前部]]となる。成長円錐は極めて高い運動性を示し、[[細胞骨格]]や[[接着分子]]、[[膜輸送]]経路の制御を通じて前方へと移動し、神経突起を牽引することで伸長させる。また、成長円錐の形質膜には[[軸索ガイダンス因子]]に対する受容体が多数発現しており、軸索の成長円錐は細胞外環境に存在する軸索ガイダンス因子に応じてその運動性と進行方向を変化させ、神経軸索を正しい標的細胞へと投射させる。 | ||
== 構造 == | |||
成長円錐は2次元基質上では扇状に広がった手のような構造で、その形態から[[周辺部]](peripheral domain)と[[中心部]](central domain)の2つの部分に大別される(図2、上)。また、周辺部と中心部の境界部分を[[移行帯]](transition zone)として分類することもある。 | 成長円錐は2次元基質上では扇状に広がった手のような構造で、その形態から[[周辺部]](peripheral domain)と[[中心部]](central domain)の2つの部分に大別される(図2、上)。また、周辺部と中心部の境界部分を[[移行帯]](transition zone)として分類することもある。 | ||
=== 周辺部 === | === 周辺部 === | ||
周辺部は扁平の構造で、成長円錐中央から放射状に伸びた細い指のような[[糸状仮足]](filopodia)の間を、水掻きのような薄いシート状の[[葉状仮足]](lamellipodia)が埋めている(図2)。成長円錐の周辺部は[[アクチン]] | 周辺部は扁平の構造で、成長円錐中央から放射状に伸びた細い指のような[[糸状仮足]](filopodia)の間を、水掻きのような薄いシート状の[[葉状仮足]](lamellipodia)が埋めている(図2)。成長円錐の周辺部は[[アクチン]](actin)繊維に保持されているが、糸状仮足と葉状仮足ではアクチン繊維の形状が異なる。糸状仮足内のアクチン繊維は比較的長い束状の直線的な形状であるのに対し、葉状仮足内では短いアクチン繊維が枝分かれした網目状の構造をしている。また、周辺部には比較的動的な[[微小管]](microtubule)末端も見られる<ref><pubmed> 12105186 </pubmed></ref> 。 | ||
=== 中心部 === | === 中心部 === | ||
中心部は軸索からつながった成長円錐中央部の比較的厚みのある部分で、神経突起から伸びている安定な微小管が主な構成成分である(図2)。中心部は神経突起内の微小管束の末端部分に相当し、中心部における[[チューブリン]] | 中心部は軸索からつながった成長円錐中央部の比較的厚みのある部分で、神経突起から伸びている安定な微小管が主な構成成分である(図2)。中心部は神経突起内の微小管束の末端部分に相当し、中心部における[[チューブリン]]の付加は神経突起の伸長を、脱重合は神経突起の退縮を引き起こす。中心部には比較的安定なアクチン繊維も存在し<ref><pubmed> 14659092 </pubmed></ref>、細胞骨格の他にも[[ミトコンドリア]]や[[小胞体]]などの[[細胞小器官]]、膜小胞なども多く含まれる 。 軸索内の微小管は[[Microtubule-associated proteins]](MAPs)により束ねられているが、中心部では先端部がほどけ、一部の微小管は周辺部に向かって放射状に広がっている。 | ||
=== | === 周辺部におけるアクチン繊維と微小管の役割 === | ||
周辺部のアクチン繊維は糸状仮足、葉状仮足とも[[プラス端]]を外側に向けて配向している。先端部での単量体アクチンの重合によるアクチン繊維の伸長は、糸状仮足や葉状仮足を周辺部に向けて拡大させ、成長円錐の[[wikipedia:ja:形質膜|細胞膜]]は前方に推し進められる。すなわち、周辺部におけるアクチン繊維の重合-脱重合の制御は成長円錐の運動性を規定する大きな要因の一つである。 | |||
周辺部の微小管もアクチン線維と同様にプラス端を外側に向けて配向しており、周辺部への[[細胞接着分子|接着分子]]や膜成分の輸送をガイドする足場として機能する。この微小管依存的な[[膜輸送|小胞輸送]] | 周辺部の微小管もアクチン線維と同様にプラス端を外側に向けて配向しており、周辺部への[[細胞接着分子|接着分子]]や膜成分の輸送をガイドする足場として機能する。この微小管依存的な[[膜輸送|小胞輸送]]経路は成長円錐の旋回運動に重要で、周辺部における微小管の空間的な制御が成長円錐の旋回方向を規定する要因の一つと考えられている。 | ||
さらに、周辺部においてアクチン繊維と微小管は両結合性分子を介して相互作用しており、このアクチン繊維-微小管の相互作用も成長円錐の運動性に大きく関与する。両結合性分子として[[Shot]]、[[Dpod-1]]等が同定されており、これらの分子をを欠く神経細胞では軸索の伸長や走行に異常を示す<ref><pubmed> 11874915</pubmed></ref><ref><pubmed> 12948445 </pubmed></ref> 。 | |||
== 成長円錐前進運動の分子メカニズム == | == 成長円錐前進運動の分子メカニズム == | ||
成長円錐は①周辺部先端での糸状仮足の形成・伸長、②糸状仮足間への葉状仮足の流れ込みによる周辺部の拡大、③後方からの中心部の侵入、という3つの過程を繰り返すことで前方へと移動していく。この成長円錐の前方移動の分子メカニズムとして、[[クラッチ仮説]]が有力なものとして提唱されている<ref><pubmed> 10934316 </pubmed></ref>。クラッチ仮説ではアクチン繊維の後方移動と成長円錐形質膜上に発現する接着分子、接着分子とアクチン繊維をつなぐ[[クラッチ分子]]、接着分子のリサイクリングが協調して働き、成長円錐が前方に移動すると説明される。 (①ー③の過程と、クラッチ仮説を図、または動画で御示し頂く訳にはいかないでしょうか) | |||
=== アクチン繊維の後方移動 === | |||
周辺部に存在するアクチン繊維は、プラス端を成長円錐先端に、[[マイナス端]]を中心部側に向けて規則正しく配置されており、単量体アクチンのアクチン繊維への付加は主に先端部で、アクチン繊維の解離は主に中心部側で起こる。同時にアクチン繊維全体は[[モータータンパク質]]である[[ミオシン]](myosin)Ⅰb<ref><pubmed> 12356865</pubmed></ref>やミオシンⅡ<ref><pubmed> 16501565 </pubmed></ref>の作用により一定の速度(約5 μm/min)で先端部から中心部へと移動している。このアクチン繊維の後方移動を動力源として成長円錐は前進運動すると考えられる。 | |||
=== 接着分子 === | === 接着分子 === | ||
成長円錐の形質膜には[[免疫グロブリン]](immunogloblin)ファミリー、[[カドヘリン]](cadherin)ファミリー、[[インテグリン]](integrin)ファミリーなどの接着分子が発現しており、[[細胞外基質]]、または隣接する細胞との接着を媒介している。多くの場合、細胞外領域での接着分子の[[リガンド]] | 成長円錐の形質膜には[[免疫グロブリン]](immunogloblin)ファミリー、[[カドヘリン]](cadherin)ファミリー、[[インテグリン]](integrin)ファミリーなどの接着分子が発現しており、[[細胞外基質]]、または隣接する細胞との接着を媒介している。多くの場合、細胞外領域での接着分子の[[リガンド]]結合および細胞表面での接着分子のクラスタリングは細胞内領域における接着分子とアクチン繊維間の結合を誘導する。このような接着分子-アクチン繊維間の結合は、接着分子の接着性を増強するとともに、アクチン繊維の後方移動により発生した牽引力を細胞外周囲環境に伝達し、その結果として成長円錐が前方に推進されると考えられている。 | ||
=== クラッチ分子 === | === クラッチ分子 === | ||
成長円錐の前方移動の仕組みを自動車の走行に例えると、エンジンの役割を果たすのがアクチン繊維の動態(重合・脱重合・後方移動)であり、タイヤの役割を果たすのが周辺環境と接着している接着分子である。このエンジンとタイヤをつなぐ役割を果たすものがクラッチ分子と呼ばれ、アクチン繊維の動態を、接着分子を介した成長円錐の推進力へと変換する役割を担っている。成長円錐内においてクラッチ分子の実態および制御機構は不明な点が多いが、アクチン繊維と[[L1]]間のクラッチ分子として[[シューティン]](shootin)が同定され<ref><pubmed> 18519736</pubmed></ref>、[[アンキリン]](ankyrin)や[[カテニン]](catenin)といった[[リンカー分子]]<ref><pubmed> 14657231</pubmed></ref>、[[エズリン]](ezrin)<ref><pubmed> 22219290</pubmed></ref>などもクラッチ分子として機能すると考えられている。 | |||
=== 接着分子のリサイクリング === | === 接着分子のリサイクリング === | ||
アクチン繊維と結合した接着分子は、アクチン繊維の後方移動に伴って成長円錐中心部へと運ばれてしまう。成長円錐ではその前方移動を恒常的に維持するため、後方へ移動した接着分子を周辺環境から脱着し、再び成長円錐先端部へと輸送し再利用する機構が存在すると考えられている。例えば、アクチン繊維の後方移動により中心部に到達したL1は、[[クラスリン]](clathrin)依存的[[エンドサイトーシス]]によって膜小胞に取り込まれた後、微小管のガイドによって細胞質内を成長円錐先端部まで輸送され、形質膜に再挿入される<ref><pubmed> 10804209</pubmed></ref><ref><pubmed> 11717353</pubmed></ref>。このように接着分子は、①成長円錐先端部での基質との接着、②アクチン繊維の後方移動に伴う成長円錐中心部への移動、③基質からの脱着と成長円錐内への取り込み、④成長円錐先端部への輸送、⑤先端部での形質膜への再挿入、という過程でリサイクルされており、成長円錐の恒常的な前進運動の分子基盤となっていると考えられている。(これも図示して頂けないでしょうか) | |||
== 成長円錐と軸索ガイダンス == | == 成長円錐と軸索ガイダンス == | ||
| 63行目: | 53行目: | ||
軸索ガイダンス因子は発生過程の組織内に領域特異的に存在することで成長円錐に空間情報を提供し、成長円錐を正しい標的細胞へと誘導する分子として定義される。生体内における軸索ガイダンス因子は多種多様であるが、大きく4つの作用様式に分類される。細胞外基質や細胞膜に発現し接触を介して近距離に作用する接触因子と、分泌性で濃度勾配によって長距離に作用する拡散性因子、そしてそのそれぞれに対して誘引因子と反発因子が存在する。生体内ではこれら4種類の軸索ガイダンス因子が協調的に働き軸索を正しい標的へ導くと考えられている。成長円錐には個々の軸索ガイダンス因子に対する特異的な受容体ファミリーが存在しており<ref><pubmed> 12471249</pubmed></ref>、受容体の形質膜への発現は軸索ガイダンス因子に対する成長円錐の感受性を規定する。また、成長円錐には同一の軸索ガイダンス因子に対する反応性を場所や時期に応じて切り替える機構が備わっている<ref><pubmed> 10395576</pubmed></ref>。 以下に代表的な軸索ガイダンスについて概説する。 | 軸索ガイダンス因子は発生過程の組織内に領域特異的に存在することで成長円錐に空間情報を提供し、成長円錐を正しい標的細胞へと誘導する分子として定義される。生体内における軸索ガイダンス因子は多種多様であるが、大きく4つの作用様式に分類される。細胞外基質や細胞膜に発現し接触を介して近距離に作用する接触因子と、分泌性で濃度勾配によって長距離に作用する拡散性因子、そしてそのそれぞれに対して誘引因子と反発因子が存在する。生体内ではこれら4種類の軸索ガイダンス因子が協調的に働き軸索を正しい標的へ導くと考えられている。成長円錐には個々の軸索ガイダンス因子に対する特異的な受容体ファミリーが存在しており<ref><pubmed> 12471249</pubmed></ref>、受容体の形質膜への発現は軸索ガイダンス因子に対する成長円錐の感受性を規定する。また、成長円錐には同一の軸索ガイダンス因子に対する反応性を場所や時期に応じて切り替える機構が備わっている<ref><pubmed> 10395576</pubmed></ref>。 以下に代表的な軸索ガイダンスについて概説する。 | ||
==== ネトリン | ==== ネトリン ==== | ||
[[ネトリン]](netrin)は[[分泌性タンパク質]]で、発生期の[[脊髄]]において[[底板]]から分泌され[[交連神経]]軸索を誘引して[[運動神経]]軸索を反発する典型的な両方向性軸索ガイダンス因子として働く<ref><pubmed> 8978605</pubmed></ref><ref><pubmed> 15960985</pubmed></ref>。ネトリン受容体としては[[DCC]]と[[UNC-5]]が同定されている。ネトリン-1に対する成長円錐の反応性はこれら2種類の受容体の発現パターンに依存しており、DCCのみでは誘引、DCCとUNC-5が共発現し形質膜上で受容体ヘテロダイマーを形成すると反発を呈する<ref><pubmed> 10399920</pubmed></ref>。 | |||
==== セマフォリン | ==== セマフォリン ==== | ||
[[セマフォリン]](semaphorin)ファミリーは代表的な反発性軸索ガイダンス因子で、分泌型の他に膜貫通型、[[GPIアンカー]]膜結合型など8つのグループに分類される<ref><pubmed> 10932095</pubmed></ref>。分泌型である[[Sema3A]]は生体内で脊髄神経の走行領域を取り囲むように発現しており、Sema3Aノックアウトマウスでは脊髄神経軸索が脱束化しその走行と投射パターンが大幅に乱れる<ref><pubmed> 9331345 </pubmed></ref>。クラス3セマフォリンに対する受容体としては、[[ニューロピリン]](neuropilin)と[[プレキシン]](plexin)が同定されている。ニューロピリンの細胞内領域は短く、ニューロピリン単独ではセマフォリンによる細胞内シグナル経路を活性化できないが、プレキシンと複合体を形成しプレキシンの細胞内領域において別の分子と相互作用することにより、セマフォリンのシグナルを細胞内シグナルへと伝達する<ref><pubmed> 10520994 </pubmed></ref>。 | [[セマフォリン]](semaphorin)ファミリーは代表的な反発性軸索ガイダンス因子で、分泌型の他に膜貫通型、[[GPIアンカー]]膜結合型など8つのグループに分類される<ref><pubmed> 10932095</pubmed></ref>。分泌型である[[Sema3A]]は生体内で脊髄神経の走行領域を取り囲むように発現しており、Sema3Aノックアウトマウスでは脊髄神経軸索が脱束化しその走行と投射パターンが大幅に乱れる<ref><pubmed> 9331345 </pubmed></ref>。クラス3セマフォリンに対する受容体としては、[[ニューロピリン]](neuropilin)と[[プレキシン]](plexin)が同定されている。ニューロピリンの細胞内領域は短く、ニューロピリン単独ではセマフォリンによる細胞内シグナル経路を活性化できないが、プレキシンと複合体を形成しプレキシンの細胞内領域において別の分子と相互作用することにより、セマフォリンのシグナルを細胞内シグナルへと伝達する<ref><pubmed> 10520994 </pubmed></ref>。 | ||
| 79行目: | 69行目: | ||
[[受容体型チロシンキナーゼ]][[Eph]]のリガンドである[[エフリン]](Ephrin)は、GPIアンカーによる膜結合型の[[エフリンA]](エフリンA1-A5)と、細胞膜貫通型である[[エフリンB]](エフリンB1-B3)に分類され<ref><pubmed> 9530499 </pubmed></ref>、いずれも接触型のガイダンス因子として機能する。受容体であるEphファミリーは[[EphA]]と[[EphB]]に大別され、大まかにはエフリンAグループはEphAグループと、エフリンBグループはEphBグループと結合する。エフリンとEphは発生過程の様々な領域、特に網膜-視蓋投射系において、神経回路形成に重要な役割を担っている。 | [[受容体型チロシンキナーゼ]][[Eph]]のリガンドである[[エフリン]](Ephrin)は、GPIアンカーによる膜結合型の[[エフリンA]](エフリンA1-A5)と、細胞膜貫通型である[[エフリンB]](エフリンB1-B3)に分類され<ref><pubmed> 9530499 </pubmed></ref>、いずれも接触型のガイダンス因子として機能する。受容体であるEphファミリーは[[EphA]]と[[EphB]]に大別され、大まかにはエフリンAグループはEphAグループと、エフリンBグループはEphBグループと結合する。エフリンとEphは発生過程の様々な領域、特に網膜-視蓋投射系において、神経回路形成に重要な役割を担っている。 | ||
==== モルフォゲン | ==== モルフォゲン ==== | ||
初期発生における未分化な細胞に対しその発生運命を決定する因子を[[モルフォゲン]](morphogen)といい、代表的なものとして[[ヘジホッッグ]](hedgehog)、[[Wnt]]、[[TGF-β]]、[[ | 初期発生における未分化な細胞に対しその発生運命を決定する因子を[[モルフォゲン]](morphogen)といい、代表的なものとして[[ヘジホッッグ]](hedgehog)、[[Wnt]]、[[TGF-β]]、[[BMP]]などの分泌性タンパク質が知られている。近年、モルフォゲンが軸索ガイダンス因子として機能することが報告されている。例えば、[[脊髄蓋板]]から分泌され交連神経等の[[脊髄背側介在神経細胞]]への運命決定を司るBMPは、分化した交連神経の軸索に対しては反発性ガイダンス因子として機能する<ref><pubmed> 10677032 </pubmed></ref>。また、底板から分泌されるソニックヘッジホッグ(sonic hedgehog)は、ネトリン-1とともに交連軸索に対する誘因性ガイダンス因子としてはたらく<ref><pubmed> 12679031 </pubmed></ref>。 | ||
==== 神経栄養因子 | ==== 神経栄養因子 ==== | ||
[[NGF]]、[[BDNF]]などの[[神経栄養因子]]は、標的細胞から分泌され神経細胞の分化、軸索伸長、生存維持等の生理活性を持つ<ref><pubmed> 11520916</pubmed></ref>。発生期の生体内において、神経栄養因子が明瞭な濃度勾配を形成しているという決定的な証拠はないが、NGFは培養条件下で成長円錐を誘引する作用を持つ因子として最初に報告された<ref><pubmed> 493992 </pubmed></ref>。また、発生期の組織内に神経栄養因子に浸したビーズを置くと周辺の軸索がビーズに向かって伸長することも報告されている<ref><pubmed>11135642 </pubmed></ref>。 | [[NGF]]、[[BDNF]]などの[[神経栄養因子]]は、標的細胞から分泌され神経細胞の分化、軸索伸長、生存維持等の生理活性を持つ<ref><pubmed> 11520916</pubmed></ref>。発生期の生体内において、神経栄養因子が明瞭な濃度勾配を形成しているという決定的な証拠はないが、NGFは培養条件下で成長円錐を誘引する作用を持つ因子として最初に報告された<ref><pubmed> 493992 </pubmed></ref>。また、発生期の組織内に神経栄養因子に浸したビーズを置くと周辺の軸索がビーズに向かって伸長することも報告されている<ref><pubmed>11135642 </pubmed></ref>。 | ||
=== | === 成長円錐の旋回運動を制御する細胞内シグナル経路 === | ||
成長円錐の運動性は細胞骨格、接着分子とそのリサイクリングにより規定されるが、成長円錐の前進速度に空間的な非対称性が生じれば、成長円錐は全体として旋回運動を呈することになる。実際に、軸索ガイダンス因子が制御する成長円錐の旋回運動にも[[Rho]]ファミリー[[低分子量Gタンパク質]]、[[ADF]]/[[コフィリン]]、[[Ena]]/[[Vasp]]、[[APC]]などの細胞骨格制御分子<ref><pubmed>19373241</pubmed></ref> 、[[FAK]]、[[Src]][[チロシンリン酸化|チロシンキナーゼ]]による細胞接着の制御<ref><pubmed>21940449</pubmed></ref> が関与することが明らかにされている。 | |||
上述したとおり、成長円錐は軸索ガイダンス因子に対する応答性(反応の有無、誘引- | 上述したとおり、成長円錐は軸索ガイダンス因子に対する応答性(反応の有無、誘引-反発の方向)を場所や時期により変化させる。また、成長円錐は生体内で様々な軸索ガイダンス因子のシグナルを受容しており、成長円錐の旋回方向は多様な細胞内シグナル伝達経路の複雑なクロストークの結果決定されると考えられる。近年、成長円錐の旋回方向(誘引 or 反発)を決定する分子メカニズムの理解が急速に進んでおり、以下に旋回方向を規定する因子について概説する。 | ||
==== セカンドメッセンジャーによる制御 ==== | ==== セカンドメッセンジャーによる制御 ==== | ||
===== 環状ヌクレオチド | ===== 環状ヌクレオチド ===== | ||
[[環状ヌクレオチド]]である[[CAMP|cAMP]]および[[CGMP|cGMP]] | [[環状ヌクレオチド]]である[[CAMP|cAMP]]および[[CGMP|cGMP]]シグナルは、同一軸索ガイダンス因子に対する成長円錐の旋回方向を規定するものとして報告が多い。 例えば、ネトリン-1及びBDNFの濃度勾配に対する成長円錐の誘引は、cAMPのアンタゴニストである[[Rp-cAMPs]]の投与によって反発へと逆転する<ref><pubmed>9427246</pubmed></ref><ref><pubmed>9230436</pubmed></ref>。また、[[軸索再生]]阻害因子として知られ軸索反発を誘導する[[MAG]]の濃度勾配に対する反発は、cAMPアゴニストである[[Sp-cAMPs]]の投与により誘引へと逆転する<ref><pubmed>9727979</pubmed></ref>。さらに、cGMPのアゴニストである[[8-Br-cGMP]]の投与によりネトリン-1による誘引が反発へと逆転する報告もあり<ref><pubmed>12827203</pubmed></ref>、多くの軸索ガイダンス因子に共通するメカニズムとしてcAMPシグナルが優位だと誘引性、cGMPシグナルが優位だと反発性の旋回運動を誘導すると考えられている。 cAMP/cGMPの下流では主に[[プロテインキナーゼA]](PKA)/[[プロテインキナーゼG]](PKG)が機能すると考えられており、これら2種類のリン酸化酵素の標的分子などの違いにより成長円錐の誘引と反発という正反対の応答が誘導されると考えられている。 | ||
===== 細胞内Ca<sup>2+</sup>シグナル ===== | ===== 細胞内Ca<sup>2+</sup>シグナル ===== | ||
[[ケージドカルシウム光解離法]]を用いて、成長円錐内に局所的なCa<sup>2+</sup> | [[ケージドカルシウム光解離法]]を用いて、成長円錐内に局所的なCa<sup>2+</sup>シグナルを励起すると、成長円錐の旋回運動が誘導される<ref><pubmed>10638759</pubmed></ref>。また誘引性、反発性を問わず、様々な軸索ガイダンス因子の濃度勾配に遭遇した成長円錐内で非対称なCa<sup>2+</sup>濃度上昇が観察されること<ref><pubmed>21386859</pubmed></ref>、成長円錐内のCa<sup>2+</sup>シグナルを遮断すると軸索ガイダンス因子に対する誘引、反発応答の両方が消失することから、局所的なCa<sup>2+</sup>シグナルは成長円錐の旋回運動制御の中心的役割を担っていると考えられている。 | ||
Ca<sup>2+</sup>シグナルが誘引-反発の両方を誘導するメカニズムとして、現在2つのモデルが提唱されている。 | Ca<sup>2+</sup>シグナルが誘引-反発の両方を誘導するメカニズムとして、現在2つのモデルが提唱されている。 | ||
| 107行目: | 97行目: | ||
1つは成長円錐内で上昇するCa<sup>2+</sup>の絶対量の差が誘引-反発を決定するというモデルで<ref><pubmed>15603734 </pubmed></ref>、低Ca<sup>2+</sup>流入ではCa<sup>2+</sup>に対するアフィニティーの高い分子のみが活性化され反発性応答が、高Ca<sup>2+</sup>流入はCa<sup>2+</sup>に対するアフィニティーの低い分子も活性化され誘引性応答が誘導するとされている。 | 1つは成長円錐内で上昇するCa<sup>2+</sup>の絶対量の差が誘引-反発を決定するというモデルで<ref><pubmed>15603734 </pubmed></ref>、低Ca<sup>2+</sup>流入ではCa<sup>2+</sup>に対するアフィニティーの高い分子のみが活性化され反発性応答が、高Ca<sup>2+</sup>流入はCa<sup>2+</sup>に対するアフィニティーの低い分子も活性化され誘引性応答が誘導するとされている。 | ||
2つ目は、旋回方向は流入するCa<sup>2+</sup>チャネルの種類に依存するというモデルで、小胞体ストアからのCa<sup>2+</sup>放出を伴うと誘引性、それ以外のCa<sup>2+</sup>シグナルは反発性応答が誘導されると考えられている<ref><pubmed>16172206</pubmed></ref>。このモデルでは、各種Ca<sup>2+</sup>チャネルの近傍に存在するCa<sup>2+</sup>感受性分子の違いが成長円錐の旋回方向を決定すると予想されている。 | |||
旋回運動を誘導するCa<sup>2+</sup>シグナルの下流因子として、誘引性シグナルには[[カルモジュリン]](calmodulin)依存性[[リン酸化酵素]]である[[CaMキナーゼⅡ]](CaMKⅡ)が、反発性シグナルには[[脱リン酸化酵素]]である[[カルシニューリン]](calcineurin)がそれぞれ中心的な役割を担っていると考えられている<ref><pubmed>15363394</pubmed></ref>。 | |||
==== 膜トラフィッキング ==== | ==== 膜トラフィッキング ==== | ||
[[Image:旋回方向決定.png|thumb|450px| | [[Image:旋回方向決定.png|thumb|450px|<b>図3.成長円錐の旋回方向を規定する要因の例</b>]] | ||
近年、エキソサイトーシスやエンドサイトーシスといった細胞膜トラフィッキングも軸索ガイダンス因子が誘導する成長円錐の旋回運動に関与することが報告されている<ref><pubmed>21386859</pubmed></ref>。これまでの見解として、誘引性ガイダンス因子ではエキソサイトーシスが、反発性ガイダンス因子ではエンドサイトーシスがそれぞれ非対称に成長円錐内で活性化され、成長円錐は旋回運動を呈すると考えられている。また、人為的にエンドサイトーシスやエキソサイトーシスを成長円錐の片側で促進あるいは阻害すると成長円錐の旋回運動が誘導されるという報告もあり<ref><pubmed>20471350</pubmed></ref>、軸索ガイダンス因子は成長円錐内のエキソサイトーシス/エンドサイトーシスの空間的なバランスを制御することで、成長円錐の旋回運動の方向性を規定すると考えられる(図3)。 | |||
==== 局所タンパク質合成と分解 ==== | ==== 局所タンパク質合成と分解 ==== | ||
成長円錐には小胞体や[[ | 成長円錐には小胞体や[[MRNA]]、[[リボソーム]]、[[翻訳制御因子]]等タンパク質の[[wikipedia:ja:翻訳 (生物学)|翻訳]]合成に必要な分子機構が備わっており、近年、成長円錐内でのタンパク質の局所翻訳が軸索ガイダンス因子による旋回運動の制御に重要であることが報告されている。 | ||
例えば、細胞体から切り離した軸索の成長円錐はネトリン-1の濃度勾配に対し誘引されるが、この誘引応答はタンパク質合成阻害剤により消失する<ref><pubmed> 11754834</pubmed></ref> | 例えば、細胞体から切り離した軸索の成長円錐はネトリン-1の濃度勾配に対し誘引されるが、この誘引応答はタンパク質合成阻害剤により消失する<ref><pubmed> 11754834</pubmed></ref>。同様に、BDNF、Sema3A、Slit2など、他の軸索ガイダンス因子ついても成長円錐の旋回運動の誘導に局所タンパク質合成が必要であることが明らかにされている<ref><pubmed> 21530230</pubmed></ref>。 | ||
軸索ガイダンス因子による局所翻訳の制御機構は不明な点も多いが、少しずつ知見が得られている。例えば、ネトリン-1非存在下では受容体であるDCCとリボソームが結合しタンパク質合成を抑制しているが、ネトリン-1がDCCに結合するとリボソームがDCCから解離し抑制が外れタンパク質合成が起きることが報告されている<ref><pubmed>20434207</pubmed></ref>。 | 軸索ガイダンス因子による局所翻訳の制御機構は不明な点も多いが、少しずつ知見が得られている。例えば、ネトリン-1非存在下では受容体であるDCCとリボソームが結合しタンパク質合成を抑制しているが、ネトリン-1がDCCに結合するとリボソームがDCCから解離し抑制が外れタンパク質合成が起きることが報告されている<ref><pubmed>20434207</pubmed></ref>。 また、旋回運動を誘導するCa<sup>2+</sup>シグナルに応じて空間的に非対称なβ-[[アクチン]]のmRNAの翻訳が誘発されることも報告されており<ref><pubmed>16980965</pubmed></ref>、Ca<sup>2+</sup>シグナルの下流でタンパク質の翻訳合成を制御する機構の存在も示唆されている。 | ||
また、最近になり、[[マイクロRNA]] | また、最近になり、[[マイクロRNA]](miRNA)による局所タンパク質翻訳制御が成長円錐の旋回運動に関与することも報告されている<ref><pubmed>22051374 </pubmed></ref>。 | ||
一方、成長円錐において[[ユビキチン]]-[[プロテアソーム]] | 一方、成長円錐において[[ユビキチン]]-[[プロテアソーム]]系のタンパク質分解システムも機能しており、これも旋回運動に関与すると考えらており、今後軸索ガイダンスシグナルにより分解が促進されるタンパク質群の同定や、分解系の活性化機構の解明が待たれる。 <br> | ||
== 関連項目 == | == 関連項目 == | ||
| 136行目: | 126行目: | ||
<references /> | <references /> | ||
<br>(執筆者:森 達也、上口裕之 担当編集委員:林 康紀) | |||
2012年4月23日 (月) 10:46時点における版
英語名: Growth cone 独:Wachstumskegel 仏:cône axonique、cône d'émergence de l'axone
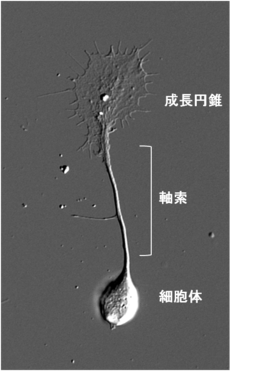
成長円錐は伸長中の神経突起の先端部に見られるアメーバ状の構造物である(図1)。19世紀にスペインの神経科学者Ramón y Cajalにより、固定染色した神経組織において神経軸索先端部に円錐状の構造が発見され、growth cone=成長円錐と名付けられた。2次元基質上で培養した場合は薄く扁平な形態をとり、多くが伸長中の神経軸索の先端に存在するが樹状突起の先端にも存在する。また、PC12細胞やN1E-115細胞のような株化細胞から伸びる神経突起様構造物の先端にも見られる。軸索の成長円錐の場合、標的神経細胞の樹状突起や組織へと到達した後は形態変化を起こしシナプス前部となる。成長円錐は極めて高い運動性を示し、細胞骨格や接着分子、膜輸送経路の制御を通じて前方へと移動し、神経突起を牽引することで伸長させる。また、成長円錐の形質膜には軸索ガイダンス因子に対する受容体が多数発現しており、軸索の成長円錐は細胞外環境に存在する軸索ガイダンス因子に応じてその運動性と進行方向を変化させ、神経軸索を正しい標的細胞へと投射させる。
構造
成長円錐は2次元基質上では扇状に広がった手のような構造で、その形態から周辺部(peripheral domain)と中心部(central domain)の2つの部分に大別される(図2、上)。また、周辺部と中心部の境界部分を移行帯(transition zone)として分類することもある。
周辺部
周辺部は扁平の構造で、成長円錐中央から放射状に伸びた細い指のような糸状仮足(filopodia)の間を、水掻きのような薄いシート状の葉状仮足(lamellipodia)が埋めている(図2)。成長円錐の周辺部はアクチン(actin)繊維に保持されているが、糸状仮足と葉状仮足ではアクチン繊維の形状が異なる。糸状仮足内のアクチン繊維は比較的長い束状の直線的な形状であるのに対し、葉状仮足内では短いアクチン繊維が枝分かれした網目状の構造をしている。また、周辺部には比較的動的な微小管(microtubule)末端も見られる[1] 。
中心部
中心部は軸索からつながった成長円錐中央部の比較的厚みのある部分で、神経突起から伸びている安定な微小管が主な構成成分である(図2)。中心部は神経突起内の微小管束の末端部分に相当し、中心部におけるチューブリンの付加は神経突起の伸長を、脱重合は神経突起の退縮を引き起こす。中心部には比較的安定なアクチン繊維も存在し[2]、細胞骨格の他にもミトコンドリアや小胞体などの細胞小器官、膜小胞なども多く含まれる 。 軸索内の微小管はMicrotubule-associated proteins(MAPs)により束ねられているが、中心部では先端部がほどけ、一部の微小管は周辺部に向かって放射状に広がっている。
周辺部におけるアクチン繊維と微小管の役割
周辺部のアクチン繊維は糸状仮足、葉状仮足ともプラス端を外側に向けて配向している。先端部での単量体アクチンの重合によるアクチン繊維の伸長は、糸状仮足や葉状仮足を周辺部に向けて拡大させ、成長円錐の細胞膜は前方に推し進められる。すなわち、周辺部におけるアクチン繊維の重合-脱重合の制御は成長円錐の運動性を規定する大きな要因の一つである。
周辺部の微小管もアクチン線維と同様にプラス端を外側に向けて配向しており、周辺部への接着分子や膜成分の輸送をガイドする足場として機能する。この微小管依存的な小胞輸送経路は成長円錐の旋回運動に重要で、周辺部における微小管の空間的な制御が成長円錐の旋回方向を規定する要因の一つと考えられている。
さらに、周辺部においてアクチン繊維と微小管は両結合性分子を介して相互作用しており、このアクチン繊維-微小管の相互作用も成長円錐の運動性に大きく関与する。両結合性分子としてShot、Dpod-1等が同定されており、これらの分子をを欠く神経細胞では軸索の伸長や走行に異常を示す[3][4] 。
成長円錐前進運動の分子メカニズム
成長円錐は①周辺部先端での糸状仮足の形成・伸長、②糸状仮足間への葉状仮足の流れ込みによる周辺部の拡大、③後方からの中心部の侵入、という3つの過程を繰り返すことで前方へと移動していく。この成長円錐の前方移動の分子メカニズムとして、クラッチ仮説が有力なものとして提唱されている[5]。クラッチ仮説ではアクチン繊維の後方移動と成長円錐形質膜上に発現する接着分子、接着分子とアクチン繊維をつなぐクラッチ分子、接着分子のリサイクリングが協調して働き、成長円錐が前方に移動すると説明される。 (①ー③の過程と、クラッチ仮説を図、または動画で御示し頂く訳にはいかないでしょうか)
アクチン繊維の後方移動
周辺部に存在するアクチン繊維は、プラス端を成長円錐先端に、マイナス端を中心部側に向けて規則正しく配置されており、単量体アクチンのアクチン繊維への付加は主に先端部で、アクチン繊維の解離は主に中心部側で起こる。同時にアクチン繊維全体はモータータンパク質であるミオシン(myosin)Ⅰb[6]やミオシンⅡ[7]の作用により一定の速度(約5 μm/min)で先端部から中心部へと移動している。このアクチン繊維の後方移動を動力源として成長円錐は前進運動すると考えられる。
接着分子
成長円錐の形質膜には免疫グロブリン(immunogloblin)ファミリー、カドヘリン(cadherin)ファミリー、インテグリン(integrin)ファミリーなどの接着分子が発現しており、細胞外基質、または隣接する細胞との接着を媒介している。多くの場合、細胞外領域での接着分子のリガンド結合および細胞表面での接着分子のクラスタリングは細胞内領域における接着分子とアクチン繊維間の結合を誘導する。このような接着分子-アクチン繊維間の結合は、接着分子の接着性を増強するとともに、アクチン繊維の後方移動により発生した牽引力を細胞外周囲環境に伝達し、その結果として成長円錐が前方に推進されると考えられている。
クラッチ分子
成長円錐の前方移動の仕組みを自動車の走行に例えると、エンジンの役割を果たすのがアクチン繊維の動態(重合・脱重合・後方移動)であり、タイヤの役割を果たすのが周辺環境と接着している接着分子である。このエンジンとタイヤをつなぐ役割を果たすものがクラッチ分子と呼ばれ、アクチン繊維の動態を、接着分子を介した成長円錐の推進力へと変換する役割を担っている。成長円錐内においてクラッチ分子の実態および制御機構は不明な点が多いが、アクチン繊維とL1間のクラッチ分子としてシューティン(shootin)が同定され[8]、アンキリン(ankyrin)やカテニン(catenin)といったリンカー分子[9]、エズリン(ezrin)[10]などもクラッチ分子として機能すると考えられている。
接着分子のリサイクリング
アクチン繊維と結合した接着分子は、アクチン繊維の後方移動に伴って成長円錐中心部へと運ばれてしまう。成長円錐ではその前方移動を恒常的に維持するため、後方へ移動した接着分子を周辺環境から脱着し、再び成長円錐先端部へと輸送し再利用する機構が存在すると考えられている。例えば、アクチン繊維の後方移動により中心部に到達したL1は、クラスリン(clathrin)依存的エンドサイトーシスによって膜小胞に取り込まれた後、微小管のガイドによって細胞質内を成長円錐先端部まで輸送され、形質膜に再挿入される[11][12]。このように接着分子は、①成長円錐先端部での基質との接着、②アクチン繊維の後方移動に伴う成長円錐中心部への移動、③基質からの脱着と成長円錐内への取り込み、④成長円錐先端部への輸送、⑤先端部での形質膜への再挿入、という過程でリサイクルされており、成長円錐の恒常的な前進運動の分子基盤となっていると考えられている。(これも図示して頂けないでしょうか)
成長円錐と軸索ガイダンス
神経回路の形成過程において、成長円錐は細胞周辺に存在する軸索ガイダンス因子を検出するアンテナとして機能する。すなわち、成長円錐は軸索ガイダンス因子の空間情報を軸索の伸長方向の制御へと変換する上で極めて重要な構造である。
軸索ガイダンス因子
軸索ガイダンス因子は発生過程の組織内に領域特異的に存在することで成長円錐に空間情報を提供し、成長円錐を正しい標的細胞へと誘導する分子として定義される。生体内における軸索ガイダンス因子は多種多様であるが、大きく4つの作用様式に分類される。細胞外基質や細胞膜に発現し接触を介して近距離に作用する接触因子と、分泌性で濃度勾配によって長距離に作用する拡散性因子、そしてそのそれぞれに対して誘引因子と反発因子が存在する。生体内ではこれら4種類の軸索ガイダンス因子が協調的に働き軸索を正しい標的へ導くと考えられている。成長円錐には個々の軸索ガイダンス因子に対する特異的な受容体ファミリーが存在しており[13]、受容体の形質膜への発現は軸索ガイダンス因子に対する成長円錐の感受性を規定する。また、成長円錐には同一の軸索ガイダンス因子に対する反応性を場所や時期に応じて切り替える機構が備わっている[14]。 以下に代表的な軸索ガイダンスについて概説する。
ネトリン
ネトリン(netrin)は分泌性タンパク質で、発生期の脊髄において底板から分泌され交連神経軸索を誘引して運動神経軸索を反発する典型的な両方向性軸索ガイダンス因子として働く[15][16]。ネトリン受容体としてはDCCとUNC-5が同定されている。ネトリン-1に対する成長円錐の反応性はこれら2種類の受容体の発現パターンに依存しており、DCCのみでは誘引、DCCとUNC-5が共発現し形質膜上で受容体ヘテロダイマーを形成すると反発を呈する[17]。
セマフォリン
セマフォリン(semaphorin)ファミリーは代表的な反発性軸索ガイダンス因子で、分泌型の他に膜貫通型、GPIアンカー膜結合型など8つのグループに分類される[18]。分泌型であるSema3Aは生体内で脊髄神経の走行領域を取り囲むように発現しており、Sema3Aノックアウトマウスでは脊髄神経軸索が脱束化しその走行と投射パターンが大幅に乱れる[19]。クラス3セマフォリンに対する受容体としては、ニューロピリン(neuropilin)とプレキシン(plexin)が同定されている。ニューロピリンの細胞内領域は短く、ニューロピリン単独ではセマフォリンによる細胞内シグナル経路を活性化できないが、プレキシンと複合体を形成しプレキシンの細胞内領域において別の分子と相互作用することにより、セマフォリンのシグナルを細胞内シグナルへと伝達する[20]。
Slit
Slitは脊椎動物の脊髄において底板に発現する分泌型の反発性軸索ガイダンス因子である。Slitの受容体であるRoboの遺伝子に変異を持つショウジョウバエ("Roundabout")では、軸索の正中交差が過剰に起きる表現型を示す[21]。Roundaboutとは別に、正中交差が全く起きなくなる"Commissureless"(comm)変異体も同定されており、CommはRoboの形質膜発現を抑制することで、交連軸索が一度だけ正中を交差する経路選択に中心的な役割を果たしていると考えられている [22]。
エフリン
受容体型チロシンキナーゼEphのリガンドであるエフリン(Ephrin)は、GPIアンカーによる膜結合型のエフリンA(エフリンA1-A5)と、細胞膜貫通型であるエフリンB(エフリンB1-B3)に分類され[23]、いずれも接触型のガイダンス因子として機能する。受容体であるEphファミリーはEphAとEphBに大別され、大まかにはエフリンAグループはEphAグループと、エフリンBグループはEphBグループと結合する。エフリンとEphは発生過程の様々な領域、特に網膜-視蓋投射系において、神経回路形成に重要な役割を担っている。
モルフォゲン
初期発生における未分化な細胞に対しその発生運命を決定する因子をモルフォゲン(morphogen)といい、代表的なものとしてヘジホッッグ(hedgehog)、Wnt、TGF-β、BMPなどの分泌性タンパク質が知られている。近年、モルフォゲンが軸索ガイダンス因子として機能することが報告されている。例えば、脊髄蓋板から分泌され交連神経等の脊髄背側介在神経細胞への運命決定を司るBMPは、分化した交連神経の軸索に対しては反発性ガイダンス因子として機能する[24]。また、底板から分泌されるソニックヘッジホッグ(sonic hedgehog)は、ネトリン-1とともに交連軸索に対する誘因性ガイダンス因子としてはたらく[25]。
神経栄養因子
NGF、BDNFなどの神経栄養因子は、標的細胞から分泌され神経細胞の分化、軸索伸長、生存維持等の生理活性を持つ[26]。発生期の生体内において、神経栄養因子が明瞭な濃度勾配を形成しているという決定的な証拠はないが、NGFは培養条件下で成長円錐を誘引する作用を持つ因子として最初に報告された[27]。また、発生期の組織内に神経栄養因子に浸したビーズを置くと周辺の軸索がビーズに向かって伸長することも報告されている[28]。
成長円錐の旋回運動を制御する細胞内シグナル経路
成長円錐の運動性は細胞骨格、接着分子とそのリサイクリングにより規定されるが、成長円錐の前進速度に空間的な非対称性が生じれば、成長円錐は全体として旋回運動を呈することになる。実際に、軸索ガイダンス因子が制御する成長円錐の旋回運動にもRhoファミリー低分子量Gタンパク質、ADF/コフィリン、Ena/Vasp、APCなどの細胞骨格制御分子[29] 、FAK、Srcチロシンキナーゼによる細胞接着の制御[30] が関与することが明らかにされている。
上述したとおり、成長円錐は軸索ガイダンス因子に対する応答性(反応の有無、誘引-反発の方向)を場所や時期により変化させる。また、成長円錐は生体内で様々な軸索ガイダンス因子のシグナルを受容しており、成長円錐の旋回方向は多様な細胞内シグナル伝達経路の複雑なクロストークの結果決定されると考えられる。近年、成長円錐の旋回方向(誘引 or 反発)を決定する分子メカニズムの理解が急速に進んでおり、以下に旋回方向を規定する因子について概説する。
セカンドメッセンジャーによる制御
環状ヌクレオチド
環状ヌクレオチドであるcAMPおよびcGMPシグナルは、同一軸索ガイダンス因子に対する成長円錐の旋回方向を規定するものとして報告が多い。 例えば、ネトリン-1及びBDNFの濃度勾配に対する成長円錐の誘引は、cAMPのアンタゴニストであるRp-cAMPsの投与によって反発へと逆転する[31][32]。また、軸索再生阻害因子として知られ軸索反発を誘導するMAGの濃度勾配に対する反発は、cAMPアゴニストであるSp-cAMPsの投与により誘引へと逆転する[33]。さらに、cGMPのアゴニストである8-Br-cGMPの投与によりネトリン-1による誘引が反発へと逆転する報告もあり[34]、多くの軸索ガイダンス因子に共通するメカニズムとしてcAMPシグナルが優位だと誘引性、cGMPシグナルが優位だと反発性の旋回運動を誘導すると考えられている。 cAMP/cGMPの下流では主にプロテインキナーゼA(PKA)/プロテインキナーゼG(PKG)が機能すると考えられており、これら2種類のリン酸化酵素の標的分子などの違いにより成長円錐の誘引と反発という正反対の応答が誘導されると考えられている。
細胞内Ca2+シグナル
ケージドカルシウム光解離法を用いて、成長円錐内に局所的なCa2+シグナルを励起すると、成長円錐の旋回運動が誘導される[35]。また誘引性、反発性を問わず、様々な軸索ガイダンス因子の濃度勾配に遭遇した成長円錐内で非対称なCa2+濃度上昇が観察されること[36]、成長円錐内のCa2+シグナルを遮断すると軸索ガイダンス因子に対する誘引、反発応答の両方が消失することから、局所的なCa2+シグナルは成長円錐の旋回運動制御の中心的役割を担っていると考えられている。
Ca2+シグナルが誘引-反発の両方を誘導するメカニズムとして、現在2つのモデルが提唱されている。
1つは成長円錐内で上昇するCa2+の絶対量の差が誘引-反発を決定するというモデルで[37]、低Ca2+流入ではCa2+に対するアフィニティーの高い分子のみが活性化され反発性応答が、高Ca2+流入はCa2+に対するアフィニティーの低い分子も活性化され誘引性応答が誘導するとされている。
2つ目は、旋回方向は流入するCa2+チャネルの種類に依存するというモデルで、小胞体ストアからのCa2+放出を伴うと誘引性、それ以外のCa2+シグナルは反発性応答が誘導されると考えられている[38]。このモデルでは、各種Ca2+チャネルの近傍に存在するCa2+感受性分子の違いが成長円錐の旋回方向を決定すると予想されている。
旋回運動を誘導するCa2+シグナルの下流因子として、誘引性シグナルにはカルモジュリン(calmodulin)依存性リン酸化酵素であるCaMキナーゼⅡ(CaMKⅡ)が、反発性シグナルには脱リン酸化酵素であるカルシニューリン(calcineurin)がそれぞれ中心的な役割を担っていると考えられている[39]。
膜トラフィッキング

近年、エキソサイトーシスやエンドサイトーシスといった細胞膜トラフィッキングも軸索ガイダンス因子が誘導する成長円錐の旋回運動に関与することが報告されている[40]。これまでの見解として、誘引性ガイダンス因子ではエキソサイトーシスが、反発性ガイダンス因子ではエンドサイトーシスがそれぞれ非対称に成長円錐内で活性化され、成長円錐は旋回運動を呈すると考えられている。また、人為的にエンドサイトーシスやエキソサイトーシスを成長円錐の片側で促進あるいは阻害すると成長円錐の旋回運動が誘導されるという報告もあり[41]、軸索ガイダンス因子は成長円錐内のエキソサイトーシス/エンドサイトーシスの空間的なバランスを制御することで、成長円錐の旋回運動の方向性を規定すると考えられる(図3)。
局所タンパク質合成と分解
成長円錐には小胞体やMRNA、リボソーム、翻訳制御因子等タンパク質の翻訳合成に必要な分子機構が備わっており、近年、成長円錐内でのタンパク質の局所翻訳が軸索ガイダンス因子による旋回運動の制御に重要であることが報告されている。
例えば、細胞体から切り離した軸索の成長円錐はネトリン-1の濃度勾配に対し誘引されるが、この誘引応答はタンパク質合成阻害剤により消失する[42]。同様に、BDNF、Sema3A、Slit2など、他の軸索ガイダンス因子ついても成長円錐の旋回運動の誘導に局所タンパク質合成が必要であることが明らかにされている[43]。
軸索ガイダンス因子による局所翻訳の制御機構は不明な点も多いが、少しずつ知見が得られている。例えば、ネトリン-1非存在下では受容体であるDCCとリボソームが結合しタンパク質合成を抑制しているが、ネトリン-1がDCCに結合するとリボソームがDCCから解離し抑制が外れタンパク質合成が起きることが報告されている[44]。 また、旋回運動を誘導するCa2+シグナルに応じて空間的に非対称なβ-アクチンのmRNAの翻訳が誘発されることも報告されており[45]、Ca2+シグナルの下流でタンパク質の翻訳合成を制御する機構の存在も示唆されている。
また、最近になり、マイクロRNA(miRNA)による局所タンパク質翻訳制御が成長円錐の旋回運動に関与することも報告されている[46]。
一方、成長円錐においてユビキチン-プロテアソーム系のタンパク質分解システムも機能しており、これも旋回運動に関与すると考えらており、今後軸索ガイダンスシグナルにより分解が促進されるタンパク質群の同定や、分解系の活性化機構の解明が待たれる。
関連項目
引用文献
- ↑
Schaefer, A.W., Kabir, N., & Forscher, P. (2002).
Filopodia and actin arcs guide the assembly and transport of two populations of microtubules with unique dynamic parameters in neuronal growth cones. The Journal of cell biology, 158(1), 139-52. [PubMed:12105186] [PMC] [WorldCat] [DOI] - ↑
Zhang, X.F., Schaefer, A.W., Burnette, D.T., Schoonderwoert, V.T., & Forscher, P. (2003).
Rho-dependent contractile responses in the neuronal growth cone are independent of classical peripheral retrograde actin flow. Neuron, 40(5), 931-44. [PubMed:14659092] [WorldCat] [DOI] - ↑
Lee, S., & Kolodziej, P.A. (2002).
Short Stop provides an essential link between F-actin and microtubules during axon extension. Development (Cambridge, England), 129(5), 1195-204. [PubMed:11874915] [WorldCat] - ↑
Rothenberg, M.E., Rogers, S.L., Vale, R.D., Jan, L.Y., & Jan, Y.N. (2003).
Drosophila pod-1 crosslinks both actin and microtubules and controls the targeting of axons. Neuron, 39(5), 779-91. [PubMed:12948445] [WorldCat] [DOI] - ↑
Jay, D.G. (2000).
The clutch hypothesis revisited: ascribing the roles of actin-associated proteins in filopodial protrusion in the nerve growth cone. Journal of neurobiology, 44(2), 114-25. [PubMed:10934316] [WorldCat] - ↑
Diefenbach, T.J., Latham, V.M., Yimlamai, D., Liu, C.A., Herman, I.M., & Jay, D.G. (2002).
Myosin 1c and myosin IIB serve opposing roles in lamellipodial dynamics of the neuronal growth cone. The Journal of cell biology, 158(7), 1207-17. [PubMed:12356865] [PMC] [WorldCat] [DOI] - ↑
Medeiros, N.A., Burnette, D.T., & Forscher, P. (2006).
Myosin II functions in actin-bundle turnover in neuronal growth cones. Nature cell biology, 8(3), 215-26. [PubMed:16501565] [WorldCat] [DOI] - ↑
Shimada, T., Toriyama, M., Uemura, K., Kamiguchi, H., Sugiura, T., Watanabe, N., & Inagaki, N. (2008).
Shootin1 interacts with actin retrograde flow and L1-CAM to promote axon outgrowth. The Journal of cell biology, 181(5), 817-29. [PubMed:18519736] [PMC] [WorldCat] [DOI] - ↑
Nishimura, K., Yoshihara, F., Tojima, T., Ooashi, N., Yoon, W., Mikoshiba, K., ..., & Kamiguchi, H. (2003).
L1-dependent neuritogenesis involves ankyrinB that mediates L1-CAM coupling with retrograde actin flow. The Journal of cell biology, 163(5), 1077-88. [PubMed:14657231] [PMC] [WorldCat] [DOI] - ↑
Marsick, B.M., San Miguel-Ruiz, J.E., & Letourneau, P.C. (2012).
Activation of ezrin/radixin/moesin mediates attractive growth cone guidance through regulation of growth cone actin and adhesion receptors. The Journal of neuroscience : the official journal of the Society for Neuroscience, 32(1), 282-96. [PubMed:22219290] [PMC] [WorldCat] [DOI] - ↑
Kamiguchi, H., & Lemmon, V. (2000).
Recycling of the cell adhesion molecule L1 in axonal growth cones. The Journal of neuroscience : the official journal of the Society for Neuroscience, 20(10), 3676-86. [PubMed:10804209] [PMC] [WorldCat] - ↑
Kamiguchi, H., & Yoshihara, F. (2001).
The role of endocytic l1 trafficking in polarized adhesion and migration of nerve growth cones. The Journal of neuroscience : the official journal of the Society for Neuroscience, 21(23), 9194-203. [PubMed:11717353] [PMC] [WorldCat] - ↑
Dickson, B.J. (2002).
Molecular mechanisms of axon guidance. Science (New York, N.Y.), 298(5600), 1959-64. [PubMed:12471249] [WorldCat] [DOI] - ↑
Song, H.J., & Poo, M.M. (1999).
Signal transduction underlying growth cone guidance by diffusible factors. Current opinion in neurobiology, 9(3), 355-63. [PubMed:10395576] [WorldCat] [DOI] - ↑
Serafini, T., Colamarino, S.A., Leonardo, E.D., Wang, H., Beddington, R., Skarnes, W.C., & Tessier-Lavigne, M. (1996).
Netrin-1 is required for commissural axon guidance in the developing vertebrate nervous system. Cell, 87(6), 1001-14. [PubMed:8978605] [WorldCat] [DOI] - ↑
Barallobre, M.J., Pascual, M., Del Río, J.A., & Soriano, E. (2005).
The Netrin family of guidance factors: emphasis on Netrin-1 signalling. Brain research. Brain research reviews, 49(1), 22-47. [PubMed:15960985] [DOI] - ↑
Hong, K., Hinck, L., Nishiyama, M., Poo, M.M., Tessier-Lavigne, M., & Stein, E. (1999).
A ligand-gated association between cytoplasmic domains of UNC5 and DCC family receptors converts netrin-induced growth cone attraction to repulsion. Cell, 97(7), 927-41. [PubMed:10399920] [WorldCat] [DOI] - ↑
Tamagnone, L., & Comoglio, P.M. (2000).
Signalling by semaphorin receptors: cell guidance and beyond. Trends in cell biology, 10(9), 377-83. [PubMed:10932095] [WorldCat] - ↑
Taniguchi, M., Yuasa, S., Fujisawa, H., Naruse, I., Saga, S., Mishina, M., & Yagi, T. (1997).
Disruption of semaphorin III/D gene causes severe abnormality in peripheral nerve projection. Neuron, 19(3), 519-30. [PubMed:9331345] [WorldCat] [DOI] - ↑
Takahashi, T., Fournier, A., Nakamura, F., Wang, L.H., Murakami, Y., Kalb, R.G., ..., & Strittmatter, S.M. (1999).
Plexin-neuropilin-1 complexes form functional semaphorin-3A receptors. Cell, 99(1), 59-69. [PubMed:10520994] [WorldCat] [DOI] - ↑
Dubkin, B.P., Govorunov, G.V., & Kreĭndlin, I.u.Z. (1977).
[Reconstructive operation of the vessels in ischemia of the lower extremities]. Rekonstruktivnye operatsii na sosudakh pri ishemii nizhnikh konechnosteĭ Khirurgiia, (1), 36-40. [PubMed:846113] [WorldCat] - ↑
Tear, G., Harris, R., Sutaria, S., Kilomanski, K., Goodman, C.S., & Seeger, M.A. (1996).
commissureless controls growth cone guidance across the CNS midline in Drosophila and encodes a novel membrane protein. Neuron, 16(3), 501-14. [PubMed:8785048] [WorldCat] [DOI] - ↑
Flanagan, J.G., & Vanderhaeghen, P. (1998).
The ephrins and Eph receptors in neural development. Annual review of neuroscience, 21, 309-45. [PubMed:9530499] [WorldCat] [DOI] - ↑
Augsburger, A., Schuchardt, A., Hoskins, S., Dodd, J., & Butler, S. (1999).
BMPs as mediators of roof plate repulsion of commissural neurons. Neuron, 24(1), 127-41. [PubMed:10677032] [WorldCat] [DOI] - ↑
Charron, F., Stein, E., Jeong, J., McMahon, A.P., & Tessier-Lavigne, M. (2003).
The morphogen sonic hedgehog is an axonal chemoattractant that collaborates with netrin-1 in midline axon guidance. Cell, 113(1), 11-23. [PubMed:12679031] [WorldCat] [DOI] - ↑
Huang, E.J., & Reichardt, L.F. (2001).
Neurotrophins: roles in neuronal development and function. Annual review of neuroscience, 24, 677-736. [PubMed:11520916] [PMC] [WorldCat] [DOI] - ↑
Gundersen, R.W., & Barrett, J.N. (1979).
Neuronal chemotaxis: chick dorsal-root axons turn toward high concentrations of nerve growth factor. Science (New York, N.Y.), 206(4422), 1079-80. [PubMed:493992] [WorldCat] [DOI] - ↑
Tucker, K.L., Meyer, M., & Barde, Y.A. (2001).
Neurotrophins are required for nerve growth during development. Nature neuroscience, 4(1), 29-37. [PubMed:11135642] [WorldCat] [DOI] - ↑
Lowery, L.A., & Van Vactor, D. (2009).
The trip of the tip: understanding the growth cone machinery. Nature reviews. Molecular cell biology, 10(5), 332-43. [PubMed:19373241] [PMC] [WorldCat] [DOI] - ↑
Myers, J.P., & Gomez, T.M. (2011).
Focal adhesion kinase promotes integrin adhesion dynamics necessary for chemotropic turning of nerve growth cones. The Journal of neuroscience : the official journal of the Society for Neuroscience, 31(38), 13585-95. [PubMed:21940449] [PMC] [WorldCat] [DOI] - ↑
Ming, G.L., Song, H.J., Berninger, B., Holt, C.E., Tessier-Lavigne, M., & Poo, M.M. (1997).
cAMP-dependent growth cone guidance by netrin-1. Neuron, 19(6), 1225-35. [PubMed:9427246] [WorldCat] [DOI] - ↑
Song, H.J., Ming, G.L., & Poo, M.M. (1997).
cAMP-induced switching in turning direction of nerve growth cones. Nature, 388(6639), 275-9. [PubMed:9230436] [WorldCat] [DOI] - ↑
Song, H., Ming, G., He, Z., Lehmann, M., McKerracher, L., Tessier-Lavigne, M., & Poo, M. (1998).
Conversion of neuronal growth cone responses from repulsion to attraction by cyclic nucleotides. Science (New York, N.Y.), 281(5382), 1515-8. [PubMed:9727979] [WorldCat] [DOI] - ↑
Nishiyama, M., Hoshino, A., Tsai, L., Henley, J.R., Goshima, Y., Tessier-Lavigne, M., ..., & Hong, K. (2003).
Cyclic AMP/GMP-dependent modulation of Ca2+ channels sets the polarity of nerve growth-cone turning. Nature, 423(6943), 990-5. [PubMed:12827203] [WorldCat] [DOI] - ↑
Zheng, J.Q. (2000).
Turning of nerve growth cones induced by localized increases in intracellular calcium ions. Nature, 403(6765), 89-93. [PubMed:10638759] [WorldCat] [DOI] - ↑
Tojima, T., Hines, J.H., Henley, J.R., & Kamiguchi, H. (2011).
Second messengers and membrane trafficking direct and organize growth cone steering. Nature reviews. Neuroscience, 12(4), 191-203. [PubMed:21386859] [PMC] [WorldCat] [DOI] - ↑
Henley, J.R., Huang, K.H., Wang, D., & Poo, M.M. (2004).
Calcium mediates bidirectional growth cone turning induced by myelin-associated glycoprotein. Neuron, 44(6), 909-16. [PubMed:15603734] [PMC] [WorldCat] [DOI] - ↑
Ooashi, N., Futatsugi, A., Yoshihara, F., Mikoshiba, K., & Kamiguchi, H. (2005).
Cell adhesion molecules regulate Ca2+-mediated steering of growth cones via cyclic AMP and ryanodine receptor type 3. The Journal of cell biology, 170(7), 1159-67. [PubMed:16172206] [PMC] [WorldCat] [DOI] - ↑
Wen, Z., Guirland, C., Ming, G.L., & Zheng, J.Q. (2004).
A CaMKII/calcineurin switch controls the direction of Ca(2+)-dependent growth cone guidance. Neuron, 43(6), 835-46. [PubMed:15363394] [WorldCat] [DOI] - ↑
Tojima, T., Hines, J.H., Henley, J.R., & Kamiguchi, H. (2011).
Second messengers and membrane trafficking direct and organize growth cone steering. Nature reviews. Neuroscience, 12(4), 191-203. [PubMed:21386859] [PMC] [WorldCat] [DOI] - ↑
Tojima, T., Itofusa, R., & Kamiguchi, H. (2010).
Asymmetric clathrin-mediated endocytosis drives repulsive growth cone guidance. Neuron, 66(3), 370-7. [PubMed:20471350] [WorldCat] [DOI] - ↑
Campbell, D.S., & Holt, C.E. (2001).
Chemotropic responses of retinal growth cones mediated by rapid local protein synthesis and degradation. Neuron, 32(6), 1013-26. [PubMed:11754834] [WorldCat] [DOI] - ↑
Jung, H., O'Hare, C.M., & Holt, C.E. (2011).
Translational regulation in growth cones. Current opinion in genetics & development, 21(4), 458-64. [PubMed:21530230] [PMC] [WorldCat] [DOI] - ↑
Tcherkezian, J., Brittis, P.A., Thomas, F., Roux, P.P., & Flanagan, J.G. (2010).
Transmembrane receptor DCC associates with protein synthesis machinery and regulates translation. Cell, 141(4), 632-44. [PubMed:20434207] [PMC] [WorldCat] [DOI] - ↑
Yao, J., Sasaki, Y., Wen, Z., Bassell, G.J., & Zheng, J.Q. (2006).
An essential role for beta-actin mRNA localization and translation in Ca2+-dependent growth cone guidance. Nature neuroscience, 9(10), 1265-73. [PubMed:16980965] [WorldCat] [DOI] - ↑
Han, L., Wen, Z., Lynn, R.C., Baudet, M.L., Holt, C.E., Sasaki, Y., ..., & Zheng, J.Q. (2011).
Regulation of chemotropic guidance of nerve growth cones by microRNA. Molecular brain, 4, 40. [PubMed:22051374] [PMC] [WorldCat] [DOI]
(執筆者:森 達也、上口裕之 担当編集委員:林 康紀)